【2026年最新】放線冠と内包の違いとは?ラクナ梗塞の解剖・症状・リハビリを徹底解説
「放線冠で梗塞が起きた」「内包の損傷がある」——脳卒中リハビリの現場でよく耳にするこの2つの部位は、どちらも運動麻痺の主要原因となります。しかし構造の広がり・線維の密度・損傷時の症状パターン・リハビリの方向性は根本的に異なります。「放線冠と内包の違いは?」「なぜ内包の小さな梗塞で広範な麻痺が起きるの?」「神経可塑性で迂回路は本当に形成されるの?」「ラクナ梗塞後のリハビリはいつ始めるべきか?」——この記事ではこれらの疑問に、解剖学・最新エビデンス・臨床の3つの視点から徹底的にお答えします。
放線冠・内包・ラクナ梗塞の解剖と臨床を動画で確認できます。
放線冠(Corona Radiata)は大脳皮質から内包にかけて扇形に広がる白質線維帯、内包(Internal Capsule)はその線維が高密度に集約される皮質下深部構造です。脳深部の穿通枝動脈閉塞による15mm未満のラクナ梗塞はこれらの部位に好発し、純粋運動麻痺・運動失調性片麻痺・不器用手構音障害などの「ラクナ症候群」を引き起こします。適切なリハビリによって脳の「神経可塑性(neuroplasticity)」を最大限に引き出すことが機能回復の鍵です。放線冠梗塞後に皮質脊髄路が病変を迂回して再構成された症例がDTI画像で確認されています(Jang SH, 2015)。
- 放線冠(Corona Radiata):大脳皮質直下〜内包上縁にかけて扇形に広がる白質線維帯。皮質脊髄路・視床皮質路・前頭橋路などが混在。「広さ」が症状の多様性と神経可塑性の両方に影響
- 内包(Internal Capsule):放線冠が収束した高密度の皮質下構造。前脚・膝部・後脚の3区画に機能が分かれ、わずか数mmの梗塞でも広範な片麻痺が起きやすい
- 内包後脚の体部位局在:前内方に顔面・上肢、後外方に下肢の皮質脊髄路が配列。この局在性が「少量の病変でも上下肢対称麻痺を来す」機序
- ラクナ梗塞:穿通枝動脈閉塞による15mm未満の小梗塞。内包・放線冠・被殻・視床・橋に好発。日本の脳卒中全体の30〜40%を占める
- 最多原因:慢性高血圧による穿通枝脂肪変性(lipohyalinosis)が約60〜70%。糖尿病・高脂血症・喫煙が促進因子
- 代表的ラクナ症候群(Fisher CM, 1982):①純粋運動麻痺(内包後脚)②運動失調性片麻痺(内包後脚・放線冠・橋※複数部位が原因となりうる)③不器用手・構音障害(内包膝部)④純粋感覚障害(視床)⑤感覚運動脳卒中
- ⚠️ 「症候群名=病変部位」の単純公式は成立しない:「運動失調性片麻痺=内包後脚」ではない。必ずMRI所見との照合が必要
- リハビリの科学的根拠:神経可塑性(neuroplasticity)。反復性・特異性・難度漸増が3大原則。AVERT試験(Lancet 2015):発症24時間以内の高強度動員は転帰悪化の可能性あり。開始時期・強度は専門家が個別判断
- 最新エビデンス(Jang SH, 2015):放線冠梗塞後にDTI画像で皮質脊髄路の迂回路形成を確認。完全麻痺(MMT0・MEP誘発不能)から10週で抗重力活動が回復
- 再発予防の最重要課題:収縮期血圧130mmHg未満の管理。抗血小板薬継続・血糖脂質管理・禁煙・有酸素運動
放線冠・内包とは ― 解剖学的概要と臨床的役割
放線冠と内包はどちらも大脳深部の白質・皮質下構造に位置し、大脳皮質と脳幹・脊髄・視床をつなぐ重要な神経線維の「幹線道路」です。脳卒中リハビリに携わるPT・OT・STにとって、この2つの構造の違いを正確に理解することは、症状の説明・予後予測・リハビリ計画の個別設計において不可欠な基礎知識です。
🔬 なぜ放線冠・内包がリハビリで重要なのか ― 4つの理由
① 運動麻痺の主要原因部位:脳卒中後の片麻痺の多くは、皮質脊髄路(錐体路)が通過する内包後脚または放線冠の損傷によって生じます。病変の正確な部位把握が予後予測の精度を高めます。
② ラクナ梗塞の好発部位:穿通枝動脈が豊富に分布するこれらの領域は、高血圧・糖尿病に起因するラクナ梗塞が最も集積する部位です。
③ 症状パターンと病変部位の対応:内包の3区画(前脚・膝部・後脚)と放線冠のどの部位が損傷しているかによって、優先すべきリハビリの種類(PT/OT/ST)が異なります。
④ 神経可塑性の舞台:放線冠は白質スペースが広く、梗塞後の皮質脊髄路迂回路が形成されやすい構造的特性があります(Jang SH, 2015)。リハビリが神経回路の再編成を促す科学的根拠がここにあります。
放線冠(Corona Radiata)― 扇形に広がる白質線維帯
放線冠(英:Corona Radiata、直訳「放射冠」)とは、大脳皮質直下から内包の上縁にかけて扇形に広がる白質神経線維群の総称です。ラテン語で「corona(冠)」「radiata(放射状の)」を意味し、大脳皮質を扇形に包むように広がる形状から命名されました。「特定の1本の神経線維路」ではなく、複数の線維路が混在した白質領域の解剖学的名称であることを理解することが重要です。
放線冠の位置・構造・通過する主な線維路
| 通過する主な線維路 | 機能・損傷時の症状 |
|---|---|
| 皮質脊髄路(錐体路) | 随意運動を上下肢・体幹へ伝える主経路。損傷→対側片麻痺(上下肢) |
| 皮質延髄路 | 顔面・口・舌・嚥下への随意運動線維。損傷→顔面麻痺・嚥下障害・構音障害 |
| 視床皮質路(後部) | 視床から感覚情報を大脳皮質へ送る求心路。損傷→対側の感覚障害 |
| 前頭橋路・側頭橋路 | 大脳皮質から橋・小脳への経路。損傷→運動協調性障害(失調様症状) |
| 脳梁からの交連線維 | 左右半球間の情報伝達。放線冠前部で混在 |
内包(Internal Capsule)― 3区画の機能と損傷症状
内包(英:Internal Capsule)は、放線冠から収束してきた運動・感覚の投射線維が極めて高密度に集まる皮質下の深部構造です。尾状核と被殻(外側)・視床(内側)に挟まれた位置にあり、大脳皮質→脳幹・脊髄への遠心性線維と、視床→大脳皮質への求心性線維が同時に通過する「神経線維のハイウェイ合流点」です。わずか数mmの梗塞でも広範な麻痺が起きやすいのは、この高密度構造が理由です。
前脚 内包前脚(Anterior Limb)― 前頭橋路・前視床放線
| 損傷時の症状 | 詳細・臨床的注意点 |
|---|---|
| 構音障害(軽度) | 発話の軽度不明瞭化。「不器用手・構音障害症候群」の一構成要素として現れることがある |
| 認知・情動変化 | 注意機能・遂行機能・情動制御の変化。「以前と比べて段取りが悪い」「感情が不安定」として現れやすい |
| 協調運動障害 | 前頭橋路損傷による小脳症状様の協調運動障害が軽度に出現することがある |
膝部 内包膝部(Genu)― 皮質延髄路の主要通過点
| 損傷時の症状 | 詳細・臨床的注意点 |
|---|---|
| 顔面麻痺(中枢性) | 下顔面の麻痺(UMN型)。口周囲・頬の動きが不良。額ひだは両側皮質支配のため比較的保たれる |
| 構音障害 | 口周囲筋・舌の随意運動障害による発話不明瞭化。NIHSSで1〜2点 |
| 嚥下障害 | 両側性の皮質延髄路損傷(偽性球麻痺)で特に重篤になる。誤嚥性肺炎リスク急増 |
| 手の不器用さ | 「不器用手・構音障害症候群」の一要素。細かい動作(箸・ボタン等)の拙劣化 |
後脚 内包後脚(Posterior Limb)― ⚠️ 臨床的に最重要の区画
| 損傷時の症状 | 詳細・臨床的注意点 |
|---|---|
| 片麻痺(対側) | 顔面・上肢・下肢の対側片麻痺。感覚は保たれることも(純粋運動麻痺の典型例) |
| 感覚障害(後部) | 視床皮質路も通過するため、後脚後部の損傷で触覚・深部感覚の障害が合併 |
| 運動失調性片麻痺 | 麻痺と失調が合併する症候群。橋基底部・放線冠も同様の症候群を呈するためMRI所見との照合が必須 |
⚠️ 内包後脚の「体部位局在」が生む臨床的重要性
内包後脚では皮質脊髄路が体部位局在的(somatotopically)に配列しています。顔面・上肢の線維は前内方、下肢の線維は後外方に位置します。
① 後脚前内方の小梗塞 → 顔面・上肢優位の麻痺(下肢は軽度)
② 後脚後外方の梗塞 → 下肢優位の麻痺
③ 後脚全体の大きな病変 → 顔面・上下肢すべてに等しい完全片麻痺(純粋運動麻痺の典型)
この体部位局在を理解することで「なぜこの患者は下肢よりも手の麻痺が強いのか」に解剖学的根拠から答えられ、PT(主に下肢・歩行)とOT(主に上肢・ADL)の介入優先度を合理的に設定できます。
専門家向け:内包の血液供給・ラクナ梗塞の病理機序詳細
血液供給の詳細:前脚は前大脳動脈の穿通枝(Heubner動脈など)、前脚〜膝部〜後脚前2/3は中大脳動脈のレンズ核線条体動脈が供給。後脚後部〜後肢の一部は前脈絡叢動脈(AChA)が担う。各穿通枝は直径100〜800μmと細く、側副血行路がほぼないため閉塞に脆弱。
脂肪変性(Lipohyalinosis):慢性高血圧によって穿通枝血管壁にフィブリノイド変性・脂肪変性が生じ、内腔が狭小化→閉塞に至る。ラクナ梗塞の最多原因(約60〜70%)。
微小アテローム(Microatheroma):穿通枝起始部へのアテローム性変化による閉塞。親動脈からのプラーク形成も含む。高脂血症・喫煙が主要危険因子。
塞栓性閉塞:心原性または大動脈弓由来の塞栓が穿通枝を閉塞する場合。比較的まれだが「ラクナ梗塞様」所見を呈することがあり、病因特定(→抗凝固 vs 抗血小板の選択)がリスク管理上重要。
DTIと予後予測:拡散テンソル画像(DTI)での皮質脊髄路のFractional Anisotropy(FA)値患健比(rFA)が回復予測の参考値として用いられる。Stinear CM(2017)のPREP2アルゴリズムはrFAを用いた上肢機能回復予測ツールとして有用性が報告されている。
放線冠 vs 内包:徹底比較とリハビリへの影響
| 比較項目 | 放線冠(Corona Radiata) | 内包(Internal Capsule) |
|---|---|---|
| 構造的特徴 | 扇形に広がる白質線維帯。皮質直下〜内包上縁の広い領域 | 線維が高密度に集中した皮質下深部構造。前脚・膝部・後脚の3区画 |
| 主な通過線維 | 皮質脊髄路・皮質延髄路・視床皮質路・前頭橋路などが混在 | 同上の線維が3区画に高密度集積。体部位局在的に配列 |
| 小さな梗塞での影響 | 障害される線維が限局しやすく症状が部分的なことも | わずか数mmでも顔面・上下肢の広範麻痺が起きやすい |
| 症状の多様性 | 病変部位・大きさによって症状が多様(運動・感覚・複合) | 3区画に対応した比較的特徴的な症候群(前脚:認知、膝部:嚥下/構音、後脚:片麻痺) |
| ラクナ梗塞との関係 | 好発部位の一つ。多発WMLで認知機能・歩行速度にも影響 | 最も典型的なラクナ梗塞好発部位(特に後脚) |
| 血液供給 | 中大脳動脈皮質枝・白質枝、前大脳動脈分枝 | レンズ核線条体動脈(MCA分枝)・前脈絡叢動脈・Heubner動脈(ACA分枝) |
| 神経可塑性・迂回路形成 | 白質スペースが広く迂回路を形成しやすい(Jang SH, 2015で確認) | 線維密度が高く迂回スペースが限られる。ただし再構成の報告あり |
| リハビリの重点 | 症状の多様性に応じた個別設計。高次脳機能も評価対象 | 区画に応じた優先順位(後脚→PT主体、膝部→ST主体、前脚→高次脳機能) |
| NIHSS上の特徴 | 広範病変では複数項目が上昇。高次脳機能障害はNIHSSで評価されにくい | 後脚:運動項目(5/6)が主に上昇。膝部:構音(10)・顔面(4)が上昇 |
⚠️ 放線冠・内包のリハビリを設計する際の3大注意点
① 「症候群名=病変部位」という単純公式は成立しない:「運動失調性片麻痺=内包後脚」とは限りません。橋基底部・放線冠・小脳脚も同様の症候群を呈します。必ずMRI所見と臨床症状を照合してください。
② 多発ラクナ梗塞の見落とし:「新しい梗塞」1か所だけに注目すると、それ以前から蓄積している放線冠の慢性白質病変(WML)が引き起こす認知機能低下・歩行障害・転倒リスクを見落とします。初回評価時に頭部MRI全体(FLAIR画像)を確認し、白質病変の範囲を把握してください。
③ 「早期リハビリ」と「超早期高強度動員」の混同:「早期離床は大切」は正しい。しかし「発症直後から高強度で動かすほど良い」は誤りです(AVERT試験 2015)。開始時期と強度の判断は担当医・リハビリ専門職が行います(→詳細はPART 7参照)。
ラクナ梗塞 ― 深部小梗塞の病理・症候群・危険因子
ラクナ梗塞(Lacunar infarction)とは、脳深部の穿通枝動脈(直径100〜800μm)が閉塞することで生じる、直径15mm未満の小梗塞です。「ラクナ(lacuna)」はラテン語で「小さな穴・湖」を意味し、慢性期に病変が液状化してMRI上に小腔隙(ラクン)が形成されることに由来します。
ラクナ梗塞の3つの病理機序
脂肪変性(Lipohyalinosis)― 最多原因(約60〜70%)
微小アテローム(Microatheroma)
塞栓性閉塞(心原性・大動脈弓由来)― 除外が必須
代表的なラクナ症候群 ― 症状から病変部位の手がかりをつかむ
① 純粋運動麻痺(PMH)
顔面・上肢・下肢の対側片麻痺。感覚障害なし。
主な部位:内包後脚、放線冠、橋基底部
② 運動失調性片麻痺(AHM)
麻痺と同側の協調運動障害が合併。
主な部位:内包後脚、放線冠、橋基底部(複数部位が原因となりうる)
③ 不器用手・構音障害(CHD)
手の巧緻性低下と発話不明瞭化。
主な部位:内包膝部〜前脚、橋基底部
④ 純粋感覚障害(PSS)
対側の感覚障害のみ(運動麻痺なし)。
主な部位:視床(腹後外側核 VPL)
⑤ 感覚運動脳卒中(SMS)
麻痺と感覚障害が同側に合併。
主な部位:内包後脚〜視床境界部
⑥ その他・非典型例
半側舞踏運動・視床性痛・構音障害単独・認知変化単独など。上記5分類に収まらないケースも多い。
⚠️ 「症候群名で病変部位を断定しない」ことの重要性
「運動失調性片麻痺=内包後脚の病変」という単純な等式は成立しません。同じ症候群でも放線冠・橋基底部・小脳脚など複数の部位が原因となりえます。臨床の現場では症候群名を「仮説」として用いつつ、必ずMRI拡散強調像(DWI)で病変の確認・局在を確定してください。「症候群名で病変部位を断定し、MRIを省略する」ことは診断ミスにつながります。
MRI画像所見 ― 病変の確認と局在診断
MRI画像で病変の位置と広がりを把握することは、症状の解釈・予後予測・リハビリ計画の立案に直結します。
📊 放線冠・内包・ラクナ梗塞のMRI評価の基本
DWI(拡散強調像):急性期梗塞の検出に最も感度が高い。発症後数時間以内から梗塞巣が高信号(白く)描出される。急性期の病変部位確認に必須。
FLAIR(液体減衰反転回復法):亜急性〜慢性期の白質病変(WML)・陳旧性ラクナ梗塞の評価に適している。多発WMLの範囲・分布を確認する上で必須。
T1強調像・T2強調像:慢性期ラクナ梗塞はT1低信号・T2高信号の小腔隙として描出される。
DTI(拡散テンソル画像):白質線維路の走行・intact性を評価。放線冠梗塞後の皮質脊髄路迂回路形成の確認にも使用(Jang SH, 2015)。FA値患健比(rFA)が回復予測に活用される(Stinear CM, 2017:PREP2アルゴリズム)。
MRA(MR血管撮影):穿通枝の親動脈(中大脳動脈幹など)のアテローム・狭窄を確認。塞栓源の検索にも有用。
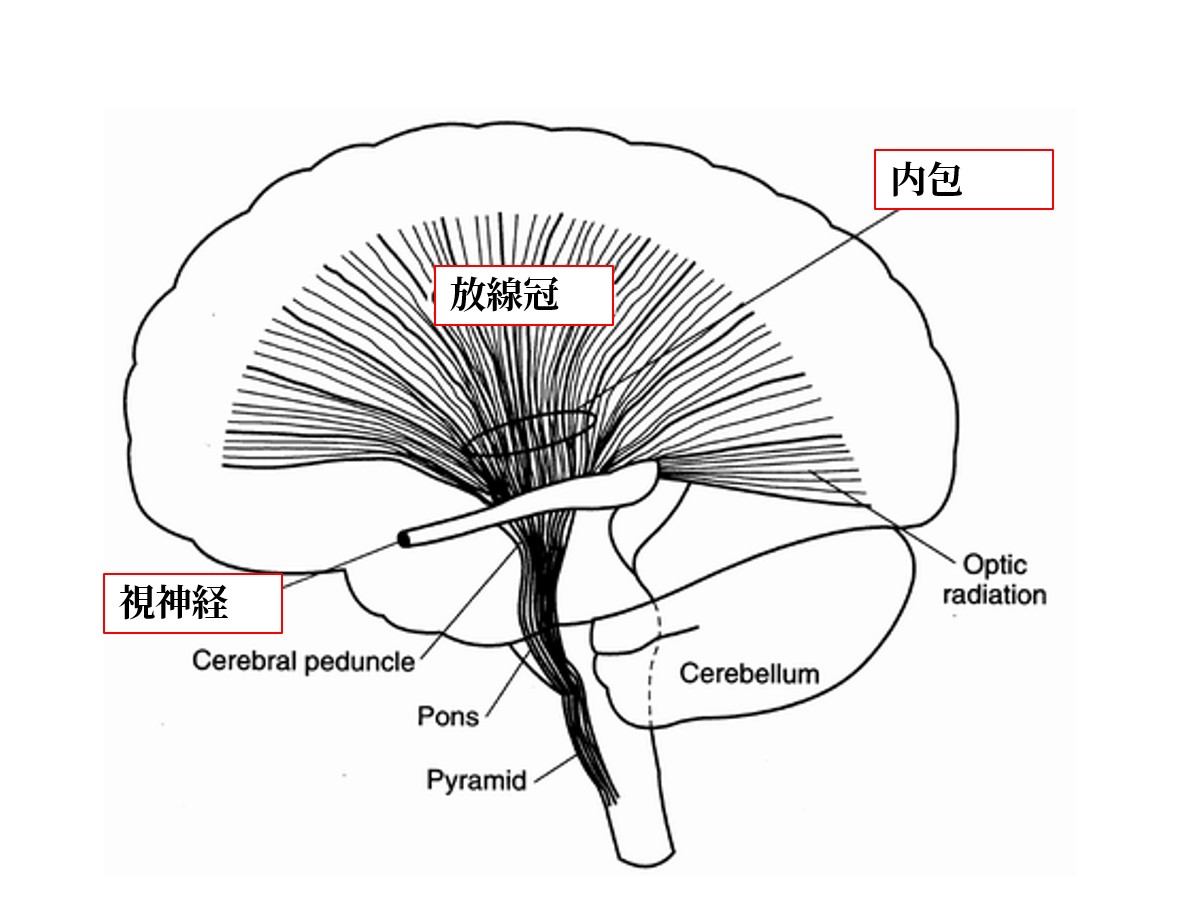 ▲ 大脳皮質〜内包にかけての神経線維走行イメージ
▲ 大脳皮質〜内包にかけての神経線維走行イメージ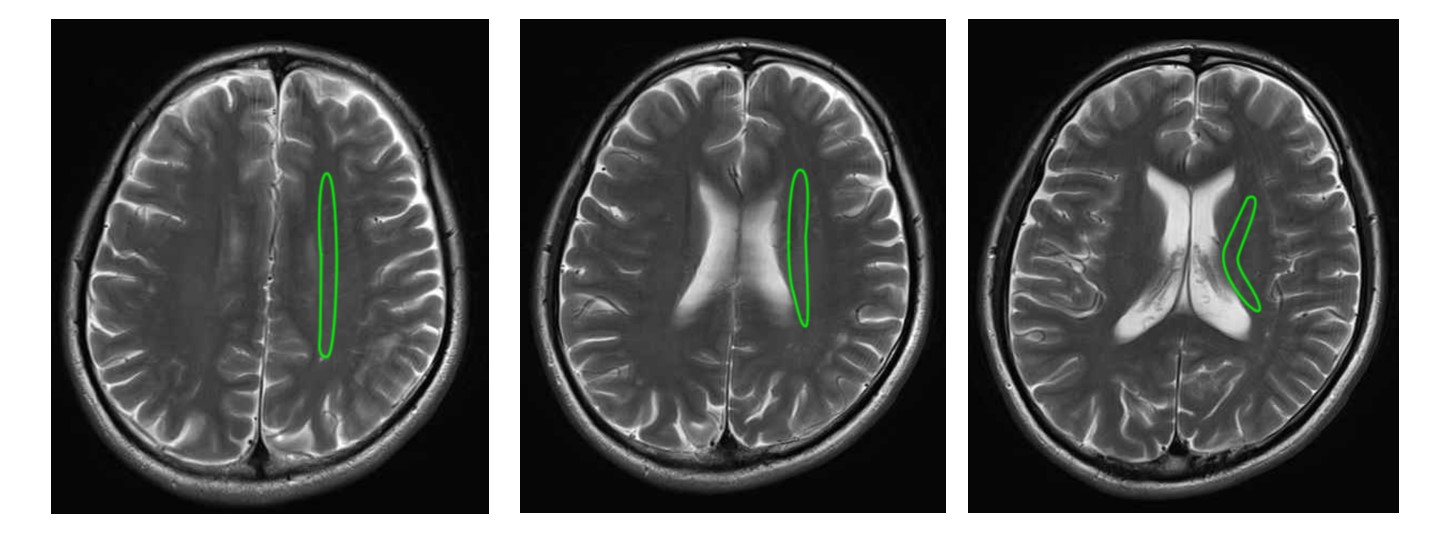 ▲ 放線冠のMRI所見(引用元:画像診断Cafe)
▲ 放線冠のMRI所見(引用元:画像診断Cafe)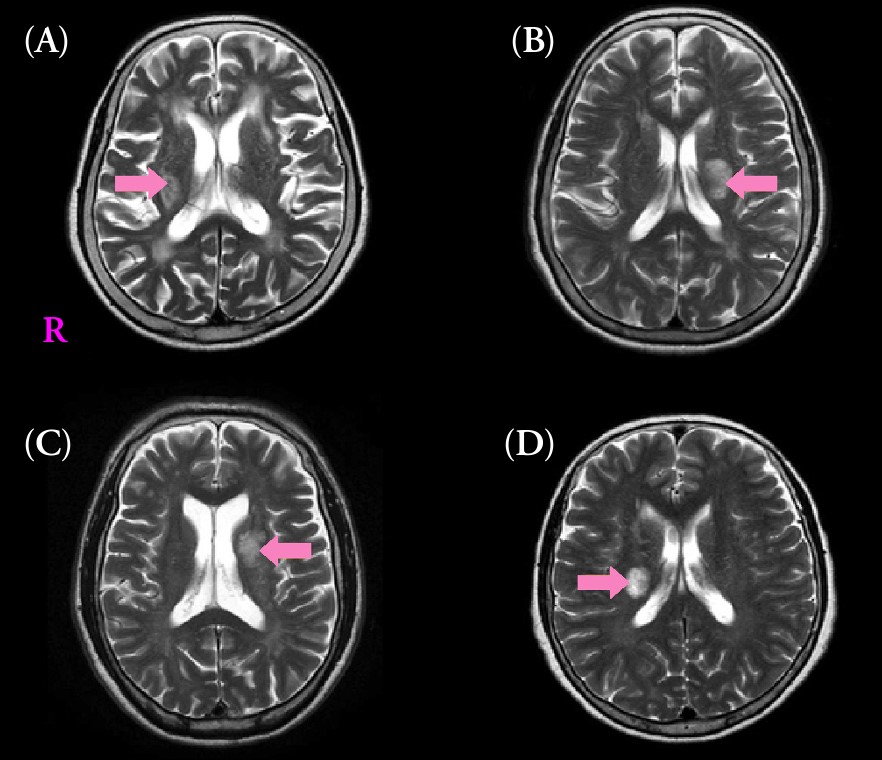 ▲ ラクナ梗塞の典型的MRI所見(点状〜小結節状の高信号域)
▲ ラクナ梗塞の典型的MRI所見(点状〜小結節状の高信号域)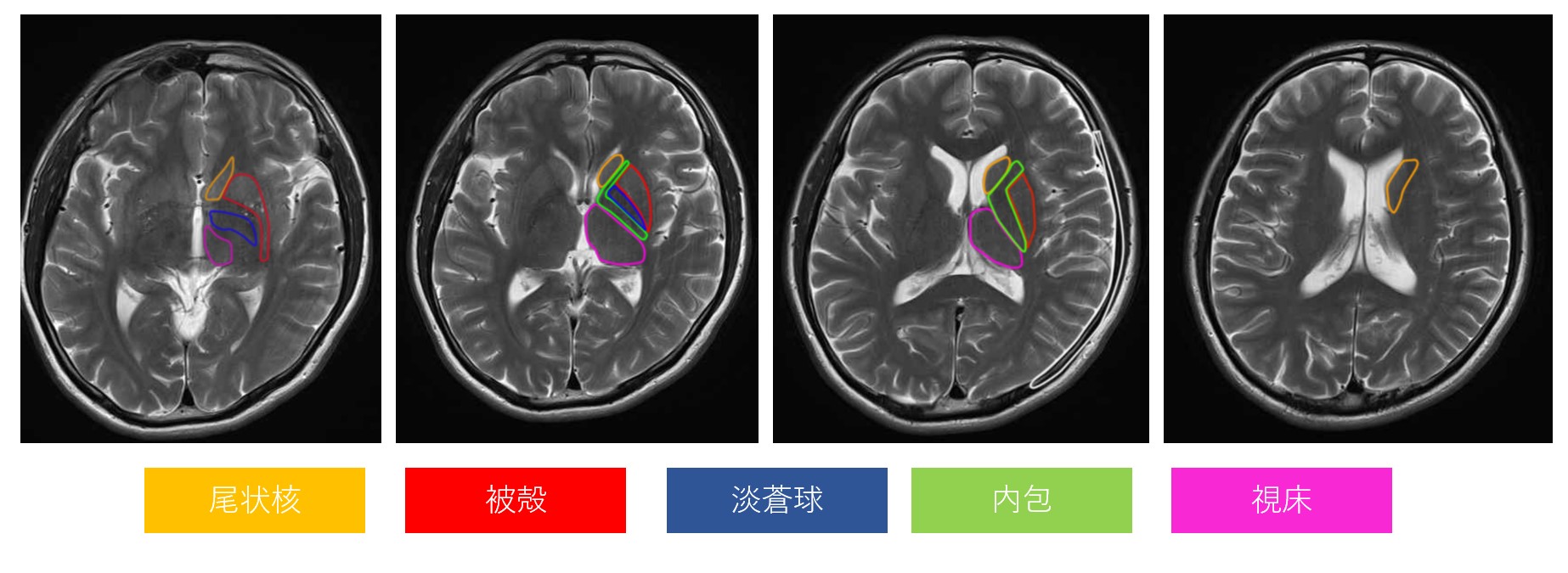 ▲ 大脳基底核周辺のMRI(引用元:画像診断Cafe)
▲ 大脳基底核周辺のMRI(引用元:画像診断Cafe)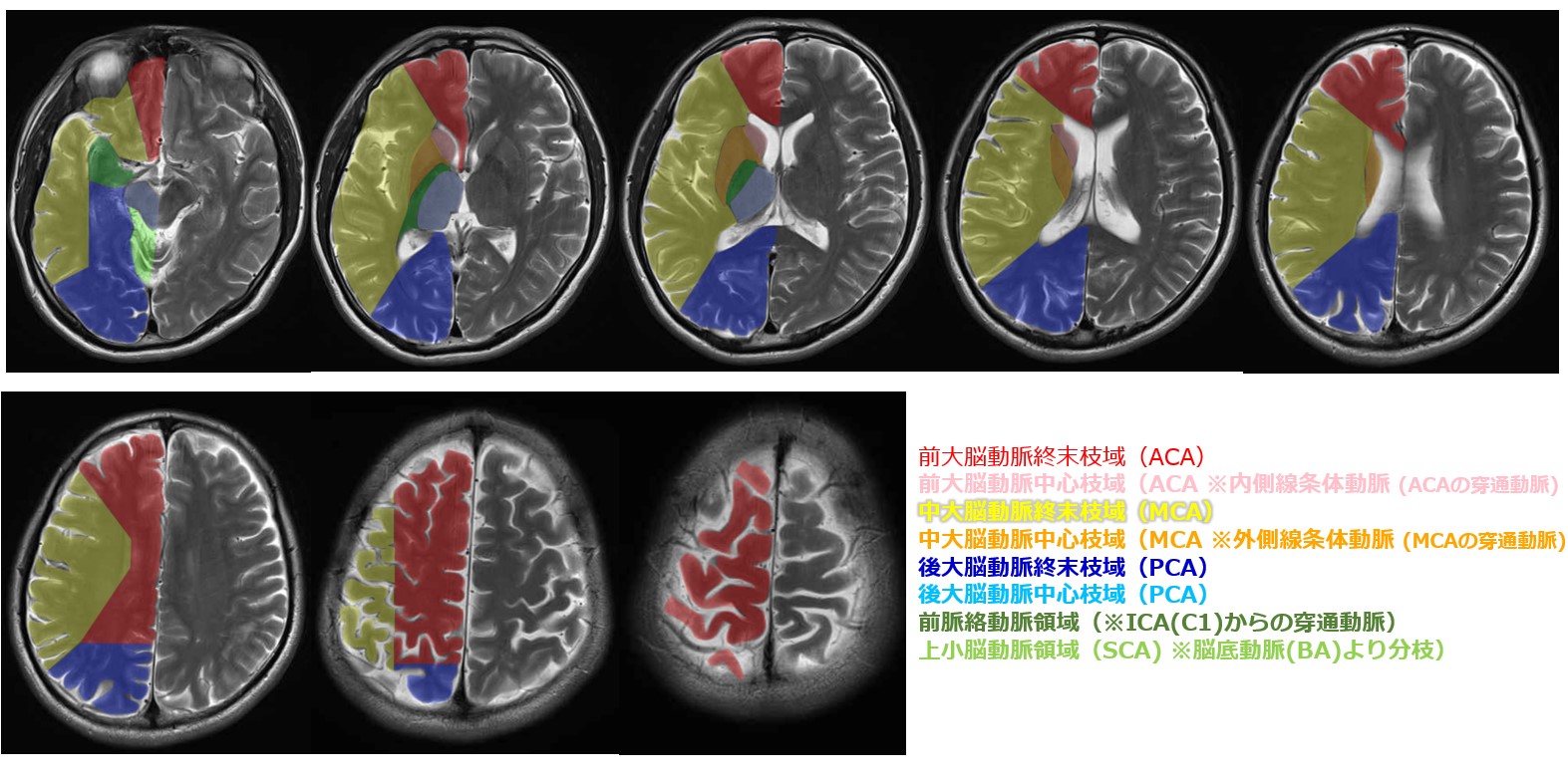 ▲ 内包周辺の血管支配(引用元:画像診断Cafe)
▲ 内包周辺の血管支配(引用元:画像診断Cafe)💡 MRI読影と臨床症状の照合:リハビリセラピストが知るべき3点
① DWI高信号の位置で「どの線維路が傷害されたか」を推定:内包後脚のどの区画に病変があるかで、上肢麻痺と下肢麻痺のどちらが強いかを事前に予測し、PT(下肢・歩行)とOT(上肢・ADL)の介入優先度を設定できます。
② FLAIR画像で白質病変の全体像を把握:「新しいラクナ梗塞」だけでなく、蓄積している白質病変の範囲が認知機能・歩行安全性に影響します。Fazekas scoreなどで白質病変の重症度を把握し、高次脳機能評価の必要性を判断してください。
③ DTIで皮質脊髄路のintact性を評価(高度専門施設):DTI tractographyによるFA値患健比(rFA)が回復予測の参考値として用いられています(PREP2アルゴリズム:Stinear CM, 2017)。発症早期の「回復の可能性を最大化するリハビリ」を目指す上で有用な情報です。
リハビリテーション ― 神経可塑性を引き出す実践的アプローチ
脳卒中リハビリの科学的根拠は「神経可塑性(Neuroplasticity)」にあります。脳が損傷を受けた後、反復的な刺激によって新しい神経回路を構築・強化していく能力のことで、刺激の量・質・タイミングが神経可塑性の発現を左右します。
🔑 神経可塑性を最大化する3大原則(すべてのリハビリに共通)
① 反復性(Repetition):同じ運動・感覚課題を繰り返すことで、使われるシナプスが強化される(ヘッブの法則:”neurons that fire together, wire together”)。1回1回の質だけでなく、十分な反復回数が重要。
② 特異性(Specificity):回復させたい機能に特化した課題が最も効果的(task-specific training)。「歩けるようになりたいなら歩く練習を」「手を使えるようにしたいなら手を使う練習を」。
③ 難度の漸増(Progressive challenge):現在の能力をわずかに超える難度の課題が脳を最も効率よく変化させる。簡単すぎる課題では神経可塑性は誘発されにくい。
⚠️ リハビリ開始時期の重要な注意:AVERT試験(Lancet 2015)の知見
大規模RCT(AVERT試験)では、発症後24時間以内の高頻度・高強度動員は転帰を改善しないどころか悪化させる可能性が示されました。現在のエビデンスでは:
・バイタルサイン安定後に体位変換・座位保持など低強度の介入から開始
・神経学的所見の安定を確認しながら段階的に強度を上げる
・リハビリ開始時期と強度は必ず担当医・リハビリ専門職が個別に判断する
「早期離床・早期リハビリ」と「超早期からの高強度動員」は区別して考えることが必要です。
回復の4フェーズとリハビリ目標
急性期(発症〜数日)― 二次障害の予防
関節拘縮・褥瘡・廃用症候群・DVT・誤嚥性肺炎を防ぐ。バイタル安定確認後に体位変換・座位保持から開始。積極的な筋力訓練は時期尚早。NIHSSで経時的に神経学的変化をモニタリング(4点以上増悪→緊急対応)。
回復初期(数日〜数週)― 正しい運動パターンの再学習
座位→立位→歩行と離床を段階的に進める。セラピストの補助のもと正しい筋収縮パターンを脳に反復入力。感覚再教育も並行して開始。内包後脚の損傷では「麻痺側の努力的な使用」が可塑性を促進(CI療法の原型)。
回復中期(数週〜数か月)― ADL自立度の向上・歩行の質的改善
筋力・バランス・協調性を統合した課題へ移行。難度を段階的に上げながら神経可塑性を促進。職場・家庭環境への応用訓練も開始。運動失調が前景に立つ場合はFrenkel体操・協調運動訓練を優先。
回復後期〜維持期(数か月〜)― 社会復帰・再発予防・QoL最大化
残存症状と長期的に付き合う方法の習得。血圧・血糖・服薬管理を通じた再発予防の徹底。必要に応じて補装具(短下肢装具・杖)・環境調整(手すり・段差解消)も実施。
病変部位別リハビリアプローチ
運動機能の回復 ― 内包後脚・放線冠の片麻痺・歩行障害に対して
純粋運動麻痺・運動失調性片麻痺など症状パターンに応じた運動課題を設計します。反復性・特異性・難度漸増の3原則のもと、歩行・立ち上がり・階段昇降・体幹安定性を段階的に改善。動画解析で歩行パターンを可視化して代償動作を修正し、運動失調が前景に立つ場合はFrenkel体操など協調運動訓練を優先します。内包後脚の体部位局在を把握して「どの筋群が最も麻痺しているか」を特定し、課題の優先順位を設定します。
ADLの再獲得と上肢巧緻性の回復 ― 内包後脚・放線冠の上肢障害・不器用手に対して
着替え・入浴・調理・書字など日常動作の段階的再獲得と上肢巧緻性向上を並行して進めます。不器用手・構音障害症候群(内包膝部〜前脚)では手指の細かい動きの再学習(箸・ボタン・PC操作)を重点的に行います。CI療法(Constraint-Induced Movement Therapy)の適応検討も有益です。高次脳機能障害(放線冠多発WMLによる注意・実行機能障害)が疑われる場合は神経心理学的評価(MoCA・TMT)を組み込みます。
構音・嚥下障害への対応 ― 内包膝部損傷で特に優先
内包膝部〜前脚の損傷では皮質延髄路が障害され、嚥下困難・発話の不明瞭化が主症状となります。嚥下機能の客観的評価(VF・VE)から食事形態の段階的調整、口周囲筋の強化訓練、発声・発音練習を系統立てて実施します。誤嚥性肺炎リスクの高い急性期ほど早期のST介入が重要であり、「内包膝部梗塞」とわかった段階でSTへの即座の依頼が推奨されます。
感覚障害の回復 ― 内包後脚後部・放線冠後部の視床皮質路損傷に対して
触覚・痛覚・固有感覚が低下した場合、異なる素材・温度・質感への接触刺激の反復によって体性感覚野の再配線を促します。固有感覚の低下はバランス・歩行・手の力加減に直接影響するため、運動訓練と並行した取り組みが重要です。グローブを用いた識別訓練・マッサージ・振動刺激なども感覚再教育の手段として活用します。
多発ラクナ梗塞・広範放線冠病変で見落とされやすい問題
放線冠の広範な白質病変や多発ラクナ梗塞では、注意機能・処理速度・実行機能などの高次脳機能障害が運動障害と合併・先行することがあります。「なんとなく段取りが悪い」「二つのことを同時にできない」といった訴えは高次脳機能障害のサインかもしれません。MMSE・MoCA・TMTなどを用いた神経心理学的評価と包括的アプローチが必要です。
上肢回復予測ツール:PREP2アルゴリズムとは
🔬 PREP2アルゴリズム(Stinear CM, 2017)― 上肢機能予後を発症7日以内に予測
PREP2(Predict Recovery Potential 2)は、発症後7日以内の評価データから上肢機能の6か月後予後を4段階で予測するアルゴリズムです(Stinear CM et al. Ann Clin Transl Neurol. 2017)。
| 予測カテゴリ | 6か月後の上肢機能 | 主な判定基準 |
|---|---|---|
| Complete(完全回復見込み) | ほぼ正常使用 | SAFE≥5点、または肩外転+手指伸展が可能 |
| Excellent(優秀回復見込み) | ADL自立レベル | TMS-MEP誘発可能+SAFE≥5 |
| Good(良好回復見込み) | 補助的使用 | TMS-MEP誘発可能+SAFE<5 |
| Limited(限定的回復) | 補助的使用も困難 | TMS-MEP誘発不能(皮質脊髄路断絶) |
SAFE:肩外転+手指伸展テスト(Shoulder Abduction and Finger Extension)。TMS:経頭蓋磁気刺激。rFA:拡散テンソル画像によるFA値患健比。
※PREP2はあくまで予測ツールであり、すべての患者に適用可能ではありません。最終的な判断は専門家が行います。
上肢回復を加速する先進アプローチ
CI療法(Constraint-Induced Movement Therapy)
非麻痺側の上肢をミトンやスリングで拘束しながら、麻痺側を強制的に使用させる集中的な行動療法。1日数時間・2週間程度の集中介入。
対象:上肢の残存運動機能がある程度ある場合(手指がわずかに動かせるレベル以上)。
エビデンス:複数の大規模RCT(Wolf et al. EXCITE Trial, JAMA 2006)で運動機能・ADL改善を確認。
ミラー療法(Mirror Therapy)
鏡の前で非麻痺側を動かし、鏡に映った映像を「麻痺側が動いている」と錯覚させる。ミラーニューロン系を活性化して運動野の再組織化を促す。
有効性:Cochrane review(Thieme H, 2018)で上肢機能・疼痛・日常生活動作の改善に有意な効果を確認。完全麻痺でも適応できる数少ない手法。
運動イメージ療法(Motor Imagery)
実際に動かさず「動かすイメージ」を繰り返すことで運動野・補足運動野を活性化。fMRI研究により、イメージと実際の運動が同一の神経基盤を共有することが実証されている。身体訓練と組み合わせることで相乗効果が得られる。
非侵襲的脳刺激(TMS・tDCS)
rTMS(反復経頭蓋磁気刺激)やtDCS(経頭蓋直流電気刺激)は、損傷半球の興奮性を高め、または健常半球の過剰抑制を軽減することで可塑性を促進。リハビリ直前に施行すると訓練効果が増強される(Priming効果)。本邦でも一部施設で実施中。
最新エビデンス ― 迂回路形成と神経可塑性の科学
放線冠・神経可塑性の最新解説動画
Jang SH et al. (2015) ― 放線冠梗塞後の皮質脊髄路迂回路形成をDTI画像で可視化
掲載誌:Neural Regeneration Research, 10(9):1428-1431 PubMed掲載ページ
放線冠梗塞後に「皮質脊髄路が病変を迂回して再構成されたこと」をDTI(拡散テンソル画像)で可視化した症例報告。神経可塑性がどのように回復に機能するかを画像で示した、臨床家・患者双方にとって希望となる研究です。
研究の3ステップ:完全麻痺から迂回路形成まで
症例:69歳・右利き女性、左放線冠梗塞 → 右片麻痺
発症後1週間のMRIで左放線冠に梗塞を確認。右上下肢はともに完全弛緩性麻痺(MMT:0)。TMS(経頭蓋磁気刺激)を最大出力100%で施行しても左半球からMEP(運動誘発電位)は誘発されず=皮質脊髄路が機能的に完全遮断された状態。
発症10週後:多くの筋でMMT3まで回復、左半球からMEP誘発に成功
右足部の筋(MMT:0のまま)を除き、右上下肢の多くの筋で抗重力活動が獲得(MMT:3)。10週後のTMSでは左半球刺激により右短母指外転筋でMEPが誘発=新たな皮質脊髄路の機能的接続が確立。
DTI(拡散テンソル画像)で迂回路を「可視化」
発症初期:左放線冠の皮質脊髄路が途絶。10週後:途絶した皮質脊髄路が放線冠の前部領域を迂回して上下方向に再接続した所見がDTI画像で確認された。
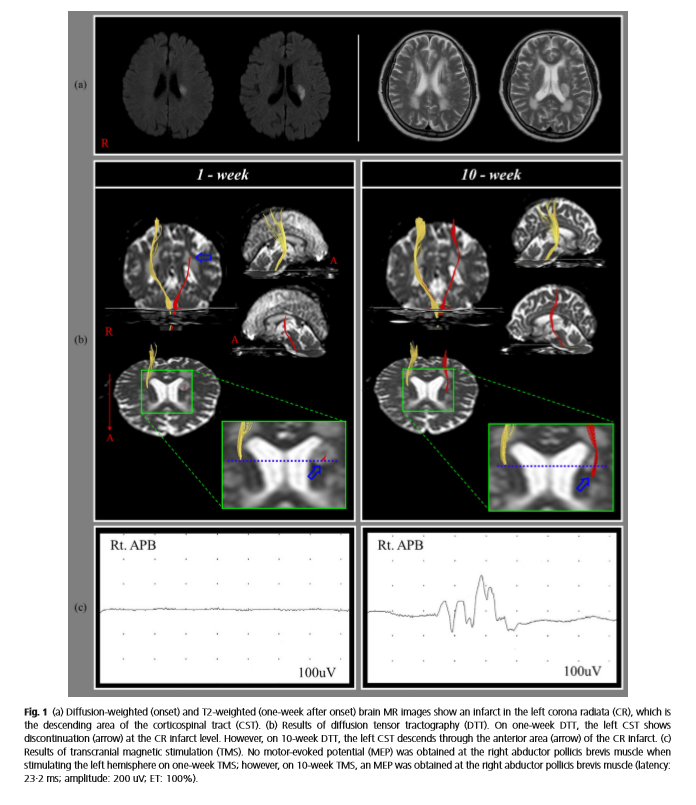 ▲ 放線冠前部を迂回した皮質脊髄路の再構成(DTI画像:Jang SH, 2015)
▲ 放線冠前部を迂回した皮質脊髄路の再構成(DTI画像:Jang SH, 2015)💡 この研究が臨床に示す3つの意義
① 「完全麻痺=回復しない」ではない:TMSでMEPが誘発されない完全遮断状態であっても、神経可塑性によって新たな経路が構築される可能性がある。発症早期の評価で「回復見込みなし」と結論づけることの危険性を示す。
② 放線冠の「広さ」が迂回路形成を可能にした:内包に比べ白質スペースが広い放線冠では、病変前部を活用した迂回路が形成されやすかったと考えられる。「病変の部位と構造の特性」がリハビリの可能性に影響することを示す。
③ 反復的リハビリが迂回路形成を促した可能性:10週間の積極的リハビリを通じた反復刺激が脳の再配線を促した。この知見を患者と共有することはリハビリへの動機づけとなり、治療同盟の強化につながります。
⚠️ エビデンスの解釈に関する重要な注意
Jang SH(2015)は単一症例報告です。すべての放線冠梗塞患者に同様の迂回路形成が起こることを保証するものではありません。回復の程度は病変の大きさ・部位・重症度・年齢・リハビリの質と量・全身状態など複数因子が関与します。「必ず回復する」ではなく、「神経可塑性の可能性を最大化するためのリハビリの価値」として理解してください。
ラクナ梗塞のリハビリ変化例
再発予防と生活管理 ― リハビリと並行して必ず取り組む
ラクナ梗塞は再発率が高い脳卒中病型です。再発するたびに障害が蓄積し、多発性ラクナ梗塞として認知機能・歩行機能・嚥下機能が複合的に低下する「血管性認知症」へと進行します。リハビリによる機能回復と並行して、再発予防の生活管理を徹底することが不可欠です。
| 再発予防の柱 | 目標・具体的内容 | 重要度 |
|---|---|---|
| 血圧管理 | 収縮期血圧130mmHg未満を目標。降圧薬継続服用+塩分制限(6g/日未満)・有酸素運動・禁煙の組み合わせ | 🔴 最重要 |
| 抗血栓療法 | 抗血小板薬(アスピリン・クロピドグレルなど)を主治医の指示通りに継続。自己判断での中断は再発リスクを著しく高める | 🔴 最重要 |
| 心房細動の管理 | 心房細動が確認されている場合は抗凝固薬(DOAC・ワルファリン)を適切に使用。ホルター心電図での除外検索も重要 | 🔴 最重要 |
| 血糖管理 | HbA1c 7.0%未満を目標。血管内皮保護・穿通枝脆弱化の予防 | 🟡 重要 |
| 脂質管理 | LDLコレステロール100mg/dL未満(高リスク例は70mg/dL未満)。スタチン薬の積極的使用 | 🟡 重要 |
| 禁煙 | 喫煙は血管内皮障害を促進し穿通枝を脆弱化。完全禁煙が原則 | 🟡 重要 |
| 有酸素運動 | 中等度強度の有酸素運動を週150分以上。血圧・血糖・脂質の改善を通じて再発リスクを低減 | 🟢 推奨 |
適度な有酸素運動は血圧・血糖・脂質の改善を通じてラクナ梗塞の再発リスクを下げます。「リハビリで歩けるようになる」ことは機能回復と再発予防という二重の意義があります。ただしリハビリ強度の設定に際しては、主治医と連携した血圧・心拍数の管理が前提となります。
よくある質問(FAQ)― 放線冠・内包梗塞のリハビリについて
放線冠と内包はどちらが重症になりやすいですか?
内包の脳卒中で完全麻痺になりましたが、回復できますか?
「運動失調性片麻痺」と言われました。病変はどこにありますか?
手の不器用さや言葉がうまく出ない症状はリハビリで改善しますか?
「多発性の白質病変(WML)」と言われました。どういう意味ですか?
ラクナ梗塞後のリハビリはいつから、どのように始めますか?
神経可塑性を高めるために患者自身でできることはありますか?
専門家向け:放線冠・内包損傷後の予後予測ツール(PREP2・NIHSS連携)
PREP2アルゴリズム(Stinear CM, 2017):発症3〜7日後の上肢機能回復を予測するバイオマーカーベースのアルゴリズム。① NIHSS上肢運動スコア ② DTIによるFA値患健比(rFA)③ 皮質脊髄路のMEP誘発可否を組み合わせ、90日後の上肢機能を4段階(完全回復〜重度障害持続)で予測。内包後脚・放線冠梗塞後の回復予測精度向上に貢献している。
NIHSSとリハビリ目標設定の連携:入院時NIHSSスコアは90日後mRSと強い相関があります(Adams et al. 1999)。特に内包後脚梗塞では運動項目(5a/5b/6a/6b)の初期スコアが最終的な歩行・ADL自立度と相関。NIHSS運動項目が4点(完全麻痺)の場合、DTIによるrFAが回復可能性の追加情報として有用。
Fazekas scoreとWMLの評価:MRI FLAIR画像による白質病変の半定量的スコアリング。Grade 0〜3で評価。Grade 2以上(合流性WML)では認知機能低下・転倒リスク・歩行速度低下との関連が強くなるため、リハビリプログラムへのMoCA・歩行速度・転倒リスク評価の組み込みが推奨される。
QCI療法はどんな人に向いていますか?自分で自宅でもできますか?
Qミラー療法は完全麻痺でも効果がありますか?
QPREP2とは何ですか?どこで受けられますか?
参考文献・引用文献
- 1) Jang SH, et al. Reorganization of the corticospinal tract to anterior area of corona radiata infarct. Neural Regen Res. 2015;10(9):1428-1431. PubMed
- 2) AVERT Trial Collaboration Group. Efficacy and safety of very early mobilisation within 24 h of stroke onset (AVERT): a randomised controlled trial. Lancet. 2015;386(9988):46-55.
- 3) Fisher CM. Lacunar strokes and infarcts: a review. Neurology. 1982;32(8):871-876.
- 4) Donnan GA, et al. Lacunar infarction. Stroke. 1982;13(2):163-169.
- 5) Ward NS, et al. Neural correlates of motor recovery after stroke: a longitudinal fMRI study. Brain. 2003;126(11):2476-2496.
- 6) Nudo RJ. Mechanisms for recovery of motor function following cortical damage. Curr Opin Neurobiol. 2006;16(6):638-644.
- 7) Pollock A, et al. Interventions for improving upper limb function after stroke. Cochrane Database Syst Rev. 2014;(11).
- 8) Pantoni L. Cerebral small vessel disease: from pathogenesis and clinical characteristics to therapeutic challenges. Lancet Neurol. 2010;9(7):689-701.
- 9) Stinear CM, et al. PREP2: A biomarker-based algorithm for predicting upper limb function after stroke. Ann Clin Transl Neurol. 2017;4(11):811-820.
- 10) Adams HP Jr., et al. Baseline NIH Stroke Scale score strongly predicts outcome after stroke. Neurology. 1999;53(1):126.
- 11) Bamford J, et al. Classification and natural history of clinically identifiable subtypes of cerebral infarction. Lancet. 1991;337(8756):1521-1526.
- 12) Powers WJ, et al. 2018 Guidelines for the Early Management of Patients With Acute Ischemic Stroke. Stroke. 2018;49(3):e46-e110.
- 13) Wolf SL, et al. Effect of constraint-induced movement therapy on upper extremity function 3 to 9 months after stroke (EXCITE Trial). JAMA. 2006;296(17):2095-2104.
- 14) Thieme H, et al. Mirror therapy for improving motor function after stroke. Cochrane Database Syst Rev. 2018;(7):CD008449.
- 15) Rossini PM, et al. Noninvasive electrical and magnetic stimulation of the brain, spinal cord, roots and peripheral nerves. Clin Neurophysiol. 2015;126(6):1071-1107.
リハビリを受けた方の声
内包後脚の梗塞で右半身が完全に動かなくなりました。最初は「これで一生か」と絶望していましたが、STROKE LABで画像を見ながら自分の身体状況についての問題点と改善の道を説明してもらったとき、初めて希望が持てました。地道なリハビリを続けた10週後には右手を自分で少し動かせるようになり、歩きも杖で外出できるまで回復しています。
50代女性・放線冠梗塞(発症後1か月〜)
多発性のラクナ梗塞で歩行がおぼつかなくなり、転倒が怖くなっていました。STROKE LABでのバランス訓練と感覚再教育を続けたことで、今は一人でスーパーへ買い物に行けるようになりました。血圧管理の大切さも改めて意識できるようになり、生活全体が変わりました。
70代男性・多発性ラクナ梗塞(発症後3か月〜)
放線冠・内包の脳卒中後リハビリは
「病変部位を理解した」専門プログラムで回復が変わります。
どこが損傷しているか・どの線維が影響を受けているか——
その把握なしに行うリハビリは、回復のスピードと深度を損ないます。
神経可塑性を最大限に引き出す個別設計のリハビリを、
STROKE LABが東京・大阪で提供しています。
まずは無料相談からお気軽にどうぞ。

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)














