【2026年版】側坐核の役割〜やる気スイッチ!?:画像CT/MRIドーパミン機能まで!
本記事では、脳の報酬・動機づけ・感情制御の中枢として近年のリハビリテーション科学で注目を集める側坐核(Nucleus Accumbens: NAc)について、解剖学的位置・神経回路・血液供給・MRI所見から、依存症・うつ病・統合失調症との関係、さらにリハビリテーションへの応用(強化スケジュール)まで完全解説します。「なぜ患者のモチベーションが続かないのか?」「強化スケジュールはどう選ぶ?」「報酬系をリハビリに活かすには?」という臨床家のリアルな疑問に答えます。
側坐核(Nucleus Accumbens: NAc)は、腹側線条体の中核をなす深部脳構造で、前脳基底部に位置します。ドーパミン・グルタミン酸・GABAを主な神経伝達物質とし、報酬処理・動機づけ・感情制御・意思決定・運動の開始に深く関与します。コア(Core)とシェル(Shell)の2部位からなり、前頭前皮質・扁桃体・海馬・視床下部と密接なネットワークを形成します。依存症・うつ病・統合失調症の病態理解に不可欠な領域であり、リハビリテーション場面では患者のモチベーション維持・強化スケジュールの設計に直結する知識です。
- 正式名称:Nucleus Accumbens(NAc)。腹側線条体(Ventral Striatum)の主要構成部位
- 位置:前脳基底部・前交連の直前上部。腹側線条体(尾状核・被殻)の腹側・内側に位置し、中隔野に隣接(”nucleus accumbens septi”=中隔に寄りかかる核の意)
- 2つの部位:NAcコア(Core)= 運動習慣・条件行動の強化 | NAcシェル(Shell)= 報酬・感情・自然報酬の調節
- 血液供給:前大脳動脈(ACA)のホイブナー反回動脈 + 中大脳動脈(MCA)のレンズ核線条体動脈
- 主な神経伝達物質:ドーパミン(DA)=動機づけ・学習 | グルタミン酸(Glu)=価値評価・記憶 | GABA=抑制・バランス調整
- 主要接続:VTA(中脳辺縁系経路) / 前頭前皮質(意思決定) / 扁桃体(感情) / 海馬(記憶) / 視床下部(動機づけ)
- 関連病態:依存症(過剰活性) / うつ病(活動低下・アンヘドニア) / 統合失調症(感情・動機づけ障害)
- 快楽ホットスポット:NAcコア吻側 = 報酬の「好み」 | NAcシェル尾側 = 報酬反応抑制・嫌悪感
- リハビリへの応用:強化スケジュール(FIS/VIS/FRS/VRS)の使い分けで側坐核の報酬系を意図的に活性化
- 臨床観察ポイント:食欲・活動への興味消失 = NAc活動低下のサイン。感情の爆発 = 扁桃体との調整不全
- 新人セラピストの落とし穴:モチベーションの軽視・家族教育の不足が回復を大きく妨げる。「努力を認識・称賛すること」がNAcを直接活性化する
側坐核とは ― 解剖学的位置・構造
側坐核(Nucleus Accumbens: NAc)は、大脳基底核の一部である腹側線条体に属する核構造で、前脳基底部・前交連の直前上部に位置します。「nucleus accumbens septi(中隔に寄りかかる核)」という名称はドイツの神経解剖学者Theodor Ziehenが1897年に命名したとされており、その後1954年にOldsとMilnerがラット脳への自己電気刺激実験で「報酬の中枢」としての機能を発見、1970〜80年代の中脳辺縁系ドーパミン研究によって神経科学の表舞台に登場しました。
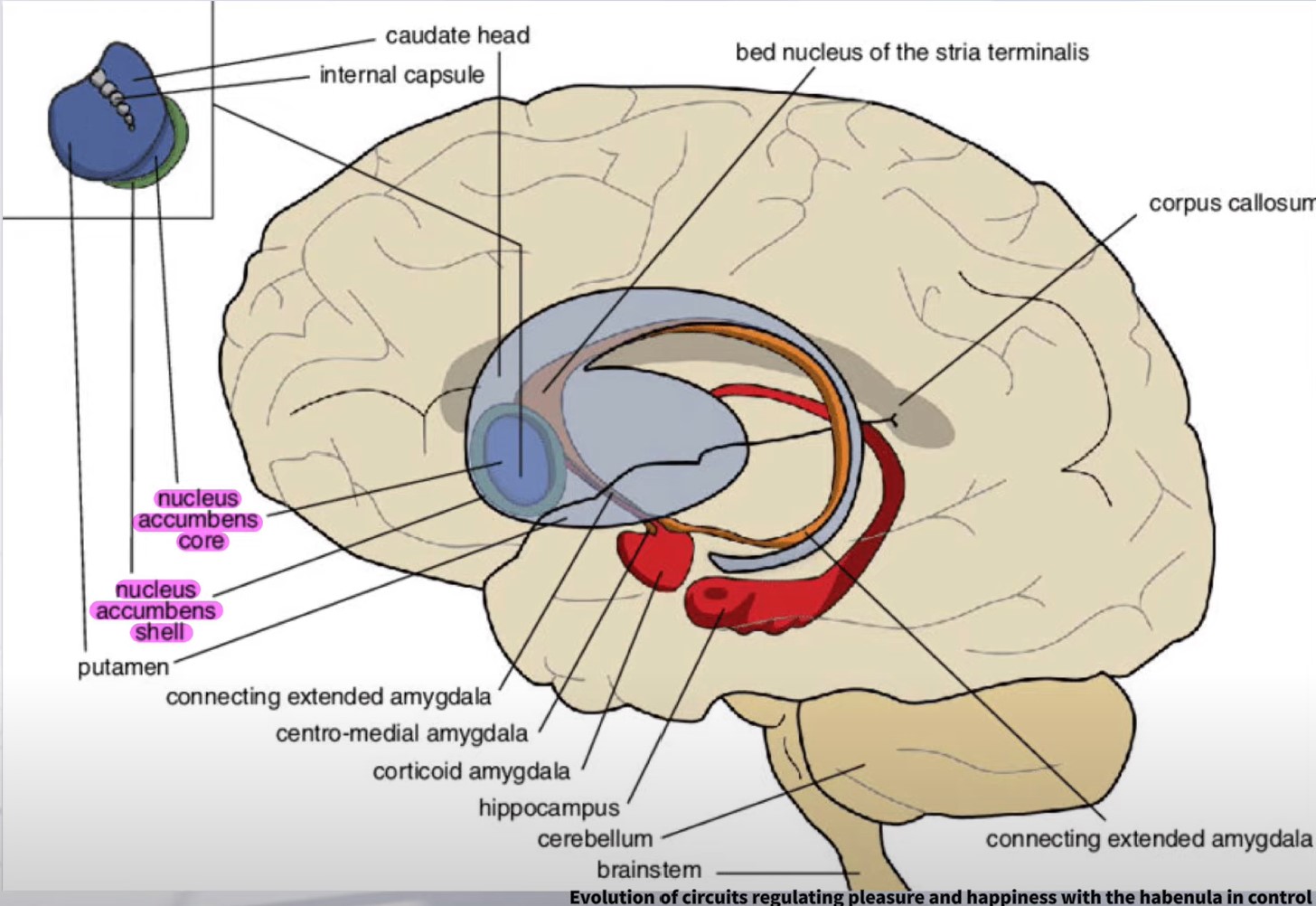
側坐核の解剖学的位置(腹側線条体・前交連との関係)
側坐核の2つの主要部位:コアとシェル
NAcコア(Core)
背側線条体(尾状核・被殻)に似た構造と機能を持ちます。運動機能、条件刺激に対する行動の開始、運動習慣の形成に寄与。薬物依存や繰り返し行動の強化にも深く関与し、「習慣的行動の回路」の中核をなします。
臨床的意義:脳卒中後の運動学習・歩行の習慣化に直接関わる部位。繰り返し練習による自動化(オートマチゼーション)の基盤となります。
NAcシェル(Shell)
大脳辺縁系との関連が強く、報酬関連行動・感情的な価値判断・自然報酬(食事・快楽など)の調節を担います。無条件刺激への反応を媒介し、「好きかどうか(liking)」の判断に関与します。
臨床的意義:「またやってみたい」という内発的動機づけの源泉。患者の治療意欲・リハビリへの主体的参加に関わる部位です。
📍 コアとシェルの機能的違い ― リハビリ視点での整理
| 比較項目 | NAcコア | NAcシェル |
|---|---|---|
| 主な機能 | 条件行動の強化・運動習慣の形成 | 報酬の感情的評価・自然報酬の調節 |
| 類似構造 | 背側線条体(尾状核・被殻) | 大脳辺縁系(扁桃体・視床下部) |
| 関連する学習 | 道具的条件づけ・習慣学習 | パブロフ型条件づけ・感情的記憶 |
| 依存症との関係 | 強迫的薬物探索行動の強化 | 薬物の主観的快楽感(陶酔感)の媒介 |
| リハビリ応用ポイント | 反復練習による動作の自動化 | 内発的動機の活性化・達成感の強化 |
🎯 快楽ホットスポットとコールドスポット(Berridge et al. の知見)
快楽ホットスポット(NAcシェル内側前方部:rostromedial shell):報酬の「好み(liking)」に関与する小領域です。Berridgeらの研究では、この部位へのμオピオイド受容体刺激やエンドカンナビノイド系の活性化が快楽反応(甘味への反応行動の増強など)を引き起こすことが示されています。ラットでは非常に小さな領域(約1/10 mm³程度)ですが、ヒトでは相同する領域がより広いと推定されます。
コールドスポット(NAcシェル尾側・内包周辺部):報酬反応の抑制・嫌悪感に関連する領域です。同じオピオイド刺激でも、ホットスポットから離れたこの部位では嫌悪反応が誘発されることがBerridgeらの実験で確認されています。快楽と嫌悪の空間的分布が同一構造内に共存するという点が側坐核の特徴的な複雑性です。
※ ホットスポット・コールドスポットの研究は主にラット・マウスでのものであり、ヒトへの直接適用には注意が必要です(Berridge KC & Kringelbach ML, 2015)。
血液供給と虚血リスク
側坐核の血液供給は、2つの主要な動脈系によって支えられています。この供給システムを理解することは、局所的な虚血や出血が側坐核の機能に与える影響を予測し、適切なリハビリ介入を設計するうえで重要です。
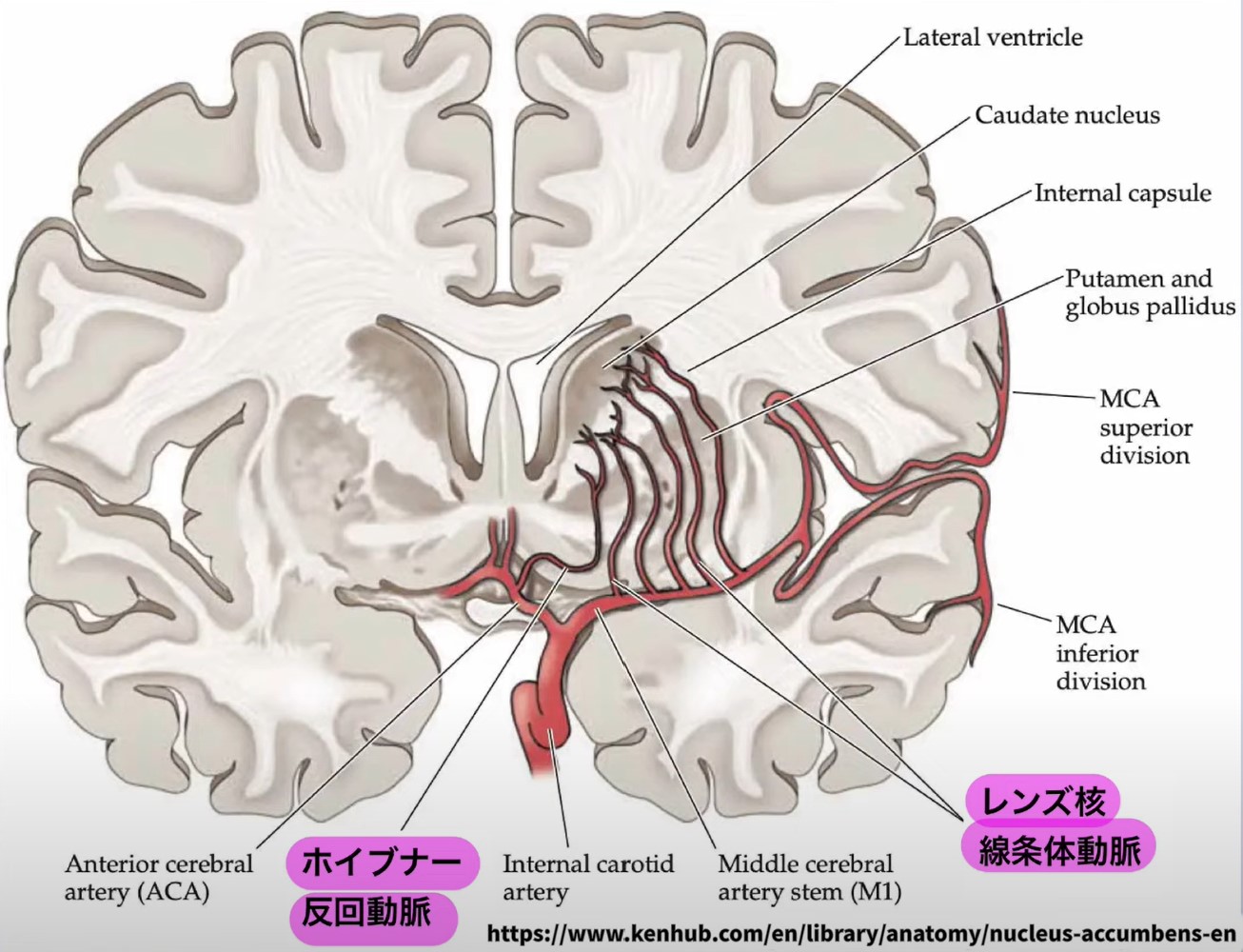
側坐核への血液供給:ホイブナー反回動脈とレンズ核線条体動脈
ホイブナー反回動脈(Recurrent Artery of Heubner)
前大脳動脈(ACA)のA1〜A2接合部から分岐する細い動脈で、側坐核・尾状核頭部の内側部・前交連周囲の血液を供給します。この動脈の閉塞では、アパシー(意欲低下)・記憶障害・行動の開始困難が生じることがあり、NAcの虚血を示唆するサインとして重要です。
レンズ核線条体動脈(Lenticulostriate Arteries)
中大脳動脈(MCA)M1部から分岐する穿通枝群で、側坐核の外側部・被殻・内包を広く栄養します。高血圧性の小血管病変や塞栓症でこれらが閉塞すると、被殻出血・ラクナ梗塞に伴う運動麻痺に加え、感情調節障害・意欲低下が混在する臨床像を呈することがあります。
⚠️ 前脳基底部梗塞と側坐核損傷 ― 見落としやすい臨床像
ホイブナー動脈閉塞:前交通動脈瘤破裂後のクモ膜下出血やACA梗塞に合併することがあります。「運動麻痺は軽微なのに、覚醒後から突然無気力になった」「家族の名前は言えるのにリハビリへの参加意欲が著しく低い」といった症状は、側坐核を含む前脳基底部損傷を強く示唆します。
リハビリ上の注意:このような患者では運動能力だけを評価・訓練しても効果が上がりにくく、神経行動学的評価(アパシー尺度・動機づけ評価)と組み合わせた介入設計が不可欠です。
神経ネットワークと神経伝達物質
中脳辺縁系ドーパミン経路:側坐核の最重要入力
中脳辺縁系ドーパミン経路(Mesolimbic Dopamine Pathway):報酬予測・動機づけ・快楽の中核回路
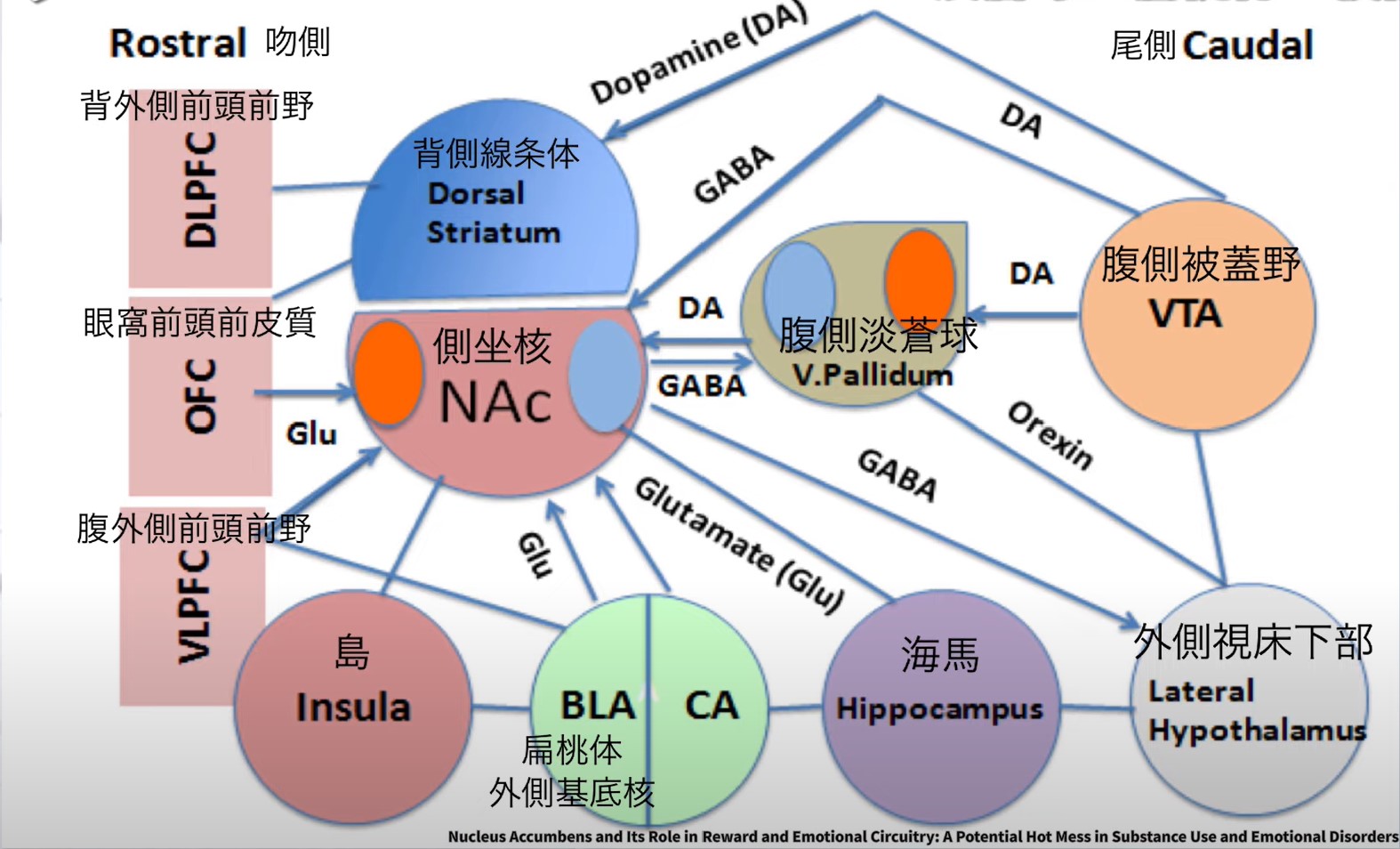
側坐核と関連脳領域の神経ネットワーク
側坐核と相互接続する主要脳領域
前頭前皮質(PFC)
意思決定・目標志向型行動の制御。トップダウン的に側坐核の活動を調節し、衝動的な報酬追求を抑制します。PFCの損傷(前頭葉病変)はNAcへの制御入力を失わせ、衝動性が増大します。
扁桃体(Amygdala)
感情的評価・恐怖記憶との連携。条件づけされた刺激(薬物関連の場所・音など)が扁桃体を介してNAcを活性化し、強迫的な報酬探索行動を駆動します。
海馬(Hippocampus)
空間記憶・文脈学習との統合。「どこで・どのような状況で報酬を得たか」の文脈情報をNAcに提供。場所に関連する依存行動の形成に寄与します。
視床下部(Hypothalamus)
基本的動機づけ(食欲・性欲・体温調節)の制御。側坐核が視床下部からの内的動機情報を受け取り、「生存に必要な報酬」への動機を形成します。
島皮質(Insula)
体内感覚・情動の統合。身体感覚(痛み・不快感・渇き)をNAcに伝達し、回避行動・嫌悪学習に関与します。慢性疼痛患者の意欲低下との関連が注目されています。
背側線条体(Striatum)
運動習慣形成との連携。目標志向的行動(NAcが関与)から習慣的行動(背側線条体が関与)への移行を支えます。リハビリでの「自動化プロセス」に直結します。
3大神経伝達物質の役割と臨床的含意
ドーパミン(Dopamine)
役割:動機づけの強化・報酬予測誤差のシグナル。「期待した報酬より良い結果」でNAcへのDA放出が増加し、その行動が強化されます。
臨床的含意:ドーパミン不足(パーキンソン病・うつ病)では意欲が低下。リハビリ課題の難易度設定と「成功体験の積み重ね」がDA系を活性化します。
グルタミン酸(Glutamate)
役割:前頭前皮質・扁桃体・海馬からの主要な興奮性入力。価値評価・文脈記憶との連携を担い、「この行動はどれほど価値があるか」を評価します。
臨床的含意:グルタミン酸系の過活性が依存症・統合失調症に関与。薬物治療(NMDA受容体拮抗薬など)との相互作用を把握することが重要です。
GABA(γ-アミノ酪酸)
役割:NAc内の主要な抑制性介在ニューロンが放出。興奮性入力のバランスを取り、行動の「ブレーキ」として機能します。
臨床的含意:GABA系の機能不全(アルコール依存症など)では衝動性が亢進。過度な刺激・プレッシャーは逆にNAcの機能を抑制させる可能性があります。
🔑 Wanting(欲しい)と Liking(好き)の分離 ― Berridgeの「動機的顕現性理論」
なぜ「やる気はあるのに楽しくない」が起きるのか ― リハビリへの応用
Berridge & Robinson(1998)が提唱した「動機的顕現性理論(Incentive Salience Theory)」は、報酬に関わる脳の仕組みを「Wanting(欲しい・求める動機)」と「Liking(好き・快楽を感じる)」の2つの独立したシステムに分解します。
Wanting系(側坐核のDA系が主役):「あれを手に入れたい・あれをしたい」という動機的衝動を生み出すシステム。ドーパミン神経系によって制御され、報酬への注意・接近行動・努力を駆動します。
Liking系(NAcシェルのオピオイド・カンナビノイド系が主役):実際に報酬を得たときの「気持ちいい・楽しい」という快楽経験そのもの。オピオイド・エンドカンナビノイド系が担い、ドーパミン系とは部分的に独立して機能します。
| 比較項目 | Wanting(欲しい) | Liking(好き) |
|---|---|---|
| 主な神経基盤 | 側坐核 DA系(VTA→NAc) | NAcシェルの μオピオイド・カンナビノイド系 |
| 機能 | 動機・接近行動・努力の生成 | 快楽経験・満足感・良い気分 |
| 依存症での変化 | 増強(薬物への強迫的衝動) | 低下(慣れ・快楽の鈍化) |
| うつ病での変化 | 低下(無気力・無動) | 低下(アンヘドニア) |
| リハビリへの示唆 | 強化スケジュールで「やりたい気持ち」を引き出す | 達成感・成功体験で「楽しかった記憶」を形成する |
💡 wanting/liking理論をリハビリで使う3つの実践法
①「やってみたい(wanting)」の種をまく:患者が次のセッションを「待ち望む」状態を作ることがwanting系の活性化です。例:「次回は初めてのバランスボードを使います」「来週は院内を実際に歩いてみましょう」と次回への期待を植え付ける一言。
②「楽しかった(liking)」の記憶を確実に作る:セッション終了時に「今日一番うまくできた動作」を患者自身に言語化させます。オピオイド系を活性化するのは「達成感の主観的体験」であり、セラピストの評価だけでは不十分です。「今日、何が一番できたと思いますか?」という問いかけが鍵です。
③ wanting と liking の乖離に気づく:「リハビリには来るが全然楽しそうではない(wanting ≒ 正常 / liking ↓)」という患者は、快楽系の機能低下(うつ・慢性疼痛・薬剤副作用)を疑います。逆に「楽しいと言うがなかなか来院しない(liking ≒ 正常 / wanting ↓)」は動機づけ障害・アパシーのサインです。
🏃 運動・身体活動が側坐核に与える直接効果
運動はNAcのドーパミン放出を増加させ、報酬感受性を改善する
Greenwood et al.(2011, J Neurosci)の動物研究では、規則的な有酸素運動がNAcのドーパミン受容体感受性を改善し、ストレス誘発性の無気力(learned helplessness)に対して保護的に機能することが示されました。ヒトを対象とした研究でも、有酸素運動後にNAcを含む報酬回路の活性化(fMRI)が増加し、気分と動機づけが改善することが複数報告されています(Pontifex et al. 2019など)。
リハビリへの含意:「運動療法そのものが側坐核に直接作用する」という視点は、リハビリの効果機序を「筋力・機能回復」だけでなく「脳の報酬系の賦活」として位置づけることを可能にします。特にうつ症状を合併した脳卒中・神経疾患患者では、中等度有酸素運動(50〜70% HRmax、20〜40分)を継続的に取り入れることで、NAcを介した気分改善・意欲向上効果が期待できます。
📊 運動とNAc機能改善 ― 臨床的に押さえる4点
① 有酸素運動(中等度)が最もDA放出増加に効果的:強度が高すぎる(>85% HRmax)と逆にコルチゾール過剰分泌でNAc機能が抑制される可能性があります。脳卒中後リハビリでは「少し息が上がる程度」が目安です。
② 運動後の「達成感の言語化」がliking系を追加活性化:運動直後に「今日の自分のベストは?」と問いかけることで、運動によるDA放出に加えてオピオイド系のliking反応が上乗せされ、報酬学習が強化されます。
③ 社会的運動(グループリハビリ)がオキシトシン系も同時活性化:仲間と行う運動は、個人の有酸素運動効果に加えて社会的報酬(承認・仲間意識)によるNAcのオキシトシン系活性化が加わり、総合的な動機づけ改善効果が期待できます。
④ 睡眠不足はNAcのDA受容体感受性を著明に低下させる:1〜2日の睡眠制限でもNAcの報酬刺激への反応が低下する(Yoo et al. 2012)ことが報告されています。「眠れていますか?」の問診がリハビリ効果を左右する可能性があります。
MRIでの同定方法 ― 解剖学的ランドマーク
🔑 MRIで側坐核を同定する3ステップ
Step 1 前脳基底部を確認:まず冠状断(Coronal)断面で前脳基底部(前交連レベル)を探します。この領域の「底部」に側坐核が位置します。
Step 2 尾状核・被殻をランドマークに:尾状核と被殻はMRIで識別しやすい大きな構造です。その腹側(底部)にある小さな楕円形の領域が側坐核です。背側線条体(尾状核+被殻)の「下」を探すイメージで同定します。
Step 3 前交連(Anterior Commissure)で確認:前交連は正中線を横切る線維束でMRIの重要な目印です。側坐核は前交連の直前上方に位置します。前交連を確認したら、その「直上+前方」を探します。
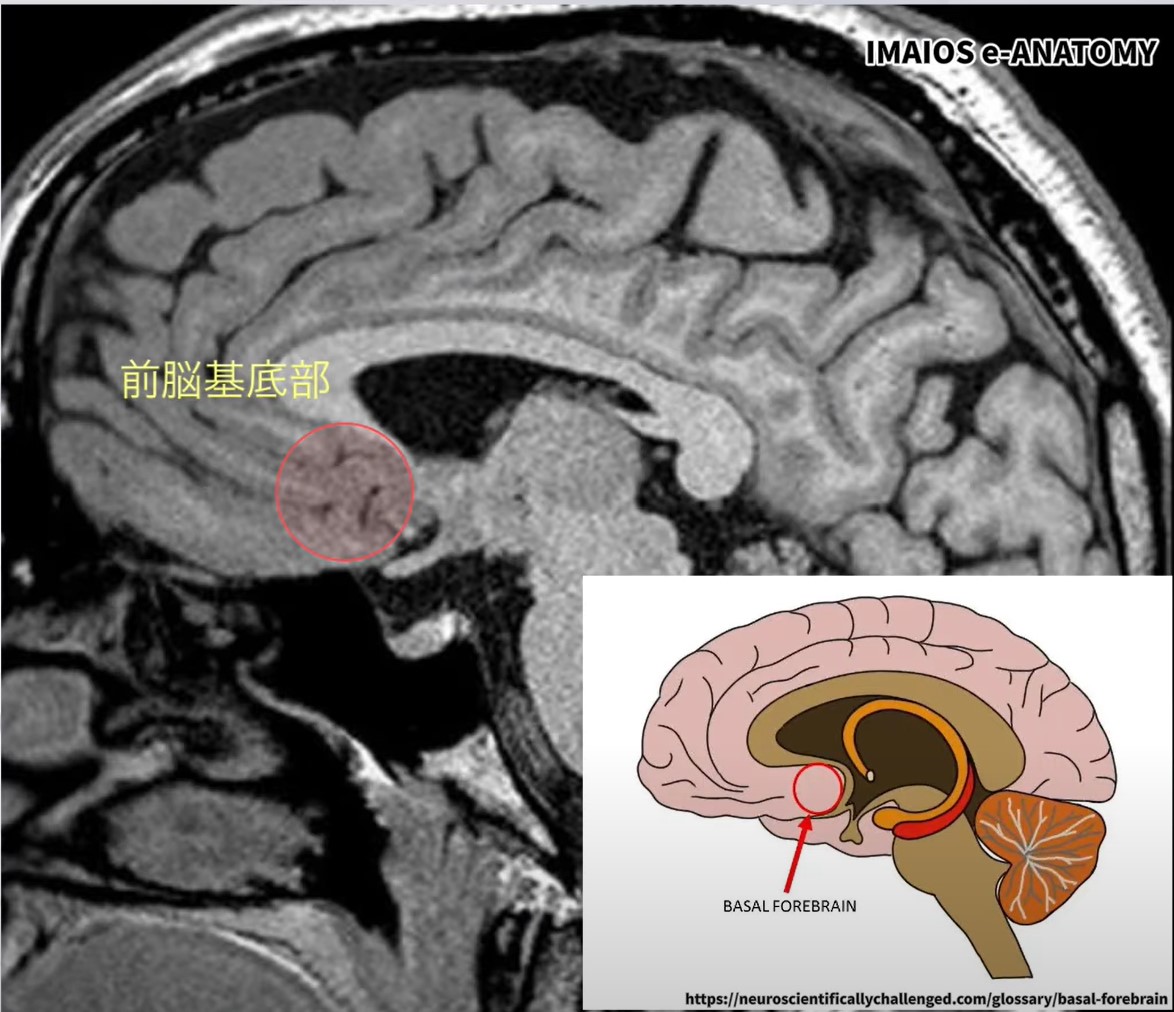
前脳基底部:側坐核の出発点
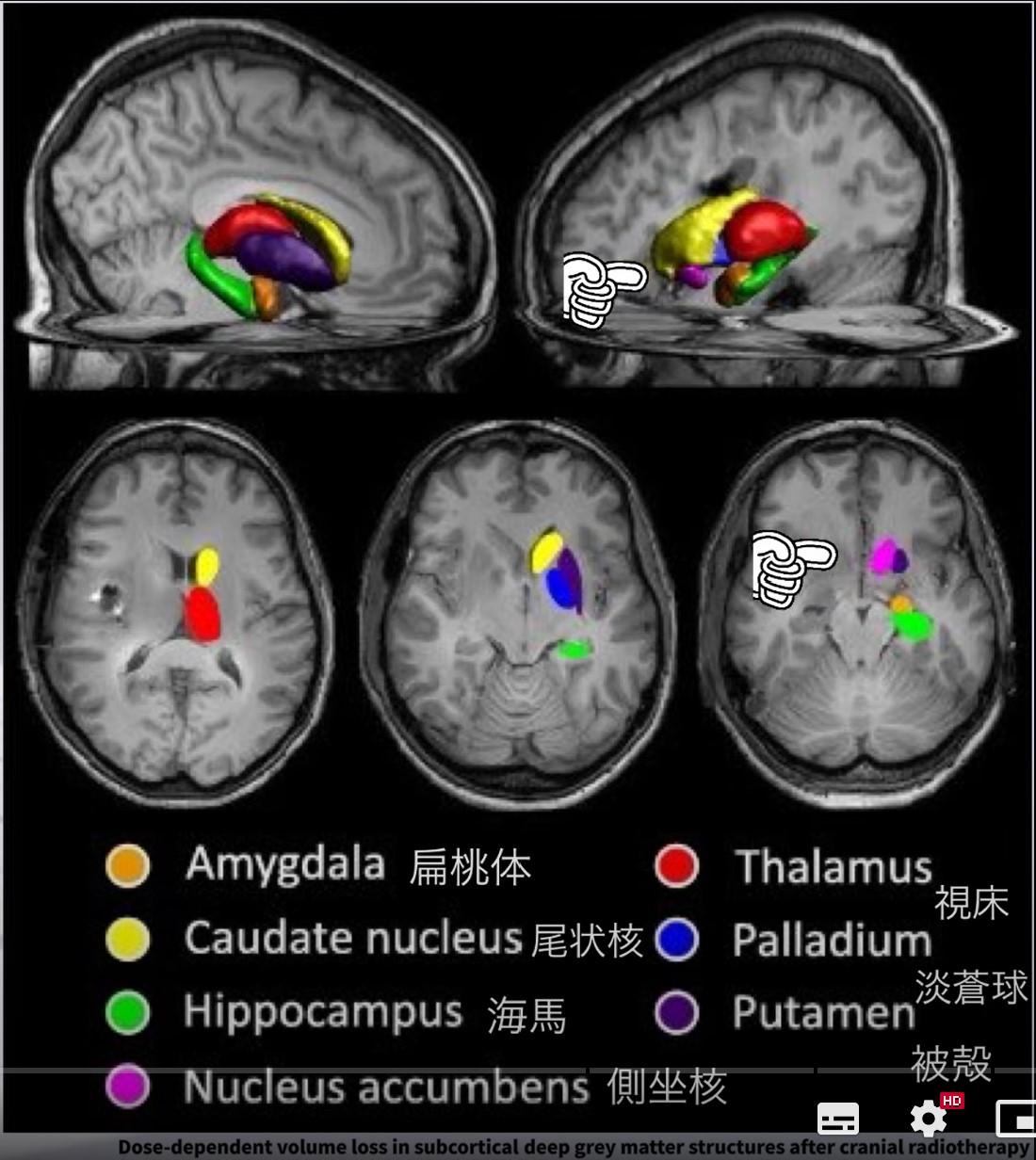
尾状核・被殻をランドマークに同定
前交連(AC):最重要ランドマーク
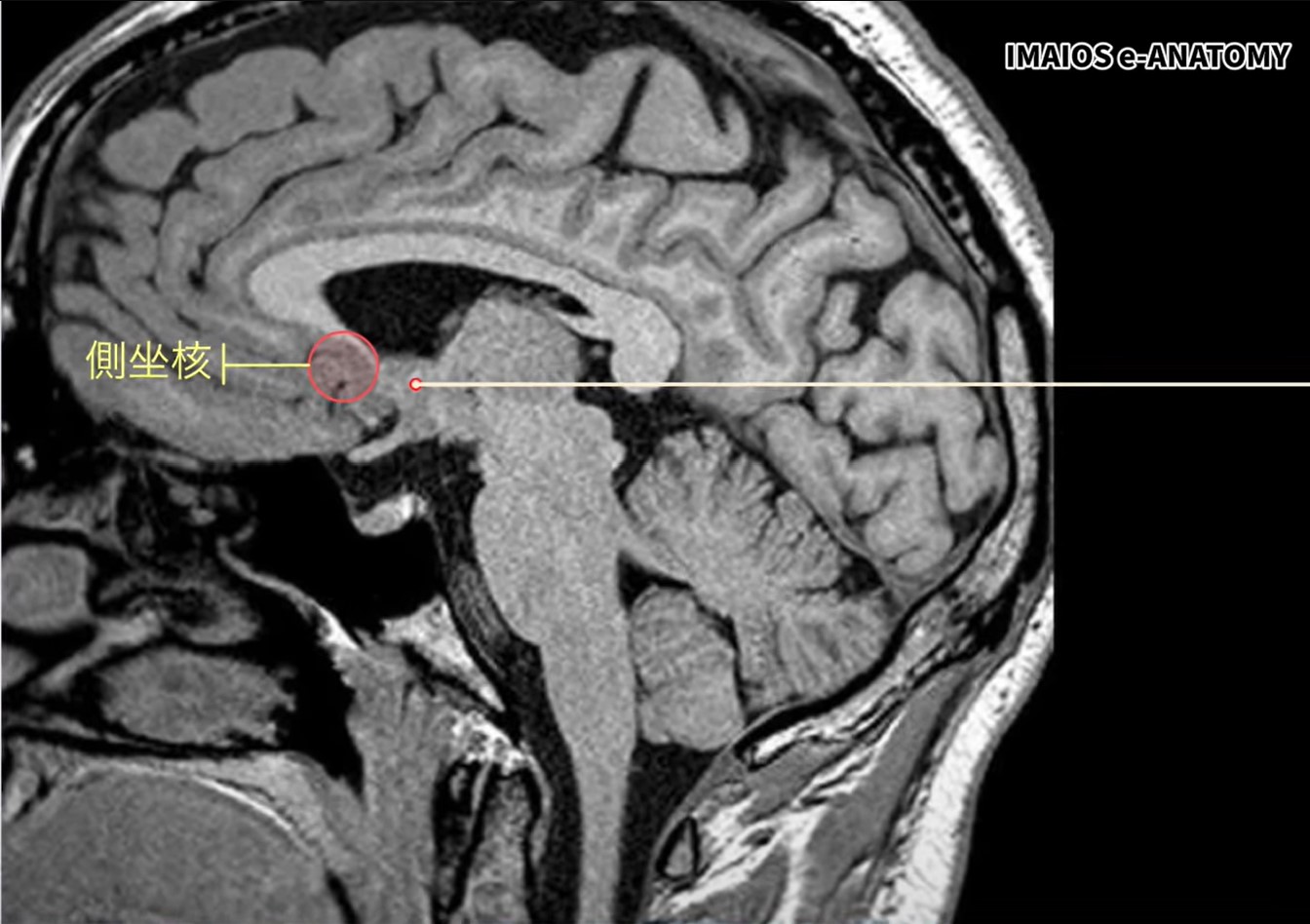
MRI上の側坐核:小さな楕円形領域
💡 MRI上での側坐核の特徴まとめ
形状:小さな楕円形(約1〜1.5cm)の構造として観察されます。大きさが小さいため、高分解能MRIが推奨されます。
信号強度:T1強調像では周囲の線条体と同程度のやや低信号。T2強調像では等〜低信号。DTI(拡散テンソル画像)では線維連絡の可視化が可能です。
同定の注意点:側坐核は個人差が大きく、標準的なアトラス(MNI空間)ではおよそ両側 x=±9〜10 mm、y=8〜12 mm、z=−6〜−8 mm 周辺に中心座標が設定されることが多いです(アトラスによって異なります)。臨床では尾状核頭部と被殻の接合部下方・前交連の直前上部を探すアプローチが実践的です。
臨床症状と精神疾患との関係
アパシー評価ツールの比較 ― NAc機能低下を数値化する
| 評価ツール | 正式名称・特徴 | スコア範囲 | カットオフ | 特長・推奨場面 |
|---|---|---|---|---|
| Starkstein Apathy Scale(SAS) | 構造化面接形式。認知・行動・感情の3ドメイン14項目 | 0〜42点(高いほど重度) | ≥14点でアパシーあり | 脳卒中・PD・認知症全般に使用可。信頼性・妥当性の実績が豊富。最も多用される |
| Apathy Evaluation Scale(AES) | 18項目。自己評価・他者評価・面接の3形式あり | 18〜72点(高いほど重度) | ≥38点がカットオフの目安 | 多様な評価形式で使い分けが可能。患者自己評価版(AES-S)は外来でも使いやすい |
| Lille Apathy Rating Scale(LARS) | 半構造化面接9ドメイン33項目。アパシーのサブタイプを分類可能 | −36〜+36点(高いほど重度) | ≥−16点でアパシーあり | PAD(うつとアパシーの分離)に優れる。PD・前頭葉病変で特に有用 |
| Neuropsychiatric Inventory(NPI)アパシーサブスケール | 12症状のうちアパシー項目を抜粋。介護者評価形式 | 0〜12点(頻度×重症度) | ≥4点でアパシーあり | 認知症患者に最適。介護者の負担感を含む評価が可能。外来・訪問リハでも使いやすい |
| Goal Engagement Scale | 目標への関与度を評価する簡易スケール | 0〜40点 | 施設・研究により異なる | リハビリ目標への取り組み意欲を直接評価。目標設定面談の補助ツールとして有用 |
⚠️ アパシー評価の注意点:うつ病との鑑別が最重要
アパシースケールとうつ尺度(GDS・BDI・HAMD)は並行して実施してください。アパシーとうつ病は共存することが多い(約30〜40%)ですが、治療方針が異なります。アパシー優位→ドパミン作動薬・行動活性化療法が有効。うつ病優位→SSRIなど抗うつ薬・認知行動療法が有効。両方を精査せずに「やる気がない患者」と一括りにすることが最もよくある落とし穴です。
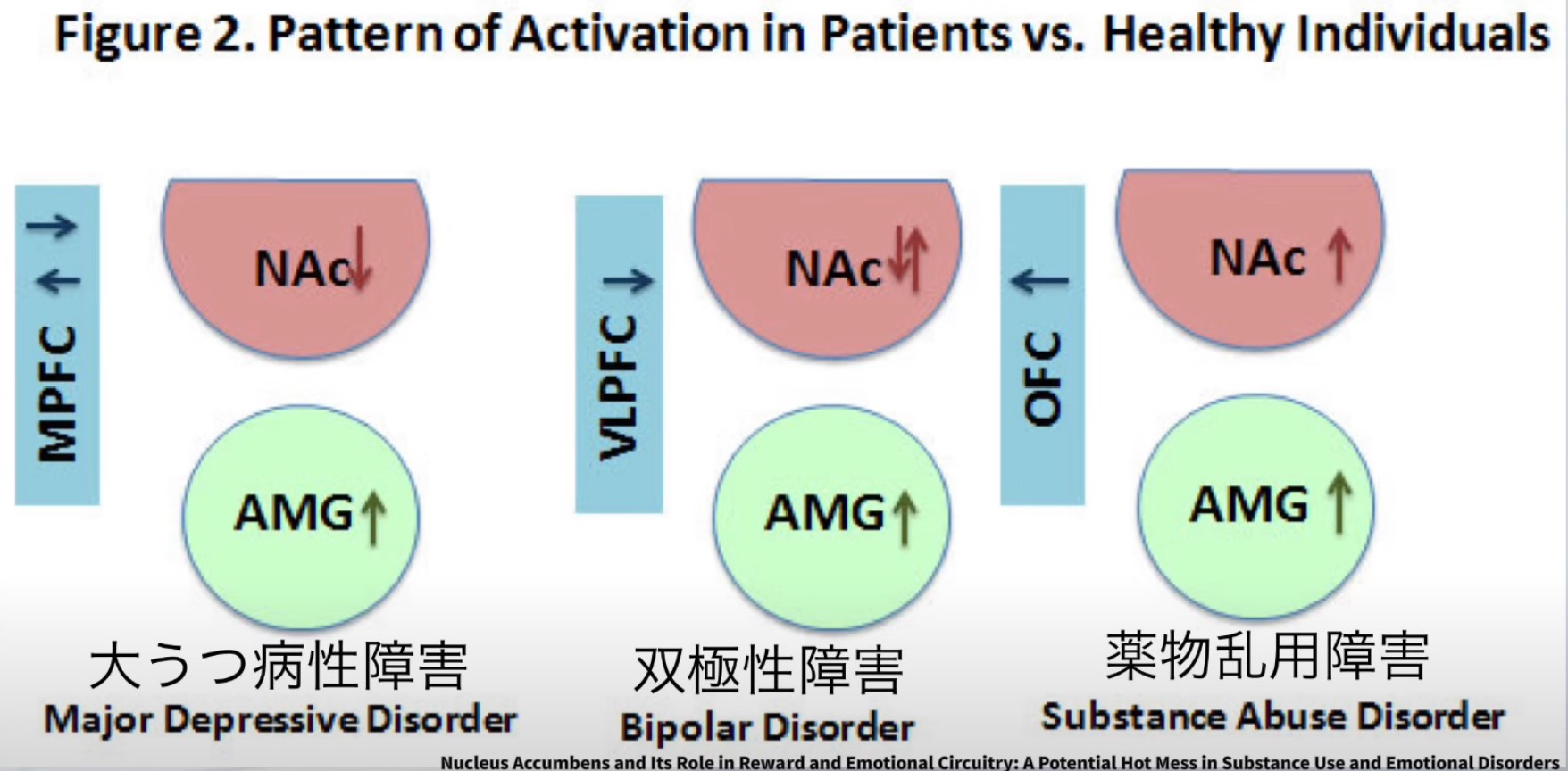
精神疾患ごとの側坐核活性化パターンの違い
| 疾患・病態 | 側坐核の変化 | 主な症状 | リハビリへの影響 |
|---|---|---|---|
| 主要な関連疾患 | |||
| 依存症(薬物・行動依存) | 報酬刺激に対する活性化が過剰増加。ドーパミン感受性の変化(脱感作) | 強迫的な薬物・行動追求、意欲の選択的亢進 | リハビリへの動機が「依存対象」と競合。構造化されたリハビリ環境の確立が必須 |
| 大うつ病性障害(MDD) | 報酬・感情刺激への反応が著明に低下(アンヘドニア) | 快楽消失、活動への興味喪失、疲労感 | リハビリ参加の拒否・無関心が頻発。強化スケジュールの工夫と薬物療法との連携が重要 |
| 双極性障害(BD) | 躁期:感情的刺激に過剰反応 / うつ期:低反応 | 躁期の衝動的行動 / うつ期のアパシー | 気分状態により参加度・安全性が大きく変動。気分モニタリングを評価に組み込む |
| 統合失調症 | DA系の機能不全(過活性または過少活性の混在) | 陰性症状(無為・感情鈍麻)、動機づけ障害 | 陰性症状が強い場合、報酬への反応が鈍く習慣学習が困難。抗精神病薬の効果確認と連携 |
| 脳卒中・神経疾患での側坐核関連症状 | |||
| 前脳基底部梗塞(ACA梗塞) | ホイブナー動脈閉塞による直接損傷 | アパシー、記憶障害、行動開始困難 | 「やる気がない」は意思の問題ではなく神経学的損傷。チームで理解を共有する |
| パーキンソン病 | 黒質-線条体路のDA減少に伴う腹側線条体への影響 | 動作開始困難、意欲低下、うつ症状 | Dopa投与タイミングと運動練習のタイミングを合わせることで学習効果が向上 |
| 慢性疼痛 | NAcのドーパミン機能低下・mPFCとの連絡変化 | 痛みへの過敏・感情的苦痛・活動回避 | 疼痛そのものだけでなく「報酬系の賦活」を目標とした活動参加が重要 |
専門家向け:側坐核のニューロサイエンス ― DBS・薬物療法との関係
深部脳刺激(DBS)への応用:難治性うつ病・強迫性障害(OCD)に対する治療標的として側坐核が注目されています。NAcシェルへのDBS(高頻度電気刺激)が難治性うつ病の症状を改善させたという複数の報告(Schlaepfer et al. 2008ほか)があり、報酬系の直接的賦活によるアンヘドニア改善が機序として想定されています。
薬物療法との相互作用:抗精神病薬(D2遮断薬)は側坐核のDA受容体を遮断することで陽性症状を改善しますが、同時にNAcのドーパミン機能を低下させ、陰性症状(無為・感情鈍麻)を悪化させる可能性があります。リハビリ担当者は薬物種別・用量・投与タイミングが患者の学習意欲・運動パフォーマンスに与える影響を主治医と共有することが推奨されます。
NAcと報酬予測誤差(Reward Prediction Error: RPE):Schultz(1998)らによる古典的研究により、VTA-NAc経路のDA放出が「予測した報酬との差分(RPE)」に比例することが示されました。「予想より良い結果(正のRPE)」でDA大量放出 → 行動強化 /「予想より悪い結果(負のRPE)」でDA放出抑制 → 行動抑制。この原理はリハビリでの「適切な難易度設定(70〜80%の成功率)」が最大の学習効果をもたらすという理論的根拠を提供します。
強化スケジュールのリハビリ応用 ― 側坐核を意図的に活性化する
強化スケジュール(Reinforcement Schedule)は、いつ・どのように行動を強化するかを決定する枠組みで、側坐核(NAc)のドーパミン放出パターンに直接影響します。Hannah et al.(2022, StatPearls)の分類に基づき、4タイプのスケジュールとリハビリでの実践例を解説します。
🧠 なぜ強化スケジュールが側坐核に効くのか
Schultzらの報酬予測誤差研究により、「予測不可能な報酬(可変スケジュール)」は「確実な報酬(固定スケジュール)」よりもDA放出量が多いことが示されました。スロットマシンが止められないのと同じ原理で、VRS(可変比率スケジュール)が最も強力な動機づけ効果を持ちます。リハビリ初期は予測可能な固定スケジュールで安心感を与え、習熟に従って可変スケジュールへ移行することで、側坐核の活性化を段階的に高めることができます。
固定間隔スケジュール(Fixed Interval Schedule: FIS)― 予測可能な時間報酬

✅ 利点
- 予測可能性が患者に安心感を与える
- 長時間セッションでのモチベーション維持
- 「あと◯分で褒めてもらえる」が行動を持続させる
⚠️ 欠点
- 報酬直後に努力が一時的に低下(スキャロップ効果)
- スケジュールに慣れると効果が薄れる
- 時間ではなく努力量への動機が生まれにくい
可変間隔スケジュール(Variable Interval Schedule: VIS)― 予測不能な時間報酬

✅ 利点
- 継続的な努力を促す(報酬を待ち続ける)
- 長期にわたってモチベーションが維持される
- 消去(報酬がなくなった場合の行動消失)が遅い
⚠️ 欠点
- 不確実性がフラストレーションを生む場合がある
- 不安が強い患者には逆効果になりうる
- 実施に評価者の判断力が必要で標準化が難しい
固定比率スケジュール(Fixed Ratio Schedule: FRS)― 回数連動の確実報酬

✅ 利点
- 努力量と報酬が直結。高いモチベーションを引き出す
- 達成感が明確で患者自身が進歩を実感しやすい
- 「あと◯回」のカウントダウンが自己効力感を高める
⚠️ 欠点
- 過度な努力による疲労・運動量過多のリスク
- 報酬達成直後の一時的モチベーション低下
- 比率設定が高すぎると挫折感につながる
可変比率スケジュール(Variable Ratio Schedule: VRS)― 最強の動機づけ形式
✅ 利点
- 4スケジュール中最も高いモチベーションを生成
- 消去が最も遅く、長期行動維持に最適
- スケジュールへの慣れが起きにくい
⚠️ 欠点
- 実施の複雑さ・セラピストの判断力が必要
- 不確実性が高いほどストレスになりうる
- 不安障害・依存傾向のある患者には慎重に使用
強化スケジュールの臨床的選択指針
| 比較項目 | VRS(可変比率) | FRS(固定比率) | VIS(可変間隔) | FIS(固定間隔) |
|---|---|---|---|---|
| NAc活性化強度 | 最強 ★★★★ | 強 ★★★ | 中〜強 ★★★ | 中 ★★ |
| 行動の持続性 | 最長(消去抵抗最大) | 長い | 長い | 短め(スキャロップ効果) |
| 実施の容易さ | 複雑(判断が必要) | やや簡単 | やや複雑 | 最も簡単 |
| 最適な時期 | 習熟期・維持期 | 中期(量的目標達成) | 長期維持期 | 初期・導入期 |
| 注意が必要な患者 | 不安障害・依存傾向 | 疲労しやすい患者 | 不安が強い患者 | 努力量に応じた動機が必要な場合 |
| 自主練習との相性 | ✅ 最適(内発的動機づけ) | ✅ 良好(目標管理) | ✅ 良好(長期継続) | △ 短期的(依存リスクあり) |
観察ポイントと臨床ヒント ― セラピストが見るべき行動サイン

側坐核機能低下を示す4つの観察ポイント
報酬系への反応の変化
患者が食事・好きな活動・達成体験への興味を失っている場合、NAcのDA受容体活性低下が疑われます。「最近食欲はありますか?好きなことをしていて楽しいと感じますか?」という簡単な問診がスクリーニングになります。アンヘドニア(快楽消失)が顕著な場合は精神科・心療内科との連携を検討します。
運動開始困難・無動
「やりたい気持ちはあるが、身体が動き始めない」という状態は、NAcコアと前頭前皮質・淡蒼球の接続不全を示唆します。パーキンソン病・前脳基底部梗塞後に頻出。動作のきっかけ(リズム音・言語的合図・視覚的目標)を提供することで、補助的に行動を開始させる介入が有効です。
異常な感情反応(衝動性・感情爆発)
急な怒り・衝動的な行動・感情の制御困難が見られる場合、前頭前皮質からNAcへの抑制入力の減弱(前頭葉損傷・双極性障害の躁期)または扁桃体との調整不全が考えられます。セラピストは「感情的な行動を叱責する」のではなく、構造化された環境・予測可能なルーティンを提供することで側坐核の安定を支援します。
意思決定・選択の困難
「何を食べるか決められない」「リハビリの目標を一緒に決めようとしても答えられない」という状態は、NAcと前頭前皮質・扁桃体ループの機能不全を示唆します。選択肢を絞る(2択)・カード形式で視覚化する・家族の意見を先に聞いてから確認するなど、認知負荷を下げる環境調整が有効です。
3つの実践的臨床ヒント

① 家族教育とサポート体制
家族・友人への側坐核の機能と「報酬系の活性化の重要性」の教育を行います。「がんばったね」という一言が、患者のNAcにDA放出を引き起こします。リハビリへの協力方法・患者の達成を評価する声かけの具体例を伝える場を設けましょう。

② 小さな進歩を積極的に祝う
「先週より2cm高く腕が上がった」「5秒だけ長く立てた」という微小な変化を可視化・称賛します。記録表・写真アルバム・グラフで進捗を「見える化」することで前向きな振り返りができる環境を整えます。VRSの原理で「次はいつ称賛されるか」の期待を利用します。

③ ピアサポートの積極活用
同じ疾患・経験を持つ仲間との交流はNAcのオキシトシン・ドーパミン系を活性化します。グループリハビリ・自助グループ・患者会への橋渡しを行い、社会的報酬(仲間からの承認・共感)を活用した動機づけ強化を図ります。
⚠️ 新人セラピストが陥りやすい2大ミス
① 家族教育の不足:患者のリハビリ環境の大部分は病院外(自宅・地域)にあります。家族が「叱責する」「過度に手伝いすぎる」ことは、NAcの報酬系を抑制し学習を妨げます。退院前に必ず家族への教育セッションを設け、「努力の認識と称賛」「適度な自立促進」の方法を伝えましょう。
② モチベーションの神経科学的背景の軽視:「やる気がない患者」を「性格の問題」として片付けることは、NAcの神経生物学的障害を見落とすリスクがあります。アパシー・無気力は神経学的サインです。評価に「Apathy Evaluation Scale(AES)」や「Starkstein Apathy Scale」を取り入れ、客観的に定量化することを習慣化してください。

リハビリ展開ケーススタディ ― 側坐核を意識した実践
📋 症例:石川さん(62歳・男性)前脳基底部梗塞(ホイブナー動脈閉塞)発症後3週間
右利き。前交通動脈瘤クリッピング術後に前脳基底部梗塞を発症。運動麻痺は軽微(上肢MMT4レベル)ながら、意思決定困難・強い無気力(アパシー)・感情の易変性・食事への興味低下が顕著。「簡単な選択が難しい」「急にイライラする」「リハビリに来ても何もしたくない」が主訴。NIHSSスコアは4点(意識1点・感覚1点・言語1点・構音1点)と低値だが機能的な困難は大きい後方循環を含む典型例。
| 評価項目 | 所見・スコア | NAcとの関連 |
|---|---|---|
| Starkstein Apathy Scale | 28点(重度アパシー) | NAcの活動低下・DA系減弱 |
| 意思決定(2択テスト) | 選択に平均45秒かかる(健常:3〜5秒) | PFC-NAcループ機能不全 |
| 感情反応(VAS) | 急な刺激で8/10の不快感。易怒性あり | 扁桃体-NAc調整不全 |
| スプーン操作(食事動作) | 手の震えあり。成功率60% | NAcコア-運動系連携低下 |
| 食欲・活動への興味 | 両方著明に低下 | NAcシェルの機能低下(アンヘドニア) |
セッション展開(田中先生 & 石川さん)
初回評価と信頼関係の構築(FIS主体 ― 安心・予測可能な環境)
使用スケジュール:FIS(固定間隔)。10分ごとに必ず進捗を石川さんと確認し、前向きなフィードバックを提供。初期の安心感・信頼関係形成を優先します。
意思決定練習(FRS主体 ― 回数連動の達成感)
使用スケジュール:FRS(固定比率)。「5回正解で報酬」という明確な達成ルールが石川さんのNAcに「あと◯回」のカウントダウン効果をもたらし、集中力と参加意欲を高めます。
感情制御訓練(VIS主体 ― 予測不能なタイミングの称賛)
使用スケジュール:VIS(可変間隔)。呼吸法の実施を継続させながら、称賛のタイミングを意図的に不規則にすることで「次はいつ褒められるか」という期待感が持続的なNAc活性化につながります。
食事動作(スプーン)練習 → 退院後の維持期(VRS主体 ― 最大の長期動機づけ)
使用スケジュール:VRS(可変比率)。退院後の自宅での自主練習継続において、家族の「予測不能な称賛」がVRSとして機能し、側坐核を最大に活性化させ長期的な行動維持をサポートします。
確認クイズ & よくある質問(FAQ)
🧩 側坐核 確認クイズ(10問)
✅ 回答(解説付き)
よくある質問(FAQ)
側坐核はリハビリにどう直接関係するのですか?
リハビリセラピストがNAcを理解することで、①患者の「やる気がない」が神経学的な問題か意志の問題かを鑑別できる ②強化スケジュールを根拠を持って選択できる ③家族・介護者への教育内容が具体化できる という3つの臨床的メリットがあります。
特に脳卒中後うつ・アパシー・前脳基底部損傷の患者では、運動能力の改善だけでなくNAcの活性化を目標に含めた介入設計が回復の鍵となります。
依存症のある患者のリハビリで気をつけることは?
① 強化スケジュールを意図的に設計し、リハビリ自体を報酬として経験できる機会を増やす
② 「依存対象が得られない状況でのリハビリ参加」という環境のストレスに配慮する
③ チームで精神科・心療内科・ソーシャルワーカーと連携し、依存症治療とリハビリを並行して進める
④ VRS(可変比率)は依存傾向のある患者では慎重に使用。過剰な期待感の形成を避けるため、初期はFIS(固定間隔)の予測可能な環境から始める
リハビリを「もう一つの依存」にしないよう、内発的動機(「できた喜び」)の育成を長期的な目標として設定することが重要です。
アパシーとうつ病の違いをNAcの観点から教えてください。
アパシー(Apathy):側坐核と前頭前皮質の接続不全による「動機づけの消失」が主体。悲しみや苦痛の感情は乏しいが、何もしたくない・何に対しても興味が持てない状態。うつ病と比較して抗うつ薬の効果が限定的な場合が多い。
うつ病(Depression):NAcの活動低下に加え、HPA軸(視床下部-下垂体-副腎皮質軸)の異常・セロトニン系の変化が加わった状態。悲しみ・絶望感・罪悪感などの感情的苦痛が前景に立つ。抗うつ薬・認知行動療法が有効。
評価にはStarkstein Apathy Scale(アパシー)とGDS / BDI(うつ病)を並行して使用し、鑑別することが推奨されます。
強化スケジュールを変えるタイミングはどう判断しますか?
① 行動の安定性:現在の課題を80〜90%の成功率で実行できるようになったら、次のスケジュールへ移行のサイン。
② 感情的反応の変化:初期の不安・緊張が軽減し、リハビリへの参加が「当たり前」になってきたら、FIS → FRSへの移行タイミング。
③ 退院・在宅移行のタイミング:医療者の管理から離れる前に、外部報酬(セラピストの称賛)から内発的動機(自己達成感)へシフトさせるため、VRSへの移行を計画的に行います。
「このスケジュールは有効か?」の確認には、行動の頻度・持続時間・エラー率の変化を記録し、2〜3週単位でモニタリングすることをお勧めします。
運動療法(歩行練習など)は側坐核に直接効きますか?
臨床的には特に3つの点が重要です。
① 強度は中等度(50〜70% HRmax)が最適:過剰な高強度は逆にコルチゾール過剰でNAc機能を抑制する可能性があるため、「ちょっと息が上がる程度」を目安にします。
② 運動直後の達成感の言語化が追加効果をもたらす:運動によるDA放出に加えて「今日うまくできたこと」を患者自身に言語化させることで、オピオイド系のliking反応が加わり報酬学習が二重に強化されます。
③ 睡眠の確保が前提条件:睡眠不足はNAcの報酬受容を著明に低下させます(Yoo et al. 2012)。運動効果を最大化するには「眠れていますか?」の問診が必須です。
つまり「運動すること自体がNAcの薬になる」というのは神経科学的に根拠のある考え方であり、「意欲を高めてからリハビリをするのではなく、リハビリをすることで意欲が高まる」という逆算的アプローチが有効です。
「Wanting(欲しい)とLiking(好き)」の区別は実臨床でどう使いますか?
① 患者の状態アセスメントに使う:「リハビリには毎回来るが表情が暗い・楽しそうではない」→ wanting(動機)は残存しているがliking(快楽体験)が低下している状態。うつ・慢性疼痛・過度な疲労・薬剤副作用が疑われます。→ 課題の楽しさ・達成感を高める工夫(好きな音楽・得意な動作)を優先。
② 家族への説明に使う:「家ではやると言うがやらない(wanting低下 = アパシー)」と「楽しいと言うが忘れてしまう(liking正常 / 記憶障害)」は全く異なります。この区別を家族に伝えることで、適切なサポートの方向性(促すか・待つか・記録するか)が変わります。
③ 介入設計に使う:wanting低下が主↓ → 強化スケジュール(FRS・VRS)で動機を外部から賦活。liking低下が主↓ → 課題の意味付け・小さな成功体験・痛みの軽減・音楽療法など快楽体験の質を高める介入を優先。
「やる気がない」を一括りにせず、wanting と liking のどちらが問題かを分けて考えることが、的外れな介入を防ぐ最短ルートです。
参考文献・引用文献
- 1) Ziehen T. Anatomische, physiologische und klinische Beiträge zur Kenntnis der Ammon’shorn-Formation. Med Klin. 1897. (”Nucleus accumbens septi”の命名者。ただし現代的な機能的研究の起点は1954年のOlds & Milnerとされる)
- 2) Olds J, Milner P. Positive reinforcement produced by electrical stimulation of septal area and other regions of rat brain. J Comp Physiol Psychol. 1954;47(6):419-427.
- 3) Schultz W, Dayan P, Montague PR. A neural substrate of prediction and reward. Science. 1997;275(5306):1593-1599. 【報酬予測誤差とドーパミン放出の古典的論文】
- 4) Berridge KC, Robinson TE. What is the role of dopamine in reward: hedonic impact, reward learning, or incentive salience? Brain Res Brain Res Rev. 1998;28(3):309-369. 【Wanting/Liking理論の原著】
- 5) Berridge KC, Kringelbach ML. Pleasure systems in the brain. Neuron. 2015;86(3):646-664. 【快楽ホットスポット・コールドスポットのヒトを含む最新レビュー】
- 6) Cardinal RN, Parkinson JA, Hall J, Everitt BJ. Emotion and motivation: the role of the amygdala, ventral striatum, and prefrontal cortex. Neurosci Biobehav Rev. 2002;26(3):321-352.
- 7) Everitt BJ, Robbins TW. Neural systems of reinforcement for drug addiction: from actions to habits to compulsion. Nat Neurosci. 2005;8(11):1481-1489.
- 8) Schlaepfer TE, Cohen MX, Frick C, et al. Deep brain stimulation to reward circuitry alleviates anhedonia in refractory major depression. Neuropsychopharmacology. 2008;33(2):368-377.
- 9) Hannah S, Dickson T. Behavior Modification. In: StatPearls. Treasure Island (FL): StatPearls Publishing; 2022. NBK459285
- 10) Starkstein SE, Mayberg HS, Preziosi TJ, et al. Reliability, validity, and clinical correlates of apathy in Parkinson’s disease. J Neuropsychiatry Clin Neurosci. 1992;4(2):134-139.
- 11) Greenwood BN, Foley TE, Le TV, et al. Long-term voluntary wheel running is rewarding and produces plasticity in the mesolimbic reward pathway. Behav Brain Res. 2011;217(2):354-362. 【運動とNAcドーパミン系改善のエビデンス】
- 12) Yoo SS, Gujar N, Hu P, et al. The human emotional brain without sleep — a prefrontal amygdala disconnect. Curr Biol. 2007;17(20):R877-R878. 【睡眠不足と報酬系の関係】
- 13) Hatem SM, Saussez G, Della Faille M, et al. Rehabilitation of Motor Function after Stroke: A Multiple Systematic Review. Front Hum Neurosci. 2016;10:442.
- 14) David FJ, Robichaud JA, Leurgans SE, et al. Exercise improves cognition in Parkinson’s disease: The PRET-PD randomized, clinical trial. Mov Disord. 2015;30(12):1657-1663.
- 15) Levy R, Dubois B. Apathy and the functional anatomy of the prefrontal cortex-basal ganglia circuits. Cereb Cortex. 2006;16(7):916-928.
- 16) Mogenson GJ, Jones DL, Yim CY. From motivation to action: functional interface between the limbic system and the motor system. Prog Neurobiol. 1980;14(2-3):69-97. 【limbic-motor interfaceの古典】
- 17) Robert PH, Clairet S, Benoit M, et al. The apathy inventory: assessment of apathy and awareness in Alzheimer’s disease, Parkinson’s disease and mild cognitive impairment. Int J Geriatr Psychiatry. 2002;17(12):1099-1105.
- 18) Pontifex MB, Gwizdala KL, Parks AC, et al. The association between physical activity and working memory in younger and older adults. Neuropsychology. 2019;33(3):411-423.
リハビリを受けた方の声 ― 報酬系介入で変わった回復
入院していたとき「やる気がない患者」と言われているのが聞こえてきて、自分でもどうしようもないと思っていました。STROKE LABで先生が「やる気が出ないのは性格ではなく脳の傷のせいです」と説明してくれて、初めて涙が出ました。10回歩いたら必ずシールをもらえる仕組みにしてもらってから、「あと何回」を数えながら練習できるようになりました。
60代男性・前脳基底部梗塞(ホイブナー動脈閉塞)発症後5ヶ月
夫が「リハビリには行くが全然楽しそうじゃない」という状態が続いていました。STROKE LABで「WantingとLikingが別々に壊れている可能性がある」と説明を受け、毎回のセッションの終わりに「今日一番うまくできたことは?」と夫自身に言わせる習慣を始めました。3週間後には「今日は左手が少し動いた気がした」と自分から話し始めました。
70代男性のご家族・脳卒中後アパシーへの対応として
側坐核の知識を活かした
「動機づけ最大化リハビリ」をSTROKE LABで。
報酬系・神経行動学に基づく脳卒中・神経疾患リハビリを提供します。
「やる気が続かない」「なかなか回復しない」とお感じの方はご相談ください。

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)












