【2026年版】ゴルジ腱器官(GTO)とIb抑制を完全解説!効果的リハビリアプローチ、メカニズムと実践法を解説
ゴルジ腱器官(GTO: Golgi Tendon Organ)は、筋腱移行部に存在する感覚受容器であり、筋張力を感知して脊髄への信号(Ib線維)を介した抑制性フィードバックを発生させます。この「Ib抑制」は脳卒中後の痙縮管理・PNF・アイソメトリックトレーニングなど、リハビリテーション臨床のあらゆる場面で応用されています。本記事では、GTOの解剖・生理から古典論文(Houk 1967)の知見、そして具体的な介入技術まで体系的に解説します。
ゴルジ腱器官(GTO:Golgi Tendon Organ)は筋腱移行部に存在する感覚受容器で、筋収縮による張力変化を感知します。Ib感覚線維を介して脊髄介在ニューロンに信号を送り、同筋の運動ニューロン活動を抑制(Ib抑制:autogenic inhibition)することで、腱・筋の過負荷損傷を防ぎます。1967年のHouk論文では、GTOは他動伸張よりも能動的な筋収縮に対してより鋭敏に反応することが示され、「ストレッチよりも筋収縮を促す方がIb抑制を引き出しやすい」という臨床的示唆が得られました。脳卒中後の痙縮・筋緊張亢進への応用、PNF・アイソメトリック収縮・徒手療法での活用法まで徹底解説します。
- 正式名称:Golgi Tendon Organ(ゴルジ腱器官)。腱紡錘とも呼ばれる。19世紀末〜20世紀初頭にCamillo Golgiが記載(詳細な記載年は文献によって幅がある)
- 位置:筋腱移行部(MTJ: musculotendinous junction)。筋線維が腱に移行するコラーゲン繊維束の間に索状に配列
- 感覚線維:Ib線維(有髄・太い・高速伝導 約70〜120 m/s)。筋紡錘はIa線維で受容
- 検出対象:主に筋張力(force)。筋紡錘が筋長(length)を感知するのと対照的
- Ib抑制(Autogenic inhibition):GTO → Ib線維 → 脊髄Ib介在ニューロン(抑制性)→ 同筋の運動ニューロンを抑制 → 筋弛緩。過度な筋収縮から腱を保護する生体防御反応
- Houk 1967の重要知見:GTOは他動伸張(160g)よりも能動的な筋収縮(18g)に対してより強く発火する。能動収縮の方が同等以上のGTO活性化を低い張力で引き出せる
- 筋線維全体への分布:同論文より、すべての筋線維に腱紡錘が付着しているわけではない(文献によって1つのGTOには3〜25本の筋線維が接続)。多くの筋線維を動員するほどIb抑制を引き出しやすい可能性
- 脳卒中・痙縮との関係:上位運動ニューロン損傷では脊髄抑制回路が障害され、Ib抑制が正常に機能しにくい。リハビリでは意図的にGTOを活性化して抑制を促す
- 臨床応用:アイソメトリック収縮・PNFストレッチ・静的ストレッチ・徒手圧迫(腱圧迫法)・関節モビライゼーション・低負荷持続収縮の6手技でIb抑制を誘導できる
- GTOの受容器特性:GTOは緩徐順応型(slowly adapting)受容器。持続的な張力変化に安定して発火する。速順応型(パチニ小体)とは異なり「リズミカルな刺激に特異的に敏感」ではない。臨床での繰り返し圧迫は「各サイクルが新たな機械的イベントを生成するため」に有効
- Ib回路の文脈依存性:Ib介在ニューロンは「常に抑制性」ではない。歩行立脚後期では促通的に切り替わり(脊髄CPGによる制御)、腓腹筋・ヒラメ筋のpush-offを支援する。歩行訓練中の過剰なIb抑制は push-off を弱める可能性に注意
- 脊髄解剖の正確な理解:Ib線維の主要シナプス部位は脊髄中間帯〜後角深部(主にlaminae V〜VII)。この部位でIb介在ニューロンと接続し、複数の筋群への出力を統合制御する
- 折りたたみナイフ現象:痙縮関節の他動運動時に「初期抵抗→急激な抵抗消失」が生じる現象。GTOのIb抑制が主要な要素の一つとして関与(グループIII/IV線維の侵害受容性入力も寄与)。この現象が観察される患者はGTO介入の適応あり
ゴルジ腱器官(GTO)とは ― 解剖・位置・基本機能
ゴルジ腱器官(GTO)は、19世紀末〜20世紀初頭にイタリアの神経解剖学者Camillo Golgiによって記載された固有受容器(proprioceptor)の一種です(詳細な記載年は文献によって幅がある)。主に骨格筋の筋腱移行部に位置し、筋収縮によって生じる張力(テンション)を精密に感知する役割を担います。
📍 GTOの解剖学的位置と構造
GTOは筋腱移行部(MTJ: musculotendinous junction)に存在します。コラーゲン繊維束(腱線維)の間に索状・カプセル状に包まれた神経終末が分布しており、1つのGTOには通常文献によって3〜25本の筋線維が直列に接続されています(Jami 1992)。この「直列接続」がGTOの機能的特性を決定づけています。
筋が収縮すると、GTOに直列に繋がった筋線維から直接的な張力がかかり、コラーゲン繊維束が変形してIb線維の神経終末が機械的に刺激されます。この仕組みにより、GTOは筋全体の総張力ではなく、接続されている特定の筋線維群の張力を選択的に検出します。
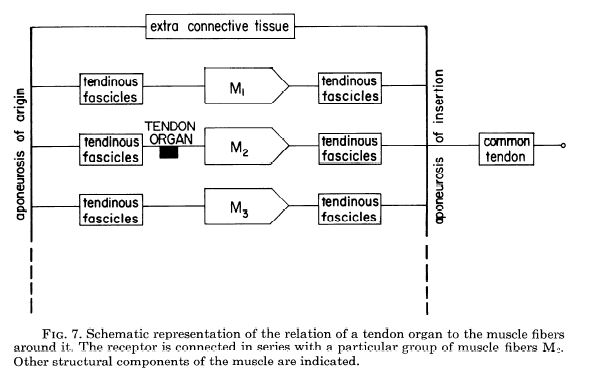
図:筋線維と腱紡錘のイメージ(Houk 1967より)。すべての筋線維にGTOが付着しているわけではない
GTOの4つの基本機能
🛡️ 過負荷保護
筋張力が過度に高まると、Ib抑制によって同筋の収縮を自動的に抑制。腱・筋の断裂・損傷を防ぐ最後のブレーキシステムとして機能します。
📊 張力モニタリング
筋が発揮している力(張力)を中枢神経系へリアルタイムで報告。小脳・大脳皮質が筋力制御の精密なフィードバック調整を行うための情報源となります。
⚖️ 筋緊張の調整
安静時の筋緊張(トーヌス)の調整にも関与。Ib抑制回路が正常に機能することで、適切な筋緊張レベルが維持されます。
🔄 協調運動への貢献
拮抗筋・協調筋との相互抑制を通じて、スムーズな関節運動を実現。Ib線維は脊髄で広範なニューロンに接続し、多関節にわたる協調制御に貢献します。
⚠️ よくある誤解:GTOは「危険センサー」だけではない
古い教科書には「GTOは筋損傷を防ぐための緊急ブレーキ」という記述のみが見られることがありますが、現在の理解ではGTOは通常の筋活動中も継続的に発火しており、常時フィードバックを提供しています。閾値は高い(かつては静的伸張でほとんど反応しないとされた)とされていましたが、Houk(1967)の論文が示したように、能動的な筋収縮に対してはきわめて低い張力でも反応します。GTOを「ほとんど発火しない受動的なセンサー」と捉えるのは誤りです。
Ib抑制のメカニズムと神経回路
Ib抑制(自原性抑制:autogenic inhibition)は、GTOが感知した張力情報が脊髄の抑制性介在ニューロンを経由して、同筋の運動ニューロンに届く抑制性フィードバック回路です。
🔬 Ib抑制の神経回路(ステップバイステップ)
Step 1:筋が収縮(または他動伸張)する → 筋腱移行部に張力が発生
Step 2:GTOのコラーゲン繊維束が変形 → Ib線維の神経終末が機械的に活性化
Step 3:Ib線維が高速(約70〜120 m/s)で脊髄に入力 → 後根から進入し、主に脊髄中間帯〜後角深部(laminae V〜VII)に終止。「感覚伝達を担う後角浅部」とは主な終止域が異なる
Step 4:脊髄内のIb介在ニューロン(主に抑制性)にシナプスを形成 → グリシン・GABAによる抑制性シナプス後電位(IPSP)を生成。ただし文脈依存的な重要な例外あり(後述)
Step 5:同筋のα運動ニューロン活動が抑制される → 筋収縮力が低下・弛緩(autogenic inhibition)
補足:Ib介在ニューロンは拮抗筋の運動ニューロンへの興奮性接続も持ち、拮抗筋の収縮(相反支配)を促す方向にも働きます。また、Ib回路は皮質脊髄路・脳幹路からの下行性制御を強く受けるため、上位中枢の状態によって抑制の強さが大きく変化します。
Ib抑制回路の概要
| 回路の要素 | 役割 | リハビリへの影響 |
|---|---|---|
| GTO(Ib受容器) | 筋張力を感知して信号を発生 | GTOを活性化する介入を選択する根拠 |
| Ib感覚線維 | 高速伝導(約70〜120 m/s)で脊髄中間帯〜後角深部へ | 介入の効果は即時に現れやすい |
| Ib介在ニューロン(抑制性) | 運動ニューロンへIPSPを発生 | 脳卒中では下行路障害でこの抑制が弱まる |
| α運動ニューロン | 抑制されることで筋張力が低下 | 痙縮の抑制・筋弛緩の誘導が目的 |
| 皮質脊髄路(下行性制御) | Ib回路全体の感度を調節 | 脳卒中では損傷により異常な過興奮状態に |
💡 Ia抑制(相反抑制)との比較
Ib抑制としばしば混同されるのがIa抑制(相反抑制:reciprocal inhibition)です。両者を明確に区別することが臨床推論の精度を高めます。Ia抑制は筋紡錘から発するIa線維が脊髄Ia介在ニューロンを介して拮抗筋の運動ニューロンを抑制するもので、一側の筋が収縮すると反対側の筋が弛緩するメカニズムです。
Ib抑制はGTOから発するIb線維が同筋(収縮中の筋そのもの)の運動ニューロンを抑制するため「自原性抑制(autogenic inhibition)」とも呼ばれます。どちらもリハビリで活用されますが、目的(拮抗筋抑制 vs 同筋の過緊張抑制)が異なります。
⚠️ 重要:Ib抑制は「常に抑制性」ではない ― 文脈依存的な回路切り替え
教科書的なIb抑制(自原性抑制)は「GTOが活性化 → 同筋を抑制」という単純な負のフィードバックとして描かれますが、生体の実際の神経回路はより複雑です。Pearsonら(1998)をはじめとする研究が示したように、Ib介在ニューロンの出力は上位中枢(皮質・脳幹・脊髄内固有回路)からの文脈依存的な制御を受け、状況によって促通性に切り替わることがあります。
特に重要な例として、歩行の立脚後期があります。立脚後期(踏み蹴り局面)では、足底・足関節伸筋群のGTOが大きな張力を感知しますが、この局面では通常の「Ib抑制(伸筋を抑える)」ではなく、むしろ伸筋運動ニューロンへの促通的な出力へと切り替わることで力強い蹴り出し(push-off)が可能となります。脊髄腰髄〜仙髄レベルに存在すると推定される歩行発生器(CPG: Central Pattern Generator)がIb介在ニューロンへの入力を調節し、立脚期には「GTOの活性化 = 伸筋をさらに働かせ続ける」という正のフィードバックが機能します。歩行開始指令は脳幹の中脳歩行誘発野(MLR: Mesencephalic Locomotor Region)から降りてきますが、実際のリズム生成と感覚フィードバック処理の中枢は脊髄にあります(CPGの詳細な脊髄局在は動物実験に基づく推定であり、ヒトでの解剖学的局在は研究中)。
つまり「Ib回路 = 常に抑制」という理解は不正確であり、同じGTOの信号が「安静時・痙縮管理では抑制的に」「正常歩行では促通的に」機能する二面性を持つことを臨床家は認識する必要があります。脳卒中後にこの脊髄CPGレベルの切り替えが障害されると、立脚後期の蹴り出しが弱くなる(push-off の欠如)という歩行パターン異常につながります。
折りたたみナイフ現象(Clasp-knife Phenomenon)との関係
痙縮の臨床評価でよく観察される折りたたみナイフ現象(clasp-knife phenomenon)は、Ib抑制と関連した現象です。痙縮のある関節を他動的に動かすと、最初は強い抵抗感(過剰な伸張反射)がありますが、ある閾値に達すると抵抗が急激に消失してナイフが折れるように動かせるようになります。
| フェーズ | 主なメカニズム | 臨床での観察 |
|---|---|---|
| 初期抵抗相 | 筋紡錘のIa反射亢進(速度依存性) | 他動運動開始直後の強い抵抗感 |
| 抵抗消失相(ナイフが折れる) | GTOのIb抑制が閾値を超えて起動(主要メカニズムの一つ)+グループIII/IV線維(侵害受容性入力)の関与(Burke et al. 1972) | 一定の張力以上で突然抵抗が抜ける感触 |
折りたたみナイフ現象を「Ib抑制回路の残存確認」として活用する
折りたたみナイフ現象が観察される患者では、GTOのIb抑制回路が少なくとも部分的に機能していると考えられます(グループIII/IV線維の侵害受容性入力も関与するため、GTO単独の証拠とは限らないことに留意)。逆に、重度の痙縮で折りたたみナイフ現象が消失している場合は、脊髄抑制回路の障害が高度であることを示唆します。評価時にこの現象の有無・程度を確認することで、GTO介入の効果が期待できるかの予測に役立ちます。また、ボツリヌス毒素投与後には筋紡錘からの過剰な入力が抑制されることで、残存するIb抑制回路がより機能的になり、リハビリ効果が高まる「介入の窓」が生まれます。
古典論文解説:Houk 1967「ネコ・ヒラメ筋の自動収縮時のGTO反応」
📄 論文情報
タイトル:Responses of Golgi tendon organs to active contractions of the soleus muscle of the cat.
著者・掲載:Houk J. J Neurophysiol. 1967 May;30(3):466-81. PubMed → 6037588
なぜ重要か:GTOは静的な他動伸張には反応しにくいという従来の定説を覆し、能動的な筋収縮に対してはきわめて低い張力でも強く発火することを実証した古典的研究。PNF・アイソメトリック収縮がIb抑制に有効な理論的根拠を提供する。
注意点:ネコを対象とした高度に人工的な実験条件(前根の選択的電気刺激)での結果であり、ヒト生体内での複雑な神経筋相互作用を完全には再現していない。ヒト臨床への外挿は有望だが、過度な一般化は避けるべき。
研究の背景と目的
1967年当時、GTOに関する主要な争点は「能動的な筋収縮と他動的な伸張でGTOの反応閾値は同じか、異なるか」という問いでした。一部の研究では「どちらも同じ閾値で反応する」とされていた一方、別の研究では「能動収縮ではGTOの閾値がはるかに低い(より敏感に反応する)」とも言われていました。Houkはこの矛盾を解決するため、精密な電気生理学実験を設計しました。
実験デザイン:ネコのヒラメ筋・単一神経線維記録
他動的な張力(160g)をベースとした状態から、L7〜S1前根のどちらか一方を周波数刺激してヒラメ筋の一部に能動収縮を誘発。各腱紡錘の発火パターンを比較しました。単一刺激では計測に支障が生じるため、反復刺激(10〜20 Hz)を採用し、筋疲労を防ぐために過度な高周波を避けた工夫がされています。
結果と考察 ― 臨床への示唆
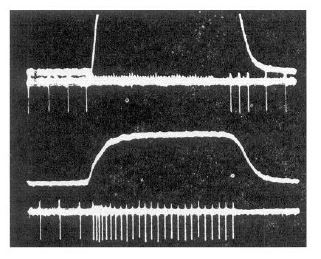
図:筋収縮(上線)と腱紡錘の発火(下線)の記録(Houk 1967より引用)。上部・下部で異なる前根を刺激
| 条件 | 張力 | GTOの反応 | 臨床的解釈 |
|---|---|---|---|
| 図(上部):強い筋収縮 | 非常に大きい(図外) | 腱紡錘の発火が停止(サイレント期) | Houk自身は電気的アーティファクトの混入を主な考察として挙げた。また、前根への同期した大きな電気刺激により収縮筋線維がGTOへの有効張力を変化させた可能性も考察されている。「GTOが飽和した」あるいは「接続筋線維への張力伝達が変化した」などの解釈は著者考察の一部であり、確定的な機序ではない点に注意 |
| 図(下部):弱い能動収縮 | 18g のみ | 他動160gより強い発火増加 | 少ない張力でも能動収縮なら十分なGTO活性化が可能 |
| 他動伸張(ベースライン) | 160g | 発火あるが増加は少ない | ストレッチ単独では同等のGTO活性化に大きな張力が必要 |
GTOは他動的な伸張(160g)よりも、わずか18gの能動的筋収縮でより多く発火しました。これは「GTOは直列に接続された筋線維の能動収縮に対して特に敏感である」ことを示します。リハビリ臨床において、痙縮の緩和や筋緊張の抑制を目的とする場合、ストレッチよりも適切な筋収縮を促すアプローチの方がGTOをより効率的に活性化できる可能性があります。ただし、これはネコを対象とした実験データであり、その後のヒト研究でも基本的な傾向は支持されているが、臨床への外挿は慎重に行うべき。
「全筋線維の動員」がIb抑制の量を決める
Houk(1967)の考察では、すべての筋線維にGTOが付着しているわけではなく(文献によって1つのGTOに3〜25本の筋線維が接続;Jami 1992)、より多くの筋線維を動員できるかどうかがIb抑制の強度を左右します。これは「どうすれば効率よくIb抑制を引き出せるか」という臨床的問いへの重要なヒントです。
具体的には:①随意的な最大収縮を引き出す課題設定、②神経筋促通法(PNF)でより広い筋線維を動員、③中枢活性化(声かけ・注意誘導)による募集閾値の最適化、④痙縮がある筋では緩やかな等尺性収縮から開始して段階的に動員を拡大する、といったアプローチが根拠づけられます。
GTO vs 筋紡錘 ― 2つの固有受容器を整理する
| 比較項目 | ゴルジ腱器官(GTO) | 筋紡錘(Muscle Spindle) |
|---|---|---|
| 位置 | 筋腱移行部(腱に直列) | 筋腹内(筋線維に並列) |
| 感知対象 | 筋張力(force) | 筋の長さ・伸張速度(length/velocity) |
| 感覚線維 | Ib線維(約70〜120 m/s) | Ia線維(一次終末 70〜120 m/s)+II線維(二次終末) |
| 脊髄での接続 | Ib介在ニューロン(抑制性) | Ia介在ニューロン・α運動ニューロン(興奮性) |
| 最終効果 | 同筋の収縮を抑制(Ib抑制) | 同筋の収縮を促進(伸張反射)+拮抗筋を抑制 |
| γ運動ニューロンによる調節 | なし(GTOの感度は直接調節されない) | あり(γニューロンが筋紡錘の感度を調節) |
| 臨床的意味 | 痙縮・過緊張の抑制に応用 | 運動促通・反射亢進(痙縮の機序)に関与 |
| リハビリでの活用例 | PNF収縮弛緩・等尺性収縮後弛緩・腱圧迫 | タッピング・クイックストレッチ・振動刺激 |
💡 なぜ「筋紡錘を抑制してGTOを活性化」がリハビリの基本戦略なのか
脳卒中後の痙縮では、上位運動ニューロン損傷により脊髄の抑制回路(Ib回路・Ia抑制回路)が機能低下し、筋紡錘のIa反射が過剰になります。この状態で「ストレッチだけ行う」と、かえって筋紡錘が刺激されて伸張反射が亢進し、痙縮を悪化させるリスクがあります。
そこでGTOのIb抑制を意図的に利用する介入(等尺性収縮・PNF・腱圧迫など)が重要になります。能動的な筋収縮でGTOを活性化し、抑制性シグナルを脊髄に送ることで、過剰な筋緊張を「内側から抑える」ことができます。Houk(1967)が示した「能動収縮でのGTO高感受性」は、この臨床戦略の直接的な基礎根拠です。
脳卒中・痙縮患者へのIb抑制の応用
過剰な筋緊張亢進
内因性抑制を引き出す
脳卒中後の痙縮(spasticity)は、皮質脊髄路の損傷により脊髄の抑制機構が機能低下し、筋紡錘のIa反射が過剰になった状態です。NIHSSの採点(特に項目5・6の上下肢運動)でも高スコアとなる患者では、痙縮が日常生活動作(ADL)や介護負担の大きな障壁となります。
⚠️ 脳卒中患者でのGTO機能と注意点
① Ib抑制回路自体の機能低下:脳卒中では上位中枢からの下行性制御が低下するため、Ib介在ニューロンの活動性も変化します。健常者と同じ介入でも効果が出にくい場合があり、より高い張力・反復刺激が必要なことがあります。
② 痙縮筋への収縮誘導の難しさ:痙縮が強い筋では随意的な収縮を誘導しにくく、電気刺激(NMES)や徒手的なファシリテーションを組み合わせた上でGTOを活性化する工夫が必要です。
③ 疼痛への配慮:過度な張力刺激は肩関節亜脱臼・腱炎のリスクを高めます。患者の疼痛評価を行いながら、適切な関節肢位・抵抗量でIb抑制を誘導してください。
| 痙縮の程度(MAS) | GTOを活性化する介入の選択 | 注意事項 |
|---|---|---|
| 軽度痙縮(MAS 1〜1+) | ||
| 関節可動域内での動き | アイソメトリック収縮・静的ストレッチ・PNFの等尺性収縮後弛緩(CR法) | 随意運動が残存しているので本人の努力を引き出す課題設定を |
| 中等度痙縮(MAS 2) | ||
| ROMが制限されてきている | 徒手腱圧迫・NMES併用アイソメトリック・関節モビライゼーション後にGTO活性化 | 他動的に関節をゆっくり動かした後に能動収縮を試みる |
| 重度痙縮(MAS 3〜4) | ||
| 拘縮傾向・ADL著明障害 | 持続的低負荷収縮・長時間静的ストレッチ(30分以上の装具・スプリント)・ボツリヌス毒素後のIb促通介入 | ボツリヌス投与後の「介入の窓」期間(効果発現:投与後2〜4週、効果持続:3〜4ヶ月)に集中的にIb抑制トレーニングを行う |
H反射を用いたIb抑制の臨床評価
GTOのIb抑制を直接評価する簡便な臨床検査は現時点では確立していませんが、H反射(Hoffmann反射)を用いたプロトコルによって脊髄の抑制回路の機能を間接的に評価できます。
🔬 H反射によるIb回路評価の概要
原理:後脛骨神経(腓腹筋・ヒラメ筋を支配)に電気刺激を与えると、Ia線維を介した単シナプス反射(H反射)が生じます。このH反射の振幅を「conditioning-test(条件刺激−試験刺激)プロトコル」で評価することで、脊髄レベルでの抑制回路の機能を推定できます。
Ib抑制の評価:GTOを機械的に刺激(条件刺激)した後にH反射(試験刺激)を測定し、H反射振幅の減少量を定量化することでIb抑制の強度を推定します。脳卒中後の痙縮患者では、このIb抑制量が健常者と比較して有意に低下していることが報告されています(Yanagawa et al. 1990)。
臨床的意義:H反射プロトコルは特殊な電気生理学検査装置を要するため一般的なリハビリ外来では難しいですが、神経生理学専門外来や研究施設では利用可能です。Ib介入の効果判定や脊髄回路の回復モニタリングに活用されています。代替的に、MAS・ROM測定・折りたたみナイフ現象の観察を組み合わせた臨床的評価が実用的です。
歩行周期とGTO ― Ib抑制から促通への切り替え
歩行という機能的文脈においてGTOとIb回路は特別な役割を担います。安静時や痙縮管理文脈で「GTOは抑制を引き出す」と説明しますが、正常歩行では同じGTOの信号が促通的に機能する局面があることは特筆すべき重要な生理学的事実です。
| 歩行周期の局面 | GTOの活動 | Ib回路の働き | 機能的意味 |
|---|---|---|---|
| 前遊脚期〜遊脚期 | |||
| 遊脚初期(下腿が離地) | 足関節伸筋GTOの活動低下 | Ib抑制が解除 | 下肢屈筋の活性化・下腿の振り出し開始 |
| 立脚期 | |||
| 荷重応答期(初期接地) | 足底圧・足関節背屈筋GTO活性化 | 抑制的(過剰な収縮防止) | 接地衝撃の吸収・適切なトルク制御 |
| 立脚中期〜後期(push-off) | 腓腹筋・ヒラメ筋GTO活性化が最大 | 促通的に切り替わる(脊髄CPGによる制御) | 力強い踏み蹴り(push-off)を持続させるための正のフィードバック |
⚠️ 歩行リハビリでのIb抑制の過剰適用に注意
脳卒中患者の歩行訓練中に、立脚後期の下腿筋(腓腹筋・ヒラメ筋)の緊張亢進を「常にIb抑制で緩めるべき」と単純に考えるのは危険です。立脚後期の腓腹筋・ヒラメ筋の活動はpush-offに不可欠であり、Ib抑制で過度に緩めると逆にpush-offが弱まり歩行効率が低下します。GTO介入による痙縮管理は安静時・前作業準備(warm-up)として行い、歩行訓練中は適切な筋活動を促通しながら歩行課題を遂行することが重要です。
パーキンソン病・脊髄損傷へのIb抑制応用
GTO・Ib抑制の臨床応用は脳卒中後の痙縮管理にとどまりません。パーキンソン病(PD)や脊髄損傷(SCI)でも、固有感覚系の機能変容とGTO介入の有用性が議論されています。
パーキンソン病(Parkinson’s Disease)とIb抑制
パーキンソン病の筋固縮(鉛管様・歯車様)は、痙縮とは神経生理学的に異なります。痙縮が速度依存性の伸張反射亢進(Ia主体)であるのに対して、固縮はIa・Ib双方の回路を含む複合的な脊髄運動制御の変容によって生じると考えられています(Johnels 1982)。ドパミン不足による基底核−視床−皮質ループの機能異常が脊髄抑制回路に影響を与え、固縮を引き起こします。
💡 PDへのGTO介入の実際
有効とされる手技:①等尺性収縮後弛緩(HR法)による固縮筋の一時的緩和 → その直後に機能的動作訓練を行う「プライミング」として活用。②リズミック・スタビライゼーション(PNFの一技法:交互の等尺性収縮)で体幹・四肢の固縮を緩和し、体重移動訓練の準備を整える。
注意点:PDでの固縮緩和効果は脳卒中後の痙縮と比べてより一時的であり、ドパミン薬の「ON時間」に合わせた介入タイミングが重要です。OFF時間(薬効切れ)での介入は効果が著しく低下することがあります。また、PD固有の姿勢異常(前傾姿勢・すくみ足)に対してはGTO介入単独ではなく、視覚・聴覚キュー・LSVT BIG等との組み合わせが推奨されます。
脊髄損傷(Spinal Cord Injury)とIb抑制
脊髄損傷後の痙縮は脳卒中後と同じく上位中枢からの下行性制御喪失によりますが、損傷が脊髄自体にあるため、Ib回路の介在ニューロンが直接損傷される可能性もあります(損傷レベルによる)。
| 損傷タイプ | Ib抑制回路の状態 | 介入の選択 |
|---|---|---|
| 不完全損傷(AIS C〜D) | 部分的に残存。介入への反応性あり | PNF・等尺性収縮・腱圧迫法が適用可能。能動収縮が引き出せる筋群に優先介入 |
| 完全損傷(AIS A〜B) | 下行性制御は完全遮断。GTO自体は正常だが抑制回路は機能低下 | FES(機能的電気刺激)でGTOを活性化し、脊髄反射レベルでのIb抑制を誘導。長時間伸張・ポジショニングを主軸に |
具体的介入技術6選 ― 手順・目的・臨床ポイント
🔑 Ib抑制介入の共通原則
① 能動収縮を優先:Houk(1967)が示した通り、他動ストレッチより能動的収縮の方がGTOを効率的に活性化できます。患者自身の収縮努力を最大限に引き出してください。
② 適切な張力を選択:過大な張力は逆に筋紡錘を興奮させ痙縮を悪化させる可能性があります。「心地よい収縮感」が得られる範囲で実施します。
③ 患者の主観的フィードバックを常に確認:「緊張が和らいでいるか」「痛みはないか」を確認しながら進めます。
④ 反復・継続が重要:Ib抑制効果は一時的であり、繰り返しの介入が長期的な変化(シナプス可塑性)につながります。
アイソメトリック収縮(等尺性収縮)によるIb抑制
適切な肢位の設定
対象筋が短縮方向でも過度な伸張でもない「中間域」に関節を置きます。例:肘屈筋の痙縮には肘関節90〜100°程度。筋が最も収縮力を発揮できるポジションでGTOへの張力が最大化されます。
収縮の誘導(10秒間)
「力を入れてください」と口頭指示し、関節角度を変えずに対象筋を収縮させます。最大収縮の50〜70%程度の努力量が目安。評価者は同じ抵抗を維持します(等尺性)。
徐々に弛緩させる
10秒後「力を抜いてください」と指示し、ゆっくり弛緩させます。等尺性収縮の直後は後収縮弛緩(post-contraction depression)が生じており、Ib抑制の余韻が残ります。この弛緩直後を利用してROMを拡大する(CR法)か、筋が弛緩した状態を保持して次の収縮に移行するかを患者の状態に応じて選択してください。「何秒以内に伸張しなければならない」という厳密な生理学的窓があるわけではありませんが、弛緩を確認した後すみやかに(5〜10秒以内を目安に)次の操作を行うことで、後収縮弛緩の効果を最大限に活用できます。
弛緩直後に関節可動域を拡大(必要時)
弛緩効果を利用して他動的に関節をさらに伸張方向へ誘導することができます(CR法:Contract-Relax法)。痙縮筋のROM拡大に有効です。3〜5回繰り返します。
PNFストレッチング ― 収縮弛緩(Contract-Relax)法
静的ストレッチング(長時間低負荷)
筋をゆっくりと他動的に伸ばし、張力が加わった状態を保持します。GTOが継続的な張力を感知することで、Ib抑制が徐々に誘発されます。静的ストレッチは即効性では能動収縮法に劣りますが、長時間の持続張力(装具・スプリント・ポジショニングクッション)と組み合わせることで、痙縮の長期管理に有効です。
徒手による腱圧迫法(Tendon Pressure Technique)
患者をリラックスした体位に置く
座位または仰臥位でリラックスさせ、過度な筋緊張がかからないよう環境を整えます。
筋腱移行部を正確に触診・特定する
上肢:上腕二頭筋腱・手関節屈筋群の腱部。下肢:アキレス腱(腓腹筋・ヒラメ筋MTJ)・膝蓋腱(大腿四頭筋MTJ)など。筋腱移行部はしばしば「ロープ状の索状体」として触知できます。
適切な圧力を段階的に加える
親指または指先の腹面で腱方向に対して垂直に圧迫します。GTOは緩徐順応型(slowly adapting)受容器であり、持続的な機械的変形に対して安定して反応し続けます。圧迫の手技上の工夫として約1〜2秒の圧迫・解放サイクルを繰り返すことがありますが、これは「GTOがリズミカルな刺激に特異的に敏感だから」ではなく、各圧迫サイクルが新たな張力変化イベントを生成し、GTOを繰り返し活性化するためです。持続圧迫(5〜10秒)も同様に有効です。1セット10〜15回を目安に実施します。
筋の反応を触診・動作で確認
圧迫後に対象筋の筋緊張が低下しているかを触診・ROM測定で確認。効果不十分なら圧迫部位・角度・強度を調整して再試行します。
⚠️ 腱圧迫法の過剰刺激に注意
過度に強い圧迫や急激な刺激は逆に筋の反射性収縮を引き起こすことがあります。「強く押せば押すほど効果が出る」わけではなく、GTOが張力変化を「感知できる程度」の適切な圧力を選択することが重要です。患者が「圧迫感はあるが痛くない」と感じる強さを目安にしてください。
持続的低負荷収縮(Sustained Low-load Contraction)
最大筋力の20〜30%程度の軽い負荷で、持続的に筋を収縮させます。アイソメトリック収縮ほどの強度は必要なく、重度麻痺患者・高齢者でも実施しやすい技術です。小さな張力でも持続的にGTOを刺激することで、段階的なIb抑制の蓄積効果が期待できます。
関節モビライゼーション + Ib抑制促通
関節モビライゼーションでまず関節受容器(パチニ小体・ルフィニ終末)を刺激して関節周囲の緊張を緩和させた後、GTOを活性化するアイソメトリック収縮を行うという複合アプローチです。モビライゼーション直後は筋緊張が一時的に低下しやすく、GTO活性化のタイミングとして最適です。
6つの介入技術 ― 目的別・状態別の選択ガイド
どの手技を選ぶかに迷ったときは、以下の比較表を参照してください。複数の手技を組み合わせることで相乗効果が期待できます。
| 手技 | 主な適応 | 難易度 | 即効性 | 継続効果 | 最も向いている状況 |
|---|---|---|---|---|---|
| ①アイソメトリック収縮 | 軽〜中等度痙縮・ROM拡大前処理 | ★★☆ | ◎ | △(繰り返し要) | 随意運動が残存している患者・PNFのベースとして |
| ②PNF収縮弛緩法(CR) | 痙縮全般・ROM制限・筋柔軟性向上 | ★★★ | ◎ | ○ | 他動的ROM拡大が目標・ハムストリングス・腸腰筋など |
| ③静的ストレッチ | 軽〜重度痙縮・装具・ポジショニング | ★☆☆ | △ | ○(長時間保持で) | 夜間スプリント・臥位ポジショニング・能動収縮困難例 |
| ④腱圧迫法 | 局所的な高緊張・徒手前処理 | ★★★ | ○ | △ | 触診スキルが十分な場合・重度麻痺で随意収縮困難例 |
| ⑤低負荷持続収縮 | 重度麻痺・高齢者・疲労しやすい患者 | ★★☆ | △ | ○(継続で蓄積) | NMES併用・立位保持訓練との組み合わせ |
| ⑥関節モビライゼーション+ | 痙縮+関節可動域制限の合併 | ★★★ | ○ | ○ | 拘縮傾向・足関節・手関節の複合制限 |
🔑 技術選択の3ステップ
Step 1 ― 随意収縮の確認:患者が随意収縮を起こせるか? → できる:①②を優先。できない(重度麻痺):③④⑤を選択し、NMES でまず収縮を誘発。
Step 2 ― 目的の確認:ROM拡大が主目標 → ②CR法。筋緊張のリセットが主目標 → ①④。長時間の維持(夜間)→ ③。機能訓練の前処理 → ①②④を組み合わせて実施。
Step 3 ― 関節制限の有無:痙縮に加え関節制限あり → ⑥を先行させてから①②。関節制限なし → ①②だけで十分な場合が多い。
その他の神経疾患へのGTO・Ib抑制の応用
GTOとIb抑制の応用は脳卒中後の痙縮に限りません。様々な神経疾患・整形外科疾患においても同様の原理が適用できます。
🧠 脳性麻痺(CP)
痙直型CPでは脳卒中後と類似した上位運動ニューロン損傷パターンを示し、Ib抑制回路の機能低下が見られます。PNF・アイソメトリック収縮はCP児の痙縮管理に広く使用されていますが、成長期の筋骨格系の変化(筋の相対的短縮・骨変形)を考慮した慎重な負荷設定が必要です。ボツリヌス毒素投与後のIb促通介入は、成人脳卒中と同様に有効とされています(Booth et al. 2018)。
🩻 脊髄損傷(SCI)
不全損傷(AIS C/D)では残存する下行路の影響を受けながら、Ib回路が部分的に機能します。完全損傷(AIS A/B)では下行性制御が完全に遮断されるため、Ib介在ニューロンへの脳幹路・皮質路からの制御が失われ、GTOへの刺激に対する反応が健常者と大きく異なることがあります。不全SCIへの応用では能動収縮の誘導(FES・経皮的電気刺激との組み合わせ)が基本戦略です。
🔶 パーキンソン病(PD)
PDでは固縮(rigidity)が主な筋緊張異常です。固縮は痙縮とは異なり「歯車様・鉛管様抵抗」を示し、速度に依存しません。GTOのIb抑制は固縮の解消にも部分的に機能するとされており、PNF・アイソメトリック収縮は固縮の一時的緩和に活用できます。ただしPDの固縮は基底核回路の障害に起因するため、GTO介入単独での長期的な効果は限定的であり、運動療法(Lee Silverman Voice Treatment・LSVT BIG等)と組み合わせることが重要です。
🦴 整形外科疾患・スポーツ
筋スパズム(外傷・術後・腰痛など)にもGTOのIb抑制原理が応用されます。特にPNFパターンを用いたアクティブリリースは、筋スパズムを伴う腰痛・頸部痛・肩こりへの徒手療法として広く実施されています。スポーツ分野では、試合前のダイナミックウォームアップにPNF要素を取り入れることでGTOを事前活性化し、筋の柔軟性と反応速度を最適化する戦略が採用されています。
⚠️ 痙縮 vs 固縮 vs 拘縮 ― 鑑別なしに介入しない
痙縮(spasticity):速度依存性の抵抗増加。上位運動ニューロン損傷(脳卒中・SCI・CP)。Ia反射亢進とIb抑制低下が共に関与。GTO介入の主要適応。
固縮(rigidity):速度非依存性の持続的抵抗。基底核障害(PD等)。Ia反射は亢進しない。GTO介入は補助的効果にとどまる。
拘縮(contracture):関節・結合組織・筋の器質的な短縮。神経学的メカニズムとは独立した構造的変化。Ib抑制介入の効果は原則なし。モビライゼーション・スプリント・手術的治療が必要。
この3つを鑑別した上でGTO介入の適応を判断することは、不必要な介入・期待値のズレを防ぐうえで不可欠です。
患者・ご家族が自宅で実践できるセルフケア(自主練習)
専門家による介入と並行して、患者自身・ご家族が自宅で継続できる取り組みは回復の大きな土台となります。以下のセルフケア手技はGTOのIb抑制原理を活かした安全な自主練習として活用できます。
タオルを使ったセルフPNF(下腿痙縮向け)
椅子座位でのかかと上げ(低負荷持続収縮)
壁を使ったアイソメトリック肘伸展(上肢屈筋痙縮向け)
※自主練習は必ず担当療法士の指導のもとで開始してください。症状の変化・痛みが生じた場合はすぐに中止し、担当者に相談してください。
新人療法士が押さえるべき10のポイント
GTOとIb抑制を臨床で効果的に活用するための、実践的なポイントを整理します。
筋腱移行部の正確な触診スキルを身につける
「ストレッチよりも能動収縮を優先」の原則を覚える
収縮タイミングを見極める ― 安静時介入と機能的介入を区別する
GTOは「緩徐順応型」受容器である ― リズム刺激神話を正す
筋緊張が「短縮」位では効果が下がる場合がある
代償動作を予防する姿勢管理
複数の筋群への横断的応用を行う
過剰な反射性収縮(クローヌス)に注意
患者フィードバックをリアルタイムで活用する
継続的な実施と効果の定量的確認
臨床ケーススタディ ― GTOを軸にした介入設計
Ib抑制介入の主要エビデンスレベルと限界
GTO・Ib抑制を直接のメカニズムとして検証したRCTは現時点では少なく、多くの臨床エビデンスはPNF・アイソメトリック収縮・静的ストレッチの効果を検証したものです。主要な知見を整理します。
- PNF収縮弛緩法 vs 静的ストレッチ:Hindle et al.(2012)のレビューでは、PNFはROM改善・筋力向上において静的ストレッチと比較して優れた効果を示す。ただし長期的な効果の持続性については証拠が不十分
- アイソメトリック収縮後の痙縮軽減:複数の観察研究でアイソメトリック収縮直後のMAS低下・ROM改善が報告されているが、効果の持続時間は数時間〜1日程度のものが多い
- ボツリヌス毒素との組み合わせ:ボツリヌス投与後にPNF・集中リハビリを組み合わせた群で投与単独群より優れたADL改善が見られるという研究が複数報告されている(Picelli et al. 2012ほか)
- Houk(1967)の解釈における注意点:ネコの実験データであり、前根の選択的刺激という高度に人工的な条件での結果。生体内での複雑な神経筋相互作用を完全には再現していない。ヒト臨床への外挿は有望ではあるが、過度な一般化は避けるべき
📋 症例:山田さん(62歳・男性)左中大脳動脈梗塞 発症後3ヶ月・回復期リハビリ病棟
左中大脳動脈梗塞により右片麻痺(左中大脳動脈梗塞では対側=右の運動・感覚障害が生じる)。右下肢伸筋群(大腿四頭筋・腓腹筋)に中等度痙縮(MAS 2)があり、立脚期の膝過伸展・足関節底屈強制によって歩行が不安定。ボツリヌス毒素投与を2週前に実施。効果発現期(投与後2〜4週)に入り、積極的なGTO促通介入を計画。
| 評価項目 | 結果 | GTOへの関連解釈 |
|---|---|---|
| 折りたたみナイフ現象 | +(陽性):大腿四頭筋・腓腹筋で確認 | GTO主体のIb抑制回路が部分的に機能している可能性。介入適応あり |
| 大腿四頭筋 MAS | 2(他動的な全可動域での著明な抵抗増加) | Ib抑制が通常より高い閾値でのみ起動している状態 |
| 腓腹筋 MAS | 2(足関節背屈制限 0°まで) | ヒラメ筋・腓腹筋MTJへのGTO介入の適応 |
| 歩行分析 | 立脚後期のpush-off欠如・歩行速度低下 | Ib促通的切り替えの障害が示唆される |
介入プログラム(ボツリヌス投与後2〜6週の集中期):
腓腹筋・ヒラメ筋へのPNF収縮弛緩法(CR法)
仰臥位で足関節を背屈方向に他動的に誘導しながら、「足を下に押す(底屈方向に等尺性収縮)」を10秒保持 → 弛緩確認後すみやかに他動背屈でROMを拡大。これを3〜5セット。ボツリヌス後の「やわらかくなった期間」を活かしてROMを早期に確保します。
アキレス腱部の徒手腱圧迫 + 直後の能動背屈
腓腹筋・ヒラメ筋MTJ(アキレス腱移行部)に持続的な圧迫(5〜10秒)を加えてGTOを活性化 → 圧迫解除直後に「足首を上に引き上げて」と能動背屈を促す。GTOのIb抑制効果を能動運動の補助として活用します。
立脚期push-off訓練(GTO促通的機能の再学習)
平行棒内での立位練習:「かかとを上げながら蹴り出す動作」を繰り返し練習し、立脚後期のGTO促通的機能(CPG制御による伸筋促通)の再学習を目指します。この段階では「腓腹筋の活動を抑制する」のではなく「適切なタイミングで活性化する」ことが目的であり、Ib回路の文脈依存的な切り替えを促します。
介入後4週の評価:足関節背屈ROM +10°改善(0° → 10°)、MAS 2 → 1+へ改善。歩行速度 0.4 m/s → 0.62 m/s(機能的歩行分類:FAC 3 → 4)。折りたたみナイフ現象は引き続き陽性で、Ib回路の部分的機能が継続確認。
加齢・薬物療法・評価ツールの補足知識
🧓 GTOと加齢 ― 高齢者リハビリへの示唆
加齢はGTOを含む固有受容器全体の機能に影響を与えます。高齢者では、感覚神経線維の伝導速度低下・末梢受容器の感受性変化・中枢神経系の情報処理速度低下が複合的に起こります。これによりGTOからIb介在ニューロンへのシグナル伝達の「精度と速度」が低下し、筋張力の調節精度が落ちるとされています(Kararizou et al. 2005)。
臨床的示唆:高齢者へのGTO介入では、①収縮強度を若年者より低め(最大収縮の30〜50%)に設定する、②収縮保持時間を少し長めに(15秒程度)設定してGTOへの十分な張力刺激時間を確保する、③反復間の休憩を十分に取り疲労を防ぐ、といった調整が推奨されます。また転倒リスクを考慮し、立位での強負荷介入は安全な環境・監視下で行ってください。
💊 薬物療法(バクロフェン・ダントロレン)とIb抑制の相互作用
痙縮の薬物療法として広く使用されるバクロフェン(GABA-B受容体作動薬)は、脊髄後角〜中間帯レベルでの抑制性シナプス伝達を促進します。これはIb介在ニューロンを含む脊髄抑制回路全体の感度を高める効果があり、GTO介入との相乗効果が期待できます。一方、バクロフェンの過剰投与は筋力低下・倦怠感を引き起こし、GTO活性化に必要な能動収縮を困難にします。
ダントロレン(筋弛緩薬:筋小胞体からのCa²⁺放出阻害)は末梢の筋線維レベルで作用するため、GTO・Ib回路への直接的な作用は少ないですが、筋収縮力の低下により能動収縮によるGTO活性化が弱まる可能性があります。リハビリスタッフは患者が使用している薬剤の種類・投与量を把握し、介入効果の評価に活用してください。
📏 MAS(修正アッシュワース評価法)の限界と代替評価
本記事で痙縮評価として使用しているMAS(Modified Ashworth Scale)は臨床で最も広く普及している評価ツールですが、評価者間信頼性・妥当性に関する批判的検証があります(Bohannon & Smith 1987; Pandyan et al. 1999)。MASは痙縮の神経生理学的メカニズムを直接反映するものではなく、他動的な抵抗感の主観的評価であるため、検査速度・関節位置・評価者スキルによって変動します。
補完的な評価指標:①Tardieu Scale(速度依存性の検査:痙縮の神経生理学的特性をより正確に反映)、②関節可動域(ROM)測定(客観的な数値化が可能)、③歩行速度・Timed Up and Go Test(機能的な影響の評価)、④筋電図(EMG)・H反射(神経生理学的客観評価)を組み合わせることで、より信頼性の高い評価が可能です。
よくある質問(FAQ)
GTOと筋紡錘はどちらが先に活性化されますか?
また、GTOは緩徐順応型(slowly adapting)受容器であり、持続的な張力変化に対して安定して発火し続けます(速順応型のパチニ小体とは異なります)。この特性がPNF・アイソメトリック収縮・長時間の静的ストレッチを有効にする生理学的根拠です。リハビリ介入では「どちらの受容器を優先的に活性化させるか」を意識して手技を選択することが重要です。
折りたたみナイフ現象はなぜ起こり、どう評価に使えますか?
評価への活用:折りたたみナイフ現象が認められる患者では「Ib抑制回路が少なくとも部分的に機能している可能性がある」と解釈できます(GTO以外の要因も含む)。この所見はGTO介入の適応を支持するひとつの参考情報となります。重篤な痙縮で折りたたみナイフ現象が消失している場合は、脊髄抑制回路の高度な障害が示唆されます。
痙縮へのストレッチは効果がないのですか?
脳卒中後の患者でGTOの機能は正常に保たれていますか?
PNFのストレッチ法のうち「収縮弛緩(CR)」と「等尺性収縮後弛緩(HR)」のどちらを選ぶべきですか?
GTOのIb抑制は健常者のトレーニングにも応用できますか?
歩行訓練中にGTO介入を行う際の注意点は?
このため、歩行リハビリ中に「立脚後期の下腿筋緊張をIb抑制で緩めよう」とすることは、push-offを弱め歩行効率を低下させる可能性があります。GTO介入による筋緊張管理は原則として歩行練習の「前処理」として行い(ウォームアップ段階での痙縮緩和)、歩行訓練中は適切な筋活動を促通しながら機能的課題を遂行してください。ただし遊脚期の足関節底屈痙縮(内反尖足)に対しては、歩行中の前脛骨筋促通と腓腹筋Ib抑制を組み合わせることが有効な場合もあります。個別の歩行分析に基づいた判断が不可欠です。
GTOは筋疲労の感知にも関与していますか?
臨床的には、高強度アイソメトリック収縮を長時間繰り返すと筋疲労が生じてGTOへの刺激効率が低下します。Ib抑制介入は1セット10〜15秒程度の中強度収縮・休憩インターバルを設けた適切な設計で実施し、疲労によるパフォーマンス低下を防いでください。
Houk(1967)の研究はネコでの実験です。ヒトに応用できますか?
STROKE LABのGTO・痙縮管理アプローチ
脳卒中後に足首が突っ張って歩けなかったのですが、STROKE LABで「力を入れてから抜く」練習を繰り返したら、初めて足首がほぐれる感覚がわかりました。先生に「GTOが活性化されて筋緊張が下がっているんです」と説明してもらってから、自主トレでも意識できるようになりました。
60代男性・右片麻痺(脳梗塞発症後8ヶ月)
上肢の屈筋痙縮が強くて肘が伸びなかったのですが、PNFのアプローチで徐々に可動域が広がってきました。「なぜこの運動をするのか」をきちんと説明してくれるので、自主練習にも取り組めています。
70代女性・左片麻痺(脳出血発症後4ヶ月)
参考文献
- 1) Houk J. Responses of Golgi tendon organs to active contractions of the soleus muscle of the cat. J Neurophysiol. 1967;30(3):466-481. PubMed 6037588 【能動収縮vs他動伸張のGTO反応比較:本記事の中心的論文・サイレント期の考察を含む】
- 2) Jami L. Golgi tendon organs in mammalian skeletal muscle: functional properties and central actions. Physiol Rev. 1992;72(3):623-666. 【GTOの緩徐順応型受容器特性・3〜25本の筋線維直列接続・Ib回路の包括的レビュー】
- 3) Pearson KG, Misiaszek JE, Fouad K. Enhancement and resetting of locomotor activity by muscle afferents. Ann NY Acad Sci. 1998;860:203-215. 【歩行周期でのIb回路の文脈依存的切り替え(脊髄CPGによる促通的機能)】
- 4) Burke D, Gillies JD, Lance JW. Hamstrings stretch reflex in human spasticity. J Neurol Neurosurg Psychiatry. 1971;34(2):231-235. 【折りたたみナイフ現象の神経生理学的機序・Ib抑制とグループIII/IV線維の関与】
- 5) Yanagawa S, Shindo M, Yanagisawa N. Ib inhibition in spastic patients. Electroencephalogr Clin Neurophysiol. 1990;77(4):347-352. 【痙縮患者でのIb抑制量低下・H反射プロトコルによる定量評価】
- 6) Pearson KG, Gordon J. Spinal reflexes. In: Kandel ER, Schwartz JH, Jessell TM, et al., eds. Principles of Neural Science. 5th ed. McGraw-Hill; 2013. 【Ib介在ニューロンの脊髄中間帯〜後角深部への終止・CPGは脊髄腰髄〜仙髄レベルに推定・回路全体像】
- 7) Shumway-Cook A, Woollacott MH. Motor Control: Translating Research into Clinical Practice. 5th ed. Lippincott Williams & Wilkins; 2017.
- 8) Hindle KB, Whitcomb TJ, Briggs WO, Hong J. Proprioceptive neuromuscular facilitation (PNF): its mechanisms and effects on range of motion and muscular function. J Hum Kinet. 2012;31:105-113. 【PNF収縮弛緩法・後収縮弛緩(post-contraction depression)のメカニズム】
- 9) Sharman MJ, Cresswell AG, Riek S. Proprioceptive neuromuscular facilitation stretching: mechanisms and clinical implications. Sports Med. 2006;36(11):929-939. 【PNF vs 静的ストレッチのROM改善効果比較・システマティックレビュー】
- 10) Kandel ER, Schwartz JH, Jessell TM, et al. Principles of Neural Science. 6th ed. McGraw-Hill; 2021. 【脊髄反射回路・γ運動ニューロン非支配の確認・GTO/筋紡錘比較・MLR vs CPG】
- 11) Johnels BI. On the pathophysiology of gait in Parkinson’s disease. Acta Neurol Scand. 1982;66(1):1-23. 【パーキンソン病固縮のIb回路関与・脊髄抑制系の変容】
- 12) Lopes de Almeida EG, et al. The effects of functional electrical stimulation cycling exercise on spasticity in people with spinal cord injuries. Spinal Cord. 2013;51(5):344-354. 【FES自転車によるGTO活性化→脊髄Ib抑制→痙縮緩和のメカニズム】
- 13) Lieber RL. Skeletal Muscle Structure, Function, and Plasticity. 3rd ed. Lippincott Williams & Wilkins; 2010.
- 14) Bohannon RW, Smith MB. Interrater reliability of a modified Ashworth scale of muscle spasticity. Phys Ther. 1987;67(2):206-207. 【MAS(修正アッシュワース評価法)の信頼性・妥当性の限界に関する原著】
- 15) Pandyan AD, et al. A review of the properties and limitations of the Ashworth and modified Ashworth Scales as measures of spasticity. Clin Rehabil. 1999;13(5):373-383. 【MAS評価の妥当性・速度依存性の課題とTardieu Scaleとの比較】
- 16) Kararizou E, et al. Morphological and morphometrical study of the human muscle spindle. J Neurol Sci. 2005;229-230:305-310. 【加齢による固有受容器の形態変化に関する参考文献(高齢者リハビリへの示唆)】
GTOとIb抑制の知識を、
あなたの患者の回復に活かしましょう。
痙縮・筋緊張の問題に対し、神経生理学的根拠に基づいた介入を。
STROKE LABで専門家によるリハビリプランをご相談ください。

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)











