【2026年版】尾状核と被殻の違いとは?運動制御と学習への役割を徹底解説!CT-MRIまで
大脳基底核の中核を担う尾状核(Caudate Nucleus)は、運動・認知・学習・報酬処理を統合する脳深部の重要構造です。本記事では、解剖学的位置と3部構成、血液供給、4つの皮質線条体ループ、ハンチントン病・脳卒中後CRPSとの関連、画像読解のポイント、そしてリハビリテーションの実践的なアプローチまでを徹底解説します。「なぜ尾状核損傷で認知障害が起きる?」「運動と認知をつなぐ機能ループとは?」「トレッドミルがなぜ有効か?」――これらの疑問にすべて答えます。
尾状核の解剖・機能・リハビリへの応用を動画で確認できます。
尾状核(Caudate Nucleus)は大脳基底核の一部(線条体の構成要素)で、側脳室に沿って頭部・体部・尾部の3部からなるC字型の構造を持ちます。前大脳動脈(ホイブナー反回動脈)と中大脳動脈(レンズ核線条体動脈)の2系統から血流を受け、動機付け・遂行機能・視覚処理・運動計画の4つの皮質線条体ループを介して学習・記憶・報酬に基づく行動選択を担います。ハンチントン病の主要変性部位であり、脳卒中後CRPSとの関連も報告されています。リハビリテーションではトレッドミル歩行再学習・認知課題・ポジティブフィードバックの3本柱が科学的根拠を持ちます。
- 正式名称:尾状核(Caudate Nucleus)/大脳基底核・線条体の一部
- 形状・位置:C字型。側脳室に沿って大脳半球深部に位置。3部(頭部・体部・尾部)に分類
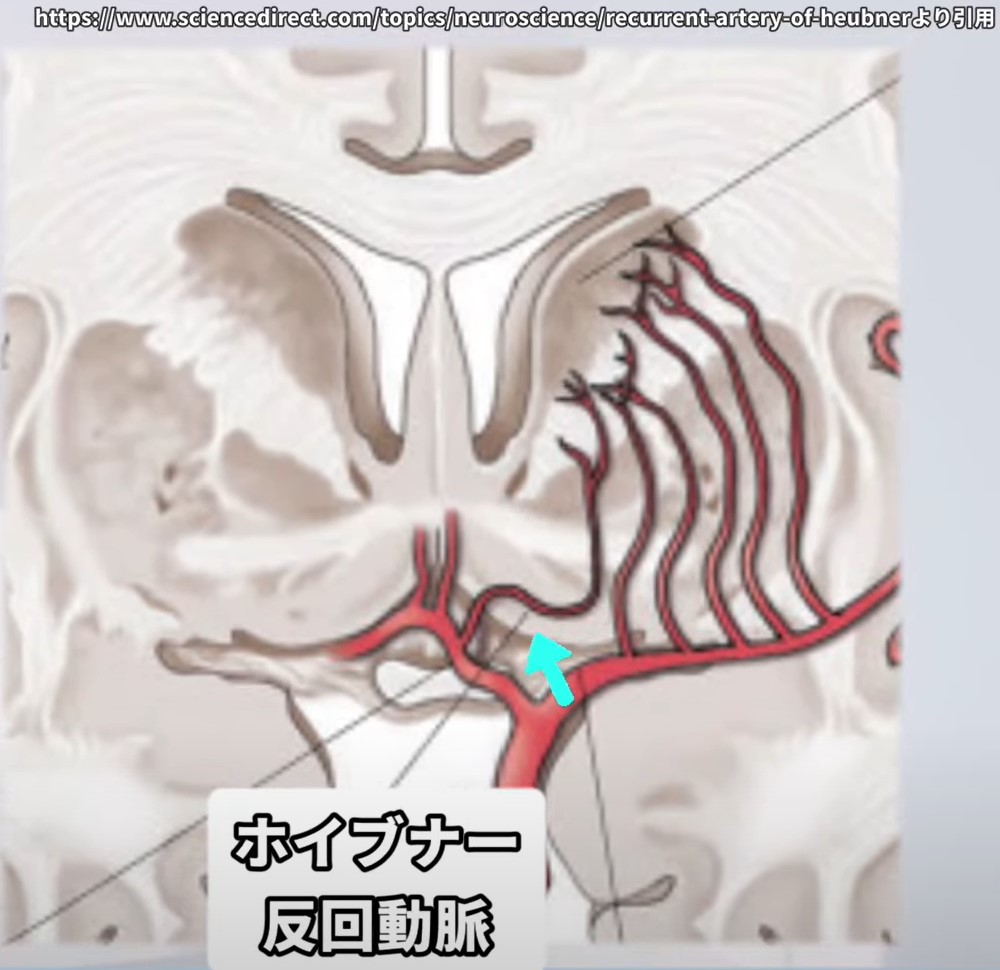
- 血液供給①:頭部 → 前大脳動脈(ACA)からのホイブナー反回動脈(Heubner’s recurrent artery)
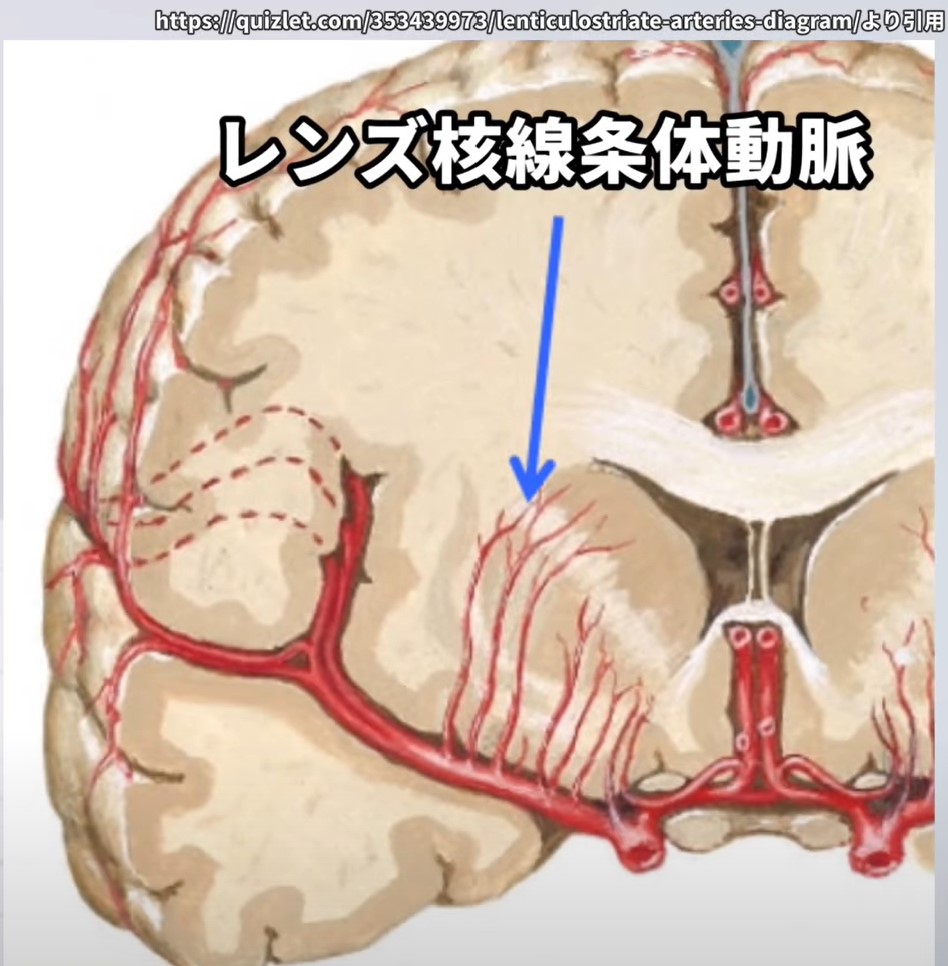
- 血液供給②:体部・尾部 → 中大脳動脈(MCA)のレンズ核線条体動脈(Lenticulostriate arteries)
- 4つの皮質線条体ループ:①動機付け(大脳辺縁系・腹側線条体)②遂行(DLPFC・尾状核頭部)③視覚(下側頭葉・尾状核体部/尾部)④運動(補足運動野・被殻)
- 主要機能:手続き記憶・遂行機能・カテゴリー学習・報酬に基づく行動選択・運動計画の補助
- 尾状核 vs 被殻:尾状核 → 認知・学習・遂行機能 / 被殻 → 運動プロセス・動作調節(機能的に明確に異なる)
- 代表的病態:ハンチントン病(尾状核の神経変性が主病巣)・脳卒中後CRPS(尾状核頭部・被殻・放線冠白質複合体との関連が VLSM で実証)
- リハビリの意義:トレッドミル歩行で歩行リズム再学習・認知課題で遂行機能賦活・ポジティブフィードバックで報酬ループ活用
- エビデンス:慢性脳卒中後でも発症6ヶ月以降にリハビリで機能改善(Hatem et al. 2016)・習慣形成介入が身体活動習慣強度を向上(Haomin et al. 2023)
尾状核とは ― 解剖・部位・血液供給
尾状核は大脳基底核を構成する核群の一つで、被殻(Putamen)とともに線条体(Striatum)を形成します。大脳半球深部に位置し、側脳室に沿ってC字型に伸びる独特の形状が特徴です。全長にわたって3つの解剖学的部位に分けられます。
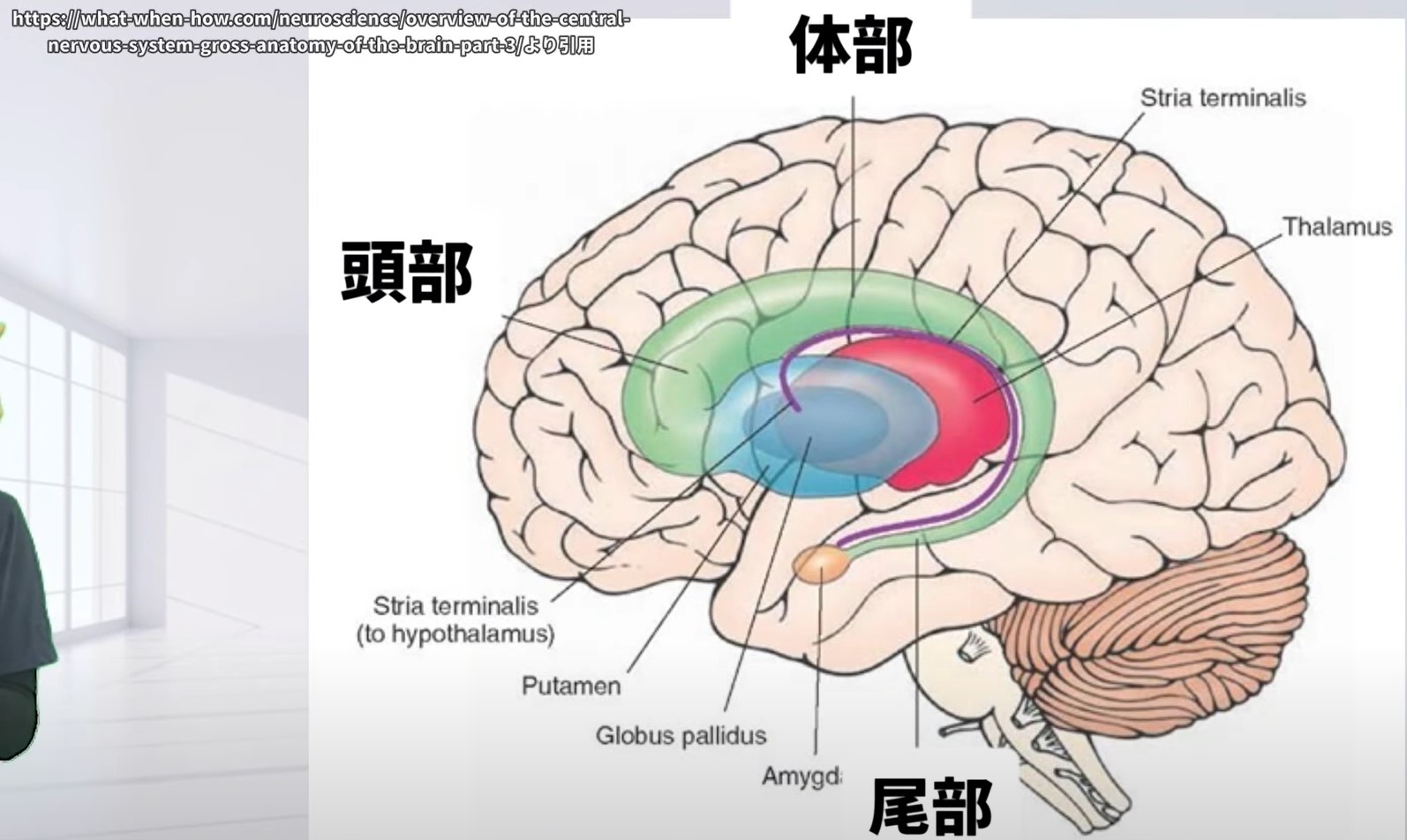
側脳室前角レベル
最も太く丸みを帯びる
側脳室体部の上壁
頭部から細くなり帯状
側脳室下角・側頭葉内
非常に細く識別が難しい
血液供給 ― 2つの動脈系が頭部と体部・尾部を分担
| 部位 | 供給動脈 | 血管名 | 臨床的意義 |
|---|---|---|---|
| 尾状核 頭部 | 前大脳動脈(ACA) | ホイブナー反回動脈 (Heubner’s recurrent artery) |
ACA梗塞では頭部への血流障害 → 遂行機能・学習障害 |
| 尾状核 体部・尾部 | 中大脳動脈(MCA) | レンズ核線条体動脈 (Lenticulostriate arteries) |
MCA梗塞・ラクナ梗塞で体部・尾部への障害 → 運動・視覚処理への影響 |
中大脳動脈(体部・尾部)
前大脳動脈・ホイブナー動脈(頭部)
⚠️ 血液供給の違いが臨床症状の違いを生む
尾状核の頭部はACA(前大脳動脈)、体部・尾部はMCA(中大脳動脈)という異なる動脈系が支配しているため、閉塞血管によって生じる症状が異なります。
ACA梗塞(頭部障害):遂行機能低下・意欲低下・学習障害が前景に立ちます。ホイブナー反回動脈は内包前脚にも血流を供給するため、軽度の対側下肢優位の運動障害を合併することがあります。
MCA穿通枝(レンズ核線条体動脈)閉塞(体部・尾部障害):尾状核の視覚ループ・運動への補助的関与が障害されます。ただし、MCA主幹部や皮質枝梗塞では運動麻痺・感覚障害・失語・半側空間無視がより前景に立つため、尾状核への影響は臨床像の一部として解釈する必要があります。急性期評価では画像所見と神経症状を照合して、どの部位のどのループが障害されているかを推定することが重要です。
皮質線条体ループ ― 4つの神経ネットワーク
尾状核を含む線条体は、大脳皮質のさまざまな領域と閉鎖回路(皮質線条体ループ)を形成し、それぞれ特定の認知・行動機能を担っています。Seger(2008)が提唱した4ループモデルは、線条体の機能分化を理解する基本的な枠組みです。
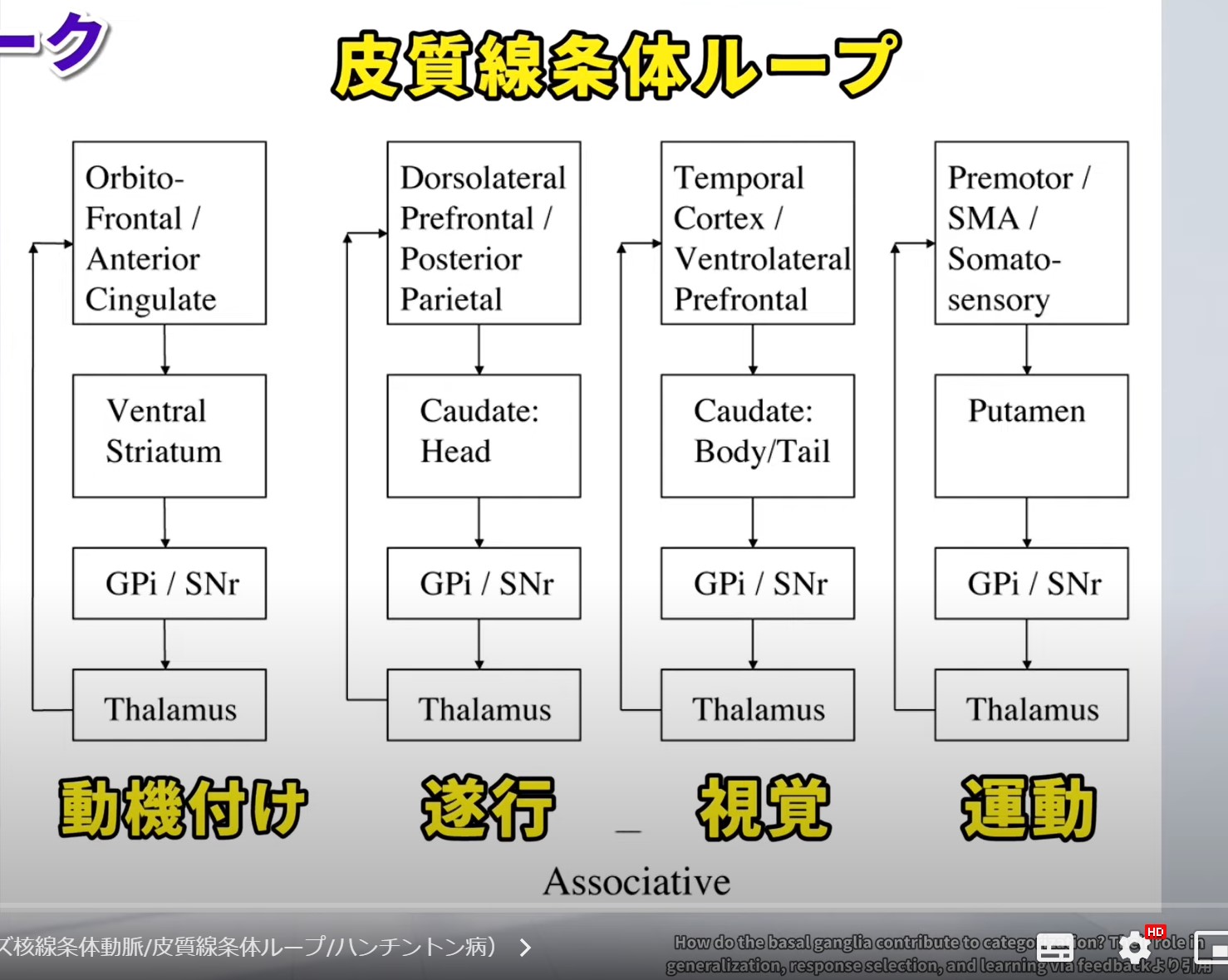
How do the basal ganglia contribute to categorization? — Seger (2008)
🔑 4つのループを理解するための「登山」のたとえ
本記事では4つのループを、登山者が山で木の実を見つけ、採集し、食べるかどうかを決めるシナリオで説明します。それぞれのループが「いつ・なぜ・何をするか」に応じて独立しながらも連携して働く様子が直感的に理解できます。
動機付け皮質線条体ループ(Motivational Corticostriatal Loop)
このループは報酬に関連する情報の処理と動機付けを担います。期待される報酬の価値を評価し、行動を起こすかどうかの動機づけを行います。「やる気」「意欲」「目標に向かう力」の神経基盤です。


遂行皮質線条体ループ(Executive Corticostriatal Loop)
高次の実行機能(計画・意思決定・戦略策定・柔軟な適応)を支えます。環境からのフィードバックを戦略に組み込む能力や、新しい状況に対応する認知的柔軟性を担います。


視覚皮質線条体ループ(Visual Corticostriatal Loop)
視覚情報のカテゴリー化と分類学習を担います。対象物を過去の経験と照合して「何か」を識別する視覚認知の基盤です。物体認識・顔認識・空間認知の一部を支えます。


運動皮質線条体ループ(Motor Corticostriatal Loop)
行動の選択と運動計画に重要な役割を果たします。「どの動作をいつ始め、いつ終えるか」を調整し、スムーズで協調的な動作を実現します。尾状核よりも被殻が主体的な役割を担うループです。


大脳基底核の回路 ― 直接路・間接路とドーパミンの役割
皮質線条体ループを正確に理解するには、その内部回路(直接路・間接路)とドーパミンシグナルの仕組みを押さえることが不可欠です。ハンチントン病・パーキンソン病・依存症・うつ病・OCDなど多くの疾患がこの回路の障害として説明できます。
🔬 大脳基底核の基本回路:3つの構成要素
①入力:大脳皮質・視床から線条体(尾状核・被殻)へ / ②中継・出力:淡蒼球(内節・外節)・黒質網様部 → 視床 / ③フィードバック:視床から皮質へ戻り、ループを完結させる。このループに黒質緻密部からのドーパミン入力が「ゲート(gate)」として作用します。
| 経路 | 走行 | 受容体 | 作用 | 関連する行動 |
|---|---|---|---|---|
| 直接路(Direct Pathway)― 運動促進系 | ||||
| 直接路 | 線条体(D1受容体)→ 淡蒼球内節/黒質網様部(抑制)→ 視床(脱抑制)→ 皮質活性化 | D1受容体(ドーパミンで興奮) | 視床の抑制を解除 → 皮質活動を促進 | 目標に向かった動作の開始・選択 |
| 間接路(Indirect Pathway)― 運動抑制系 | ||||
| 間接路 | 線条体(D2受容体)→ 淡蒼球外節(抑制)→ 視床下核(脱抑制)→ 淡蒼球内節(興奮)→ 視床(抑制増強)→ 皮質抑制 | D2受容体(ドーパミンで抑制) | 視床への抑制を増強 → 皮質活動を抑制 | 不要な動作・競合する動作プログラムの抑制 |
ドーパミンは「直接路を促進・間接路を抑制」して動作を選択的に実行させる
黒質緻密部(SNc)から線条体へのドーパミン投射は、D1受容体(直接路)を興奮させる一方でD2受容体(間接路)を抑制します。結果として、目標とする動作プログラムをONにし、競合する他の動作プログラムをOFFにする「フォーカス機能」を果たします。この機能が障害されると:
・ドーパミン過剰(ハンチントン初期・統合失調症様)→ 直接路過活動・間接路抑制 → 不要な動作が抑制されず舞踏運動・不随意運動が出現
・ドーパミン低下(パーキンソン病)→ 直接路抑制・間接路過活動 → 動作の開始困難・すくみ足・寡動
| 疾患・状態 | ドーパミン系の変化 | 直接路/間接路バランス | 主な症状 |
|---|---|---|---|
| ハンチントン病(初期) | SNc→線条体は比較的保たれる。間接路D2ニューロンが先に変性 | 間接路↓↓(抑制不足) | 舞踏運動・不随意運動(コレア) |
| ハンチントン病(進行期) | 直接路D1ニューロンも変性 | 直接路↓・間接路↓(両方障害) | 筋硬直・運動緩慢(パーキンソン様) |
| パーキンソン病 | 黒質緻密部変性 → ドーパミン低下 | 直接路↓・間接路↑↑ | 寡動・振戦・固縮・すくみ足 |
| OCD(強迫性障害) | 尾状核の代謝過活動(PETで確認) | 直接路過活動 | 強迫行為の抑制不全・反復行動 |
| 依存症(薬物・行動嗜癖) | 腹側線条体のドーパミン過剰放出・受容体ダウンレギュレーション | 報酬ループの過活動 → 慢性鈍化 | 衝動抑制困難・強迫的薬物探索 |
専門家向け:ハイパー直接路(Hyperdirect Pathway)とSTN の役割
直接路・間接路に加え、皮質から視床下核(STN)を介して淡蒼球内節に直接到達するハイパー直接路(Hyperdirect Pathway)が近年注目されています。このルートは直接路・間接路よりも伝達が速く、「緊急停止ブレーキ」として機能します。
例えば、動作を開始しようとした瞬間に「やめなければならない状況」が生じた際(Stop-signal task)、ハイパー直接路が即座に動作を中止させる役割を担います。STNへのDBS(深部脳刺激療法)がパーキンソン病の治療として確立しているのも、この回路への介入効果によるものです。
リハビリの文脈では、「動作の抑制制御の障害(impulsivity・perseveration)」がハイパー直接路の機能不全として説明できる場合があります。衝動的に不適切な動作を繰り返す・課題を変えようとしても以前の動作パターンに戻ってしまう(perseveration)などが臨床的指標となります。
尾状核と精神疾患 ― OCD・うつ病・ADHDとの関連
🔬 なぜリハビリ専門家が精神疾患と尾状核の関係を知るべきか
脳卒中・外傷後の患者では、神経学的後遺症だけでなく、うつ病・意欲障害・強迫的行動・注意障害といった精神症状が高頻度に合併します。これらは単なる「心の問題」ではなく、尾状核を含む大脳基底核の神経回路障害として理解できます。適切な介入と精神科・心療内科との連携判断に役立てましょう。
🔁 強迫性障害(OCD)
PET・fMRI研究で尾状核の代謝過活動が一貫して確認されています(Saxena & Rauch 2002)。尾状核の遂行ループ過活動により「やめたくてもやめられない」強迫行為が生じます。
脳卒中後に強迫様行動(同じ動作を繰り返す・確認行動)が現れた場合、尾状核病変の可能性を念頭に置き、SSRIや認知行動療法の専門家との連携を検討します。
😔 うつ病・意欲障害(Apathy)
うつ病では腹側線条体(動機付けループ)のドーパミン機能低下が関与します。脳卒中後のアパシー(意欲障害)は前頭葉-線条体回路の遮断として生じ、単純な「怠け」ではありません。
リハビリへの参加意欲低下・目標設定の困難さがアパシーの症状として現れます。Apathy Scaleでの評価と、必要に応じてドーパミン系薬剤の検討が推奨されます。
⚡ ADHD・注意障害
ADHDでは尾状核・前頭前野の発達的遅延および機能低下が報告されています。脳卒中後の注意障害も同様に、尾状核を介する前頭前野との接続障害として理解できます。
課題持続困難・衝動抑制困難・注意切り替えの問題が観察されます。環境調整(刺激の少ない環境・短時間の集中課題)と外部補助(スケジュール表・リマインダー)が有効です。
⚠️ 「やる気がない」をアパシーと誤解しないために
脳卒中後のアパシー(意欲障害)はうつ病と異なります。アパシーは「悲しい・辛い」という情動的苦痛を伴わない意欲・自発性の低下が主症状で、尾状核を含む前頭葉-線条体回路の障害が直接の原因です。一方、うつ病は情動的苦痛(悲しみ・絶望感)が中核症状で、治療アプローチも異なります。
Apathy Scale・NPI(Neuropsychiatric Inventory)を用いた評価を行い、アパシーであれば「内発的動機よりも外部からの構造化(schedule・goal-setting)」が有効で、うつ病には適切な薬物療法との組み合わせが必要です。
尾状核梗塞の症候論 ― 独立した臨床症候群として
尾状核梗塞(Caudate Infarction)― 独自の神経心理学的症候群
尾状核梗塞は全脳卒中の約2〜3%を占める比較的まれな病型ですが、独自の神経心理学的症候群を形成します。運動麻痺を伴わないため、急性期には「小さな梗塞」として見逃されることがあります。しかし遂行機能・意欲・学習への影響は重大であり、回復期リハビリの予後予測にも重要です。
| 症状カテゴリー | 具体的な症状・徴候 | 対応する障害ループ | リハビリでの注意点 |
|---|---|---|---|
| 神経心理学的症状(尾状核梗塞の主体) | |||
| 意欲・自発性の低下 | アパシー・自発語減少・反応の遅延・無気力 | 動機付けループ(腹側線条体) | 外部からの構造化・目標設定の明確化 |
| 遂行機能障害 | 計画立案困難・perseveration(同じ行動の繰り返し)・セットシフト困難 | 遂行ループ(尾状核頭部) | 課題を小ステップに分解・フィードバックを即時提供 |
| 記憶障害(軽度) | 作業記憶の低下・新しい手順の習得遅延 | 遂行・視覚ループ | 視覚的補助・繰り返し練習・習慣化 |
| 注意障害 | 持続的注意の低下・二重課題での成績低下 | 遂行ループ(前頭-線条体接続) | 単一課題から開始・環境の刺激を最小化 |
| 精神症状(尾状核梗塞で合併しうる症状) | |||
| 情動障害 | 過度の興奮・易怒性・情動的不安定 | 動機付けループの脱抑制 | 一定のルーティンを維持・刺激の管理 |
| 強迫様行動 | 特定行動の繰り返し・変化への強い抵抗 | 尾状核→OFC回路の損傷 | SSRIの使用を精神科と検討 |
| 運動症状(軽度・合併する場合) | |||
| 構音障害・発話変化 | 発話速度の低下・韻律の障害(まれ) | 運動ループへの波及 | ST介入・補完的コミュニケーション手段 |
| 対側軽度麻痺 | ACA領域が広がった場合に内包前脚も障害されると合併 | 内包前脚の巻き込み | 通常の脳卒中リハビリに準じる |
💡 尾状核梗塞を見逃さないための臨床サイン
「CT・MRIで小さな梗塞があるが麻痺がない → 経過観察でよい」と判断されることがあります。しかし尾状核梗塞の神経心理学的症状(アパシー・遂行機能障害)は退院後のADL・就労・社会復帰に重大な影響を与えます。急性期から神経心理士(または臨床心理士)・OT・STが連携して評価を行い、「軽微な梗塞でも認知・行動面への丁寧な評価が必要」という意識を持つことが重要です。
特に以下のサインがある場合は尾状核を含む前頭-線条体回路の評価を検討してください:①リハビリへの参加意欲が著しく低い(アパシーの可能性)②同じ誤りを何度指摘されても繰り返す(perseverationの可能性)③以前習得した動作を突然忘れる・崩れる(手続き記憶障害の可能性)
病態像 ― ハンチントン病・脳卒中後CRPS
ハンチントン病 ― 尾状核が主病巣となる神経変性疾患
ハンチントン病(Huntington’s Disease)― 尾状核の進行性変性
ハンチントン病はHTT遺伝子のCAGリピート伸長による常染色体優性遺伝の神経変性疾患です。尾状核の神経細胞(特にGABA性中型有棘ニューロン)が選択的に変性・脱落することで、舞踏運動・認知障害・精神症状の三徴が生じます。MRI上では尾状核の萎縮による側脳室前頭角の外方拡大(caudate indentation消失)が特徴的所見で、正常では側脳室前角内壁に尾状核頭部が内方に突出する「caudate impression」が失われます。尾状核の運動制御・認知処理・報酬系ループがすべて障害されるため、複合的な症状が生じます。

| 症状カテゴリー | 主な症状 | 関連する尾状核ループ |
|---|---|---|
| 不随意運動 | 舞踏運動(コレア)・バリスム・アテトーゼ | 運動皮質線条体ループ |
| 認知障害 | 遂行機能低下・注意障害・記憶障害 | 遂行皮質線条体ループ |
| 精神症状 | 抑うつ・意欲低下・易怒性・強迫症状 | 動機付け皮質線条体ループ |
| 言語・コミュニケーション | 構音障害・発語困難 | 運動ループ(口腔顔面) |
脳卒中後CRPS ― 尾状核頭部損傷との関連(VLSM研究)
脳卒中後CRPS(複合性局所疼痛症候群)と尾状核・被殻損傷
Lee ら(2021)は、虚血性脳卒中患者145名(うちCRPS 35名・対照110名)を対象にボクセルベース病変症状マッピング(VLSM)を実施。その結果、尾状核頭部・被殻・放線冠の白質複合体への病変が脳卒中後CRPS発症と有意に関連していることが示されました。これは尾状核が疼痛の認知処理においても重要な役割を担うことを示す直接的エビデンスです。
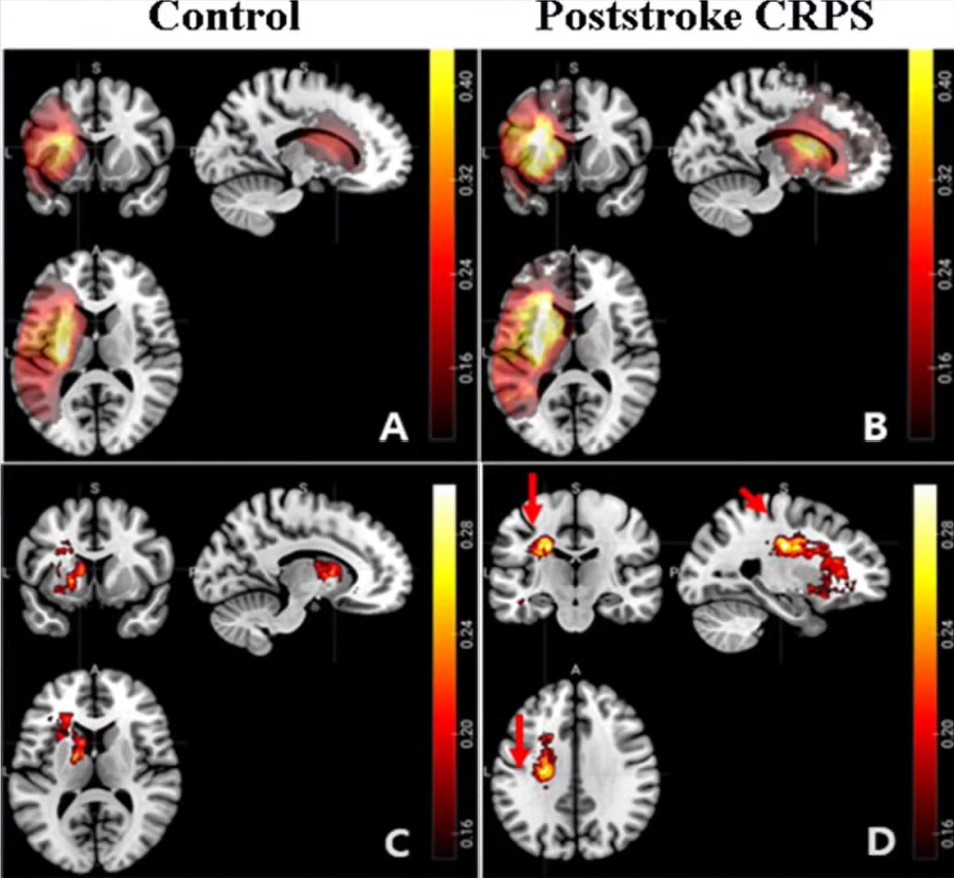
⚠️ 脳卒中後CRPSの臨床的含意
尾状核頭部・被殻に病変を持つ脳卒中患者では、CRPS発症リスクが高い可能性があります。患側上肢の疼痛・浮腫・皮膚色調変化・骨萎縮の早期徴候に注意し、肩手症候群スクリーニング・CRPS診断基準(Budapest Criteria)での評価を早期から実施することを推奨します。リハビリでは患側上肢への過度な負荷を避けつつ、適切な運動療法と鏡療法(Mirror Therapy)を組み合わせることが重要です。
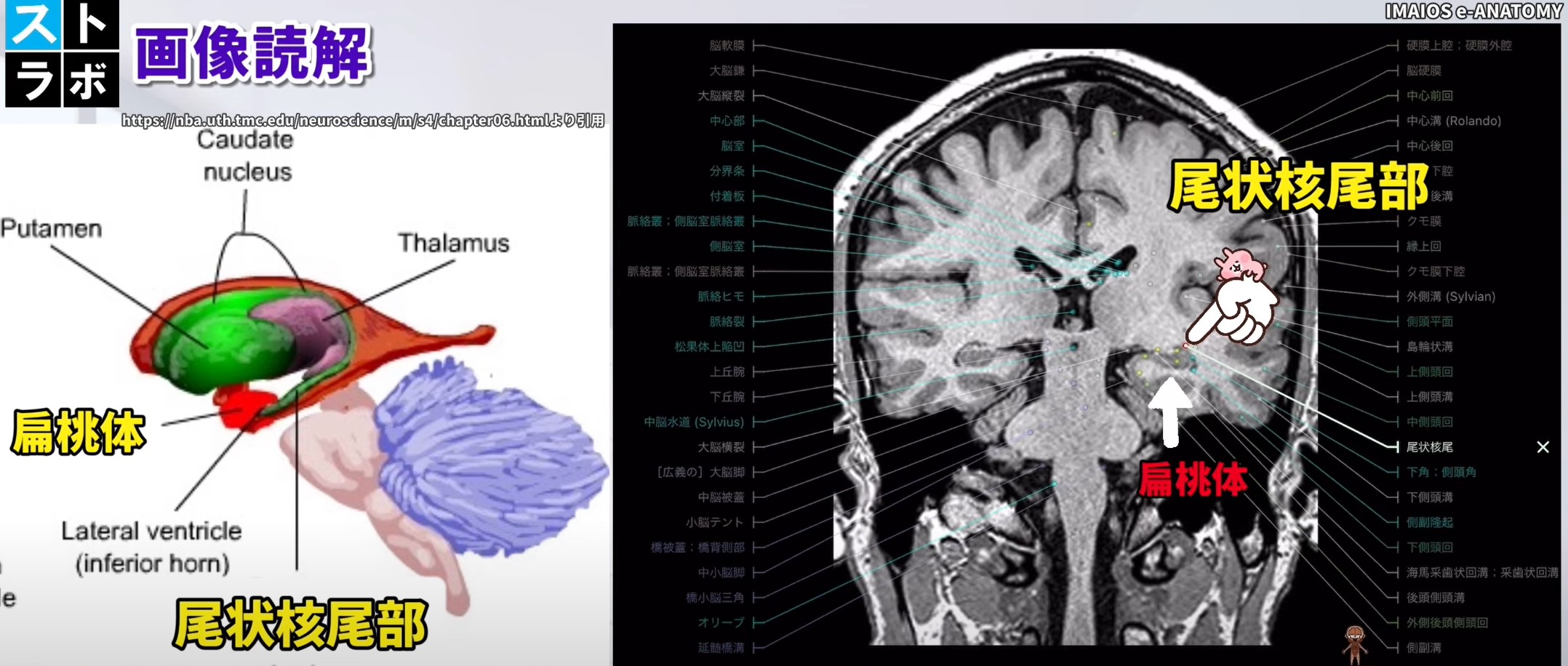
画像読解のポイント ― 頭部・体部・尾部のMRI/CT読影
💡 尾状核の全体的な画像特徴
尾状核は大脳基底核の一部で脳の深部に位置し、側脳室に沿ってC字型を描きます。MRI T1強調画像で等信号、T2強調画像でやや高信号として描出されます。これは画像上での識別における最も重要な特徴です。CT では灰白質として白質より高吸収域を呈し、石灰化(生理的)が見られることもあります。
尾状核 頭部(Caudate Head)― 側脳室前角レベル
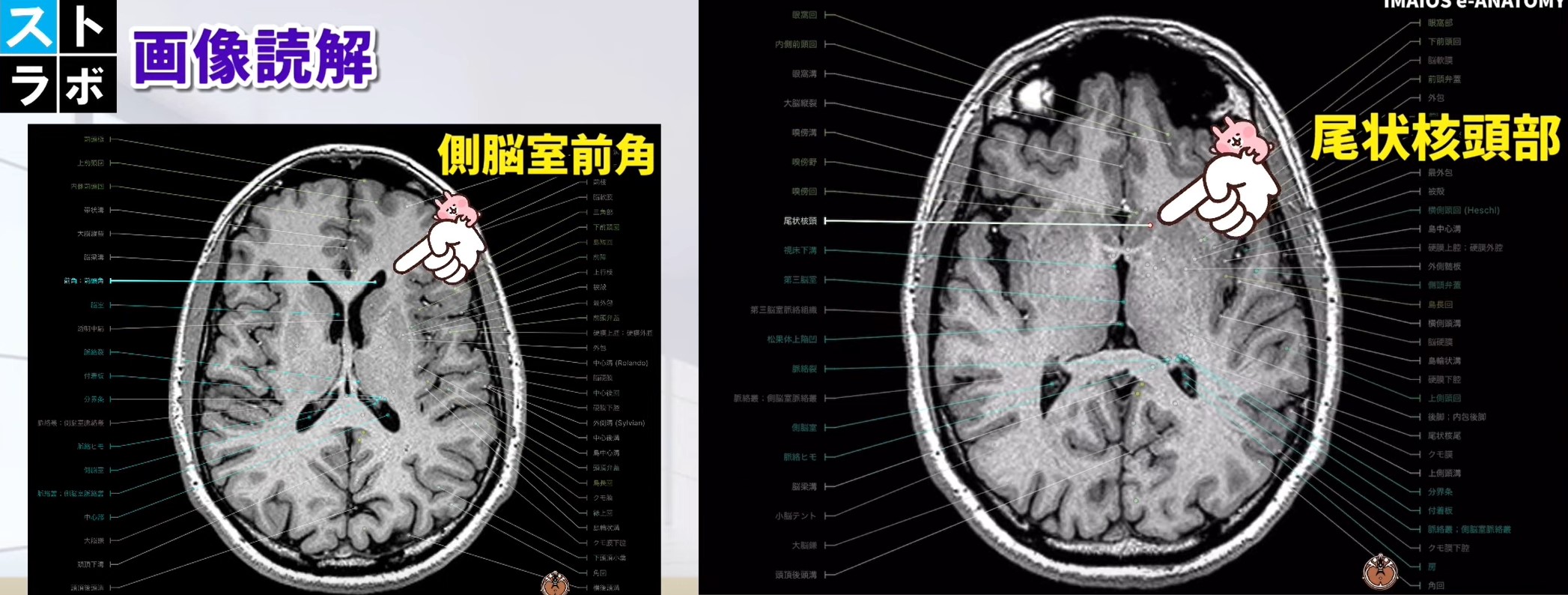
尾状核 体部(Caudate Body)― 側脳室体部レベル
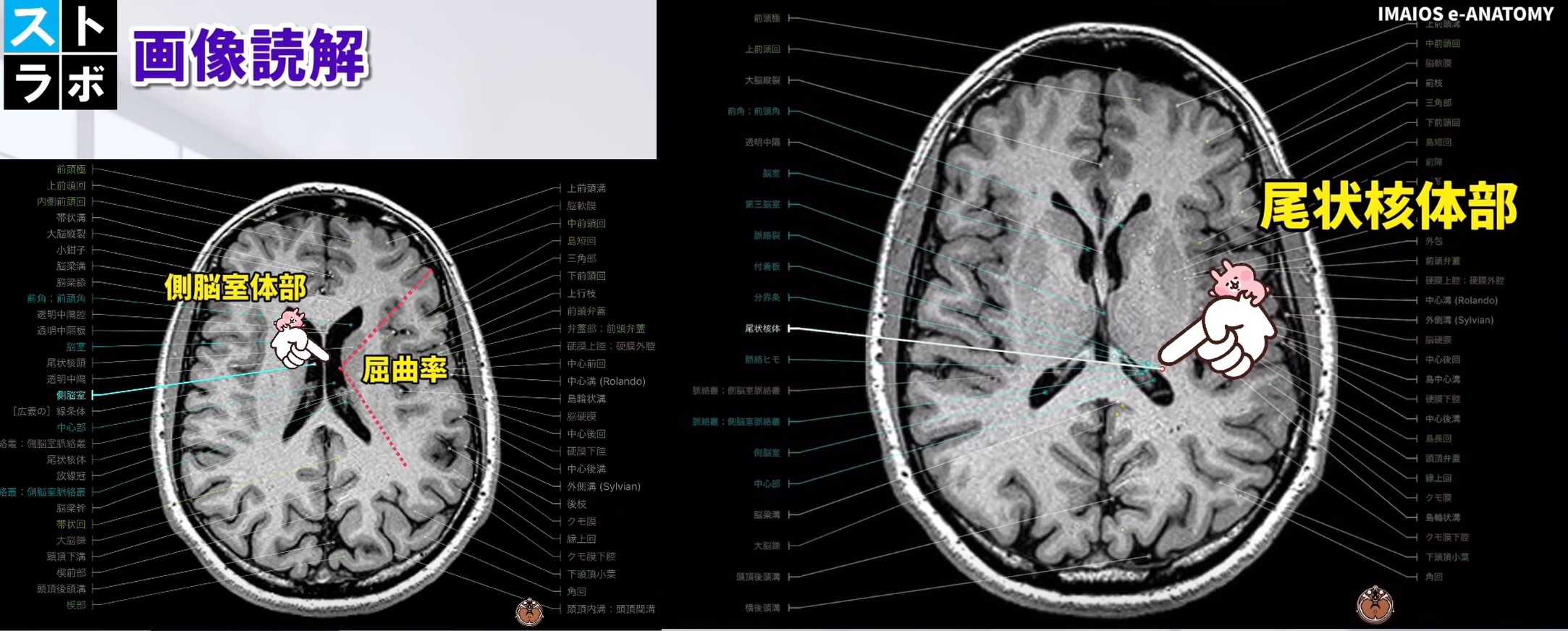
尾状核 尾部(Caudate Tail)― 側頭葉内
臨床観察と介入ヒント ― 4つの機能別アプローチ
🔑 尾状核損傷の臨床観察の基本姿勢
尾状核はその解剖学的接続から、①運動制御 ②認知処理 ③学習と記憶 ④報酬に基づく意思決定の4つの機能領域に影響します。それぞれについて観察ポイントと介入ヒントを示します。単一の機能への着目ではなく、4領域を総合的に評価することで、より精度の高い介入計画が立案できます。
運動制御(Motor Control)― 歩行リズム・協調・巧緻動作
📌 運動制御における尾状核と被殻の役割分担を整理する
純粋な運動の実行(速さ・力・タイミング)は主に被殻(Putamen)の運動ループが担います。尾状核の運動への関与は「認知的側面を持つ運動計画」つまり①どの動作プログラムを選ぶか②習慣的でない新しい動作をどう学習するか③目標達成のために運動を修正するかという側面に大きく関与します。そのため尾状核損傷では「麻痺はないが動き方がおかしい」「新しい動作が覚えられない」「状況に合わせた動き方の切り替えが難しい」という形で現れることが特徴です。

☑ 観察のポイント
- 歩行障害は?:歩行中の足上げタイミング・地面との抵抗・リズムの乱れ・バランス障害を観察。尾状核損傷では歩行リズムや協調性の乱れが生じることがある
- 細かい運動は可能?:文字を書く・調理器具を使う・ボタンを留めるなどの巧緻動作への影響を確認
- 表情と発話の障害は?:顔面筋の硬直・発声の不明瞭さ・表情の乏しさを観察
💡 臨床介入ヒント
① トレッドミルトレーニング:ハーネスを使用した安全な歩行動作の再学習。尾状核が管理するリズミカルで協調的な動作の再教育に有効。歩行速度を段階的に増加させることで負荷を調整する。
参考:Feasibility of challenging treadmill speed-dependent gait and perturbation-induced balance training in chronic stroke patients (Fü 2023)
② ガイド付き歩行(段階的課題付加):直線→曲がり角→凹凸路面→障害物回避→階段の順に複雑性を増やした歩行練習。環境変化への適応を促す。
参考:Treadmill training improves physical and metabolic health in association with declines in oxidative stress in stroke (Monica 2022)

認知処理(Cognitive Processing)― 注意・記憶・問題解決

☑ 観察のポイント
- 記憶処理の機能は?:指示や医療チーム名・日常作業の手順を思い出す能力。日常の手順の想起困難が見られることがある
- 問題解決は?:車椅子操作・障害物回避など新しい課題への対処能力の評価
- 変化への対応は?:新しい要素(変更されたスケジュール・新しい部屋・新しい担当者)への適応速度
💡 臨床介入ヒント
① 徐々に変化を与える:新しい習慣(歩行訓練の距離・速度・課題)を段階的に導入し、変化の背景とメリットを明確に説明する。急激な変化は認知的負荷を増大させ逆効果になる場合がある。
参考:Engaging patients to improve quality of care: a systematic review (Bombard 2018)
② 自立を促す:服薬スケジュールの自己管理・セルフモニタリングなど患者が自ら管理する機会を作る。自己効力感の向上が認知的回復を後押しする。
参考:Promoting self-management and patient independence (2004)

学習と記憶(Learning & Memory)― 新技能習得・手続き記憶

☑ 観察のポイント
- 新しい指示への適応性:新しい運動・器具の操作を学ぶ速さと持続性。情報の定着が難しい場合、学習・記憶機能に問題がある可能性
- 以前の習得スキルの維持:過去に学んだスキル(歩行器の使用法・移乗動作)が維持できているか。繰り返し再教育が必要なら手続き記憶への影響を示唆
💡 臨床介入ヒント
① 文書・絵・動画の活用:口頭指示だけでなく、文書・絵・写真・動画で視覚的補助を提供。後から確認できる形式にすることで学習を補完する。
参考:Effects of habit formation interventions on physical activity habit strength: meta-analysis (Haomin 2023)
② 日常の習慣としての取り組み:リハビリを毎日同じ時間・同じ手順で実施することで習慣化を促進。手続き記憶の強化に繰り返しと一貫性が重要。週2回以上・3ヶ月継続が運動学習の最低有効量とされる。

報酬に基づく意思決定(Reward-Based Decision Making)

☑ 観察のポイント
- ポジティブな結果への動機付けは?:改善への意欲・新しい目標に向かう積極性が低下していないか観察
- 報酬に対する反応は?:称賛・達成感・社会的承認への反応が減少または過剰になっていないか
💡 臨床介入ヒント
① ポジティブ・レインフォースメントの活用:課題完了・努力・小さな進歩に対して即座に正のフィードバックを与える。「できた」という経験の積み重ねが報酬回路を強化し、次の行動への動機づけを高める。
参考:A Study on Increasing Positive Behaviors Using Positive Reinforcement Techniques (Bivesa 2021)
② 進捗の可視化:歩行距離・握力・ADLの記録をグラフ化して患者と共有。数値で「進歩が見える」ことが報酬予測を強化し、継続意欲を維持する。

尾状核と被殻の違い ― 機能分化と臨床への含意

| 比較項目 | 尾状核(Caudate Nucleus) | 被殻(Putamen) |
|---|---|---|
| 主要機能 | 認知・学習・遂行機能・報酬処理 | 運動プロセス・動作調節・習慣的運動 |
| 主要な皮質ループ | 動機付け・遂行・視覚ループ | 運動ループが主体 |
| 接続する主な皮質 | 前頭前野・眼窩前頭皮質・帯状回 | 補足運動野・運動前野・一次運動野 |
| 関連疾患① | ハンチントン病(早期・主病巣) | ハンチントン病(進行期)・パーキンソン病 |
| 関連疾患② | 脳卒中後CRPS・遂行機能障害 | MCA梗塞後の純粋運動麻痺・構音障害 |
| 血液供給 | 頭部:ACA / 体部・尾部:MCA | 主にMCA(レンズ核線条体動脈) |
| リハビリの重点 | 認知課題・習慣形成・報酬フィードバック | 繰り返し運動練習・歩行再学習・作業療法 |
💡 大脳基底核の機能的理解を深めるポイント
尾状核と被殻は解剖学的に近接していますが機能的に明確に異なります。臨床上、「なぜこの患者は運動はできるのに学習が進まないのか」「なぜモチベーションが著しく低いのか」という疑問が生まれた際に、尾状核のどのループが障害されているかという視点で画像所見と症状を照合することで、より精緻なリハビリ計画が立案できます。
また、尾状核と被殻は内包(Internal Capsule)によって隔てられており、ラクナ梗塞(穿通枝梗塞)では内包・被殻が同時に障害されやすい一方、ACA梗塞では尾状核頭部が優先的に障害されます。画像読影と神経症状の組み合わせがリハビリ目標設定の精度を高めます。
臨床ケーススタディ ― 石川さんのリハビリ展開
📋 症例:石川さん(70代男性)脳卒中後 左基底核梗塞 ― リハビリ初回評価
| 評価領域 | 所見 | 尾状核の関連ループ |
|---|---|---|
| 歩行・バランス | 歩行リズムの乱れ・バランス不安定・足上げタイミングの不規則 | 運動ループ |
| 巧緻動作 | 歩行器の操作習得に時間がかかる・把持の不安定 | 運動・学習ループ |
| 記憶・学習 | 指示の定着が遅い・操作方法を繰り返し確認する | 遂行・学習ループ |
| 変化への適応 | 新しい環境・スケジュール変更への適応に困難 | 遂行ループ |
| モチベーション | 初期は不安・消極的。小さな成功で表情が明るくなる | 動機付けループ |
リハビリ目標の設定
目標①
歩行リズムとバランスの改善
トレッドミルを用いた歩行動作の再学習・協調性の回復
目標②
歩行器の安全な使用習得
視覚的補助(文書・目印)を活用した手続き記憶強化
目標③
自主トレ継続のための動機強化
ポジティブフィードバックと進捗可視化によるリハビリ意欲維持
リハビリの計画と実施
トレッドミルを使用した歩行訓練
ハーネス(免荷装置)を装着し、体重の一部をサポートした状態でトレッドミル歩行を開始。速度はゆっくりから始め、石川さんのリズムを取り戻しながら徐々に増加させます。免荷率も段階的に減らし、自立した歩行能力を回復させます。
田中先生:「ハーネスがあるので転倒の心配はありません。リズムを意識しながらゆっくり歩いてみましょう。」
石川さん:「少しずつ慣れてきた感じがします。」
歩行器の導入 ― 視覚的補助と目印の活用
歩行器の正しい使い方(持ち方・押し方・停止位置)を指導し、操作方法を紙に書いて病室に掲示。部屋・トイレに歩行器を止める位置に目印をつけ、どこで止めるかを一目で確認できるようにします。これにより学習・記憶ループへの補助的支援を行います。
田中先生:「こちらに使い方をまとめた紙を貼っておきます。これを見ながら使えば自然と慣れていけますよ。」
石川さん:「ありがとうございます。これで間違えずに使えそうです。」
ポジティブ・レインフォースメントの継続的活用
リハビリのたびに石川さんの小さな成功(歩行距離が10m伸びた・歩行器を正しい位置に止められた)を具体的に称賛します。「昨日より5歩多く歩けました」のように数値で示すことで報酬予測が明確になり、動機付けループを強化します。
田中先生:「今日の歩行器での歩行も素晴らしかったですよ!昨日より10メートル多く歩けました。」
石川さん:「少しずつですが自信が出てきました。」
数週間後の結果
①トレッドミル歩行スピードが向上し、免荷サポートなしで安定した歩行が可能に。②歩行器の使用方法を自己確認しながら病棟内を自主歩行できるようになった。③毎日同じ時間にリハビリを習慣化し、自主トレを継続するようになった。
リハビリを受けた方の声
最初は歩くたびにバランスが崩れて怖かったですが、田中先生がいつも「昨日よりここが良くなっています」と具体的に教えてくれたので、少しずつ自信がつきました。歩行器の使い方を紙に書いて貼ってもらってからは、自分一人でも病棟内を歩けるようになりました。
70代男性・左基底核梗塞 発症後2ヶ月
よくある質問(FAQ) ― 尾状核に関するQ&A
尾状核の損傷でどのような症状が出ますか?
特に臨床現場では「麻痺の程度の割に学習が進まない」「モチベーションが極端に低下している」「習慣的な動作が崩れやすい」といった現象に尾状核損傷の影響が隠れている可能性があります。
尾状核と被殻はどう違うのですか?覚え方も教えてください。
覚え方:「尾状核は”考える”線条体、被殻は”動く”線条体」。前頭前野(思考の中枢)が尾状核に強く接続し、運動野(動きの中枢)が被殻に強く接続していることを想像すると覚えやすいです。
ただし実際には両者は連携して動いており、複雑な行動(例:新しい動作の学習)では両方が同時に活動します。機能分化は相対的なものです。
ハンチントン病で尾状核が障害されるとなぜ舞踏運動が起きるのですか?
通常、大脳基底核は「不要な運動プログラムを抑制する」働きをしています。間接路の障害によりこの抑制が失われ、不必要な運動プログラムが次々と実行されることで舞踏運動(コレア)が生じます。これは「ブレーキが効かない状態」とも言えます。
進行すると直接路も障害され、最終的には筋硬直・運動緩慢(パーキンソン型)へと移行します。
脳卒中後にCRPS(複合性局所疼痛症候群)が生じた患者で尾状核はどう関与しますか?
尾状核は疼痛の認知処理(痛みをどう感じ、どう評価するか)に関与しています。具体的には、①疼痛に関連した情動反応の調節、②疼痛記憶の形成と更新、③痛みに対する注意の偏りの制御に寄与していると考えられています。
臨床的には、尾状核頭部・被殻への病変を持つ患者ではCRPS発症を念頭に置いた早期スクリーニングと、鏡療法・TENS・段階的な患側上肢負荷を組み合わせた介入計画が推奨されます。
尾状核損傷の患者にポジティブフィードバックを使う際の注意点は?
注意点①:具体性:「すごいですね」という漠然とした称賛より、「昨日より5メートル多く歩けました」という具体的なフィードバックが報酬予測を強化します。
注意点②:適切な頻度:過剰な称賛は「この程度で褒められるの?」という認知的不一致を生む場合があります。達成度に見合った称賛を心がけます。
注意点③:失敗への対応:失敗した際に否定的なフィードバックを与えることは避け、「次はこうしてみましょう」という前向きな方向付けを行います。
注意点④:外的動機から内的動機へ:長期的には、外的報酬(称賛)から「自分でできた」という内的達成感へと移行させることが自立支援の目標です。
尾状核のリハビリに特化した評価法はありますか?
・遂行機能:Trail Making Test(TMT)・Wisconsin Card Sorting Test(WCST)・Frontal Assessment Battery(FAB)
・記憶・学習:RBMT(リバーミード行動記憶検査)・WMS-R
・運動協調:Berg Balance Scale・Timed Up and Go(TUG)・歩行分析
・動機付け・抑うつ:Apathy Scale・GDS(老年期うつ評価尺度)
・疼痛(CRPS疑い):Budapest Criteria・VAS・LANSS
これらを急性期・回復期・退院時の各タイミングで実施し、経時的な変化を追うことで介入効果を可視化できます。
専門家向け:尾状核と手続き記憶 ― 海馬との機能的分業
海馬(陳述記憶)vs 尾状核(手続き記憶)の二重解離:海馬は「いつ・どこで何があった」というエピソード記憶・宣言記憶(陳述記憶)に関与します。一方、尾状核を含む線条体は「どうやって行動するか」という手続き記憶(procedural memory)・習慣記憶の主要基盤です。
この二重解離は、海馬損傷(健忘症)患者が新しい運動スキル(鏡描写など)を正常に学習できる一方でその学習記憶がないと報告するという古典的研究(Milner 1962)で示されています。逆に線条体損傷患者は運動スキル学習が障害される一方、エピソード記憶は保たれます。
臨床的含意:アルツハイマー病では早期から海馬が障害されますが線条体は比較的保たれるため、習慣化されたADL動作(手続き記憶)は長期間維持されます。この原則はリハビリでの反復練習設計に重要です。一方、ハンチントン病・尾状核梗塞では手続き記憶の新規形成が障害されるため、新しいADL動作の習得に著しい困難が生じます。
自己評価チェック ― 理解度確認10問
参考文献
- 1) Seger CA. How do the basal ganglia contribute to categorization? Their roles in generalization, response selection, and learning via feedback. Neurosci Biobehav Rev. 2008;32(2):265-278. PubMed
- 2) DeLong MR. Primate models of movement disorders of basal ganglia origin. Trends Neurosci. 1990;13(7):281-285. PubMed 【直接路・間接路モデルの古典的出典】
- 3) Lee J, et al. Neuroanatomical correlates of poststroke complex regional pain syndrome: a voxel-based lesion symptom-mapping study. Stroke. 2021;52(9):2913-2920. PubMed
- 4) Kumral E, et al. Caudate nucleus infarcts: clinical and magnetic resonance imaging findings. Stroke. 1999;30(1):100-108. PubMed 【尾状核梗塞の症候論】
- 5) Saxena S, Rauch SL. Functional neuroimaging and the neuroanatomy of obsessive-compulsive disorder. Psychiatr Clin North Am. 2002;25(4):833-834. PubMed 【OCD・尾状核過活動】
- 6) Marin RS. Apathy: a neuropsychiatric syndrome. J Neuropsychiatry Clin Neurosci. 1991;3(3):243-254. PubMed 【アパシーの定義・評価】
- 7) Hatem SM, et al. Rehabilitation of Motor Function after Stroke: A Multiple Systematic Review. Front Hum Neurosci. 2016;10:442. PubMed
- 8) Fu Q, et al. Feasibility of challenging treadmill speed-dependent gait and perturbation-induced balance training in chronic stroke patients with low ambulation ability. Eur J Phys Rehabil Med. 2023;59(4):455-465. PubMed
- 9) Monica BJ, et al. Randomization to Treadmill Training Improves Physical and Metabolic Health in Association With Declines in Oxidative Stress in Stroke. J Stroke Cerebrovasc Dis. 2022;31(10):106647. PubMed
- 10) Haomin Y, et al. Effects of habit formation interventions on physical activity habit strength: meta-analysis and meta-regression. Health Psychol Rev. 2023;17(4):687-706. PubMed
- 11) Bombard Y, et al. Engaging patients to improve quality of care: a systematic review. Implement Sci. 2018;13(1):98. PubMed
- 12) David FJ, et al. Exercise improves cognition in Parkinson’s disease: The PRET-PD randomized, clinical trial. Mov Disord. 2015;30(12):1657-1663. PubMed
- 13) Milner B. Les troubles de la mémoire accompagnant les lésions hippocampiques bilatérales. Physiologie de l’Hippocampe. 1962:257-272.
- 14) STROKE LAB 金子唯史.「脳の機能解剖とリハビリテーション」医学書院,2024年.

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)