【徹底解説】網様体脊髄路(RST)の解剖・機能と脳卒中後の病態メカニズム:臨床評価からリハビリテーション応用まで
脳卒中後のリハビリテーション現場で「なぜ麻痺側の腕が曲がったまま固まるのか」「なぜ歩行時に姿勢が崩れるのか」「運動の回復に皮質脊髄路だけでなく別の経路が重要と聞くが、具体的にどういうことか」――この答えの多くが網様体脊髄路(Reticulospinal Tract:RST)にあります。本記事では解剖・機能・脳卒中後の病態から論文エビデンス・評価・リハビリ応用・症例検討まで、最新の神経科学的知見をもとに徹底解説します。
網様体脊髄路(Reticulospinal Tract:RST)は脳幹の網様体から脊髄へ下行する錐体外路系の主要経路で、姿勢制御・筋緊張調整・自動的な運動パターン生成に中心的な役割を果たします。橋を起始とする内側路(橋網様体脊髄路)と延髄を起始とする外側路(延髄網様体脊髄路)の2系統があり、それぞれ主に抗重力筋・伸筋と屈筋系の運動ニューロンへ入力します。脳卒中後に皮質脊髄路(CST)・皮質網様体路(CRT)が損傷されると、内側RSTが上位からの制御を失って相対的に優位となり、近位筋への過剰バイアス・痙縮・屈曲-内転シナジー・連合反応の温床となります。一方、適切なリハビリテーション介入によってRSTを介した神経可塑性が誘導され、機能回復の重要な基盤となることも近年明らかになっています。
- 正式名称:Reticulospinal Tract(RST)/ 網様体脊髄路。錐体外路に含まれる下行路
- 2系統の構成:内側路(橋網様体脊髄路・前索走行・主に伸筋・抗重力筋へ興奮性入力)と外側路(延髄網様体脊髄路・側索走行・主に屈筋へ興奮性入力+内側路の調節)。一般的教科書は外側路のみ掲載のことが多い
- 🔑 重要な修正ポイント:橋RST(内側)の本来の生理作用は「伸筋・抗重力筋の興奮」。脳卒中後の「屈曲シナジー」は、CSTの選択的抑制消失+内側RST亢進による近位筋への過剰バイアスの複合によって生じる
- 主な機能:姿勢制御・筋緊張調整・α・γ運動ニューロン活動の制御・呼吸・循環のサポート・歩行リズム生成(CPG連動)
- 脳卒中後の変化:CST・CRT損傷 → 内側RST(橋)が上位制御を失い相対的に優位 → 近位筋への過剰バイアス → 屈曲-内転シナジー・痙縮・連合反応
- 脊髄内介在ニューロンとの連携:Ia相反抑制介在ニューロン(CSTで制御)・Renshaw細胞(反回抑制)がCST損傷後に機能不全となり、痙縮を増悪させる
- 神経可塑性・回復:CST損傷後にRSTが新しい単シナプス入力を手の運動ニューロンへ形成する可能性(Zaaimi et al. 2012)。RSTを介した代償的回復はリハビリターゲットとなりうる
- 皮質網様体路(CRT):運動前野(area6)を起始とし、放線冠・内包後脚を通り橋・延髄網様体核へ。皮質脊髄路の前内側を並走(Yeo et al. 2012)。内包レベルでのCRT損傷は姿勢制御障害の主因
- 体幹筋のremote effect:体幹筋収縮中に上下肢のMEPが有意に増大。体幹筋は一次運動野内で四肢への興奮波及のハブとして機能する可能性(Sasaki et al. 2018)
- 痙縮評価:Modified Ashworth Scale(MAS)・Tardieu Scale(速度依存性の評価に優れる)。脳卒中後の痙縮管理にはボツリヌス毒素(BTX-A)+リハビリの組み合わせが標準
網様体脊髄路とは ― 解剖・走行・錐体外路系での位置づけ
網様体脊髄路(Reticulospinal Tract:RST)は、脳幹の網様体(reticular formation)を起始核とし、脊髄へ下降する錐体外路系の主要な下行路のひとつです。「網様体」とは脳幹(中脳・橋・延髄)全体に広がるニューロン集団で、神経線維が網の目状に絡み合う構造から名付けられています。感覚・運動・自律神経・意識・呼吸など多彩な機能を統括するハブとして機能します。
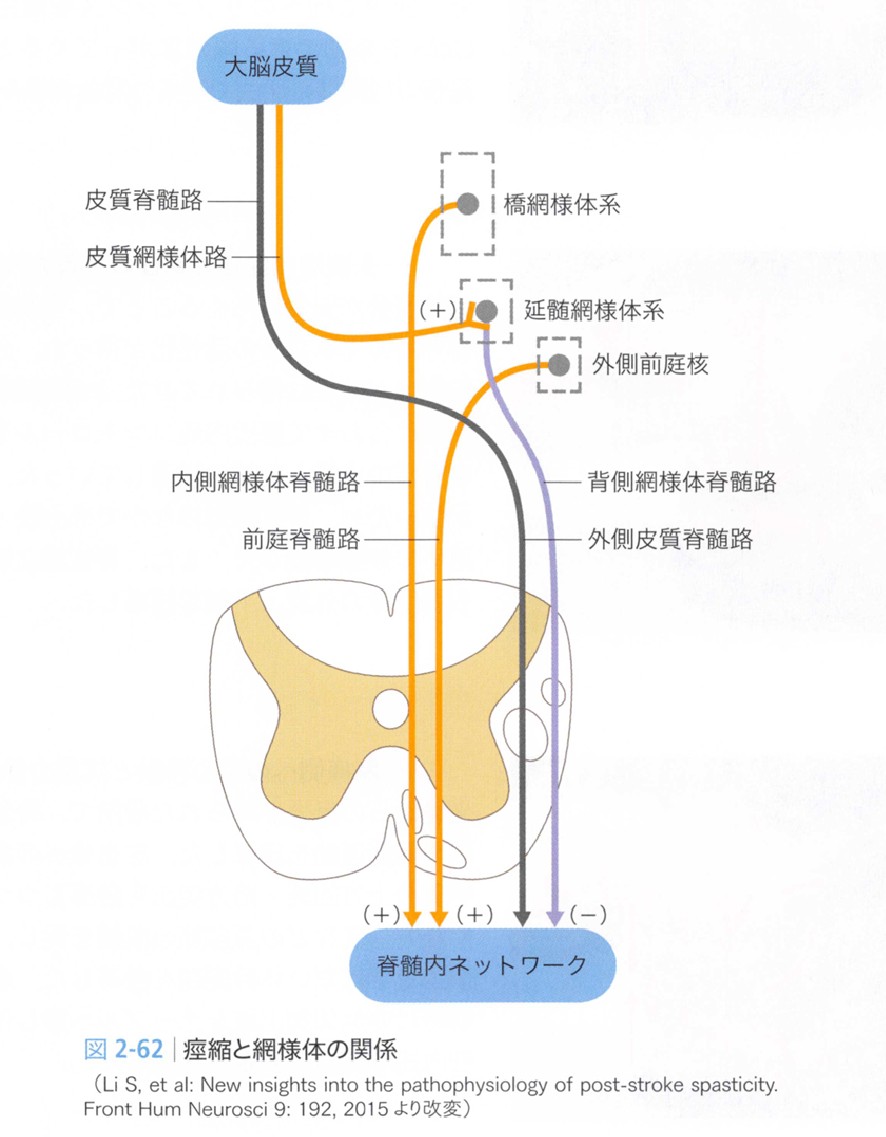
金子唯史:脳卒中の動作分析・医学書院より引用。各下行路の走行と脊髄内への入力を示す。
🔬 網様体脊髄路の2系統:内側路と外側路
下行網様体脊髄路は走行と機能から内側路(橋網様体脊髄路)と外側路(延髄網様体脊髄路)に大別されます。一般的な教科書では外側路(側索走行)のみが掲載されていることが多いですが、姿勢制御・脳卒中後病態の理解には内側路の知識が不可欠です。
内側路(橋網様体脊髄路):橋の網様体核(橋被蓋)を起始とし、脊髄前索を同側優位に下行。脊髄前角・中間層の腹内側部に投射し、主に体幹・伸筋系・抗重力筋の制御を担います。姿勢保持・抗重力機能を支える経路です。
外側路(延髄網様体脊髄路):延髄の網様体核(巨細胞野・傍巨細胞野)を起始とし、脊髄側索を両側性に下行。脊髄前角・中間層の外側部に投射し、主に屈筋系の運動ニューロンへ興奮性入力を行うと同時に、内側路の活動を調節することでトーンのバランスを整えます。
⚠️「内側RST=屈筋系」「外側RST=抑制系」という単純化への注意
一部の参考書では内側RST(橋)を「屈筋系の経路」、外側RST(延髄)を「抑制性経路」と単純化して記載しているケースがあります。しかし、Kuypers(1981)以来の古典的知見では、橋RST(内側)は主に体幹・伸筋・抗重力筋を興奮させる経路です。延髄RST(外側)は屈筋系への興奮性入力を持ちつつ、内側RSTの活動を調節します。「外側RSTが純粋に抑制性」というわけではありません。
脳卒中後に内側RSTの代償亢進で「屈曲シナジー」が出現するのは、①CSTによる遠位・選択的筋制御の消失 ②内側RSTの近位筋全般への過剰バイアス ③屈筋抑制の相対的な消失という複合メカニズムによるものです。「内側RSTが屈筋を直接亢進させる」という単純な図式ではありません。
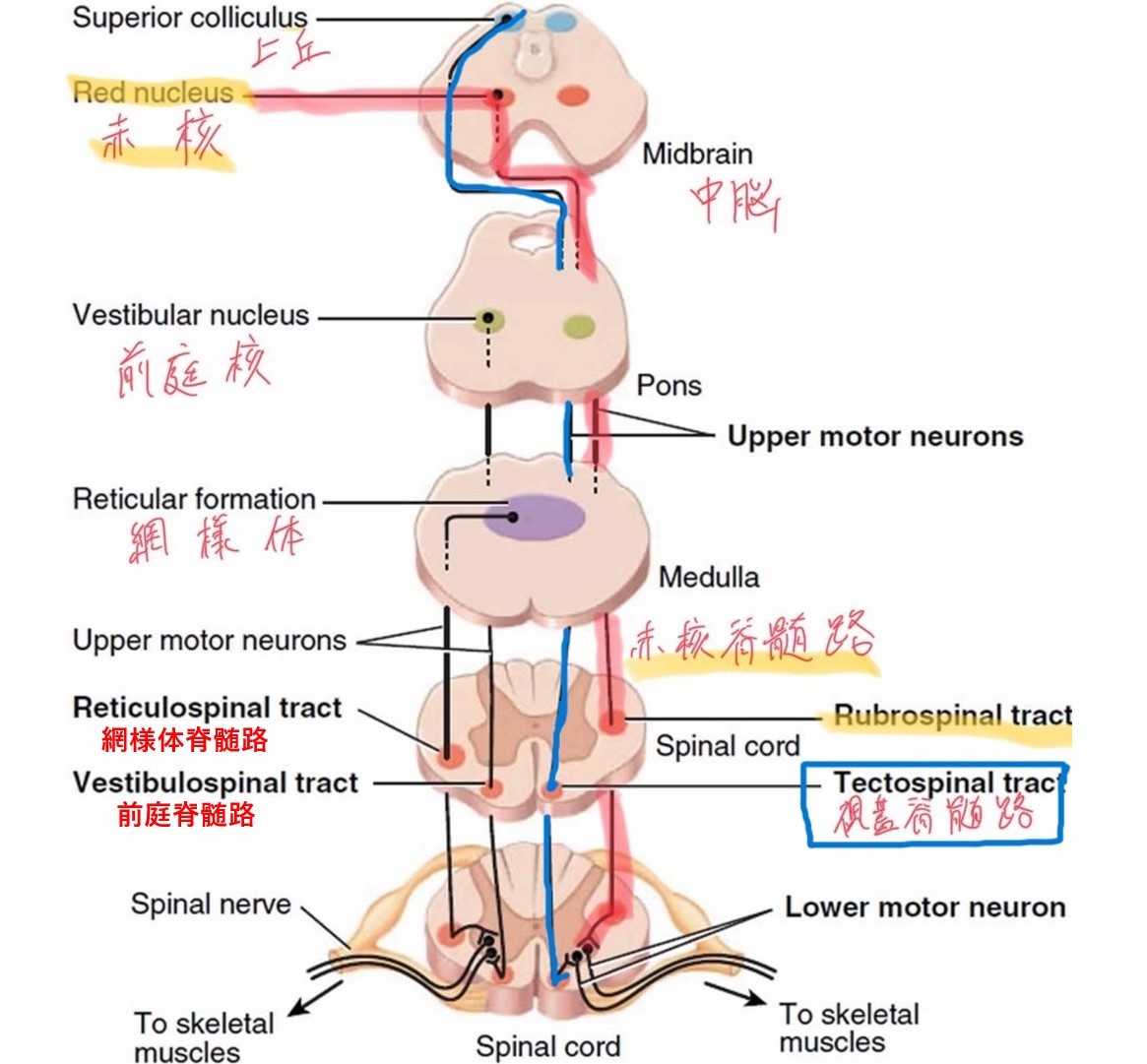
外側路(延髄網様体脊髄路)の走行。内側路(前索)は多くの教科書で省略されているため、両路の比較理解が重要。
内側・外側網様体脊髄路の機能と違い
内側路(橋網様体脊髄路)の機能
橋網様体脊髄路(Medial Reticulospinal Tract)― 抗重力姿勢と体幹安定の主役
- 体幹の運動ニューロンおよび伸筋・抗重力筋の運動ニューロン(例:姿勢維持のための下肢伸展・体幹起立筋)への主要な興奮性入力を担う(Kuypers 1981)
- 中脳の運動中枢(MLR:中脳歩行誘発領域)を刺激するとパターン化した運動(例:足踏み)が生じる → 歩行リズム生成との連動
- α・γ運動ニューロン両方に投射し、筋紡錘の感度設定にも関与
- 前庭脊髄路と協調し、同時に多くの筋肉を選択的に活性化することが可能(介在ニューロン経由)
- 大脳皮質-網様体路(CRT)を通じて近位筋の姿勢フィードフォワード制御を担う
- 霊長類の研究(Baker 2011):CST損傷後にRSTが手の運動ニューロンへの新しい単シナプス入力を形成し、代償的な機能回復に貢献する可能性
📌 脳卒中後に「屈曲シナジー」が生じる理由(正確なメカニズム)
橋RST(内側)の本来の生理作用は「体幹・伸筋の興奮」ですが、脳卒中後に上位制御が失われると近位筋全般(上肢では屈筋系が優位な近位筋を含む)への過剰バイアスが生じます。これにCSTによる遠位・選択的筋制御の消失、Ia相反抑制介在ニューロンの機能低下が加わり、上肢では屈曲-内転シナジーが優位となります。「内側RSTが直接屈筋を亢進させる」のではなく、「内側RSTの過剰活動+CST制御の消失が組み合わさって屈曲パターンが生じる」という複合メカニズムです。
外側路(延髄網様体脊髄路)の機能
延髄網様体脊髄路(Lateral Reticulospinal Tract)― 屈筋系の駆動と筋緊張バランスの調整
- 屈筋系の運動ニューロンへの主要な興奮性入力を担う(内側路の伸筋優位と相補的)
- 内側路の活動を調節することで、伸筋・屈筋のバランスを整え「適正な筋緊張」を維持する(トーンの精細調節)
- 両側性投射により、片側の遊脚期に対側の立脚筋を維持するなど歩行の左右協調に関与
- 脳卒中後にCSTの制御が消失すると、延髄RSTの調節機能も低下し、内側RST過剰→全体的トーン過剰の方向へ
網様体脊髄路の全機能リスト
🔑 網様体脊髄路の多面的な機能(臨床的に重要な順)
① 姿勢制御:日常的な状況下での姿勢安定付与。反射的・自動的な姿勢調整(フィードフォワード)を担う。皮質脊髄路が「随意的・認知的課題(精細運動)」を担うのに対し、RSTは「自動的・習慣的姿勢制御」を担う。
② α・γ運動ニューロンの制御:筋線維の収縮力(α)と筋紡錘の感度(γ)を同時に調整。γ運動ニューロン活性の変化は伸張反射の閾値を変更し、脳卒中後の痙縮に深く関与する。
③ 歩行のリズム生成:中枢性パターンジェネレータ(CPG)と連動し、屈筋・伸筋の交互活動を駆動。内側RSTが歩行の「立脚相(伸展維持)」を、延髄RSTが「遊脚相(屈曲駆動)」を支援すると考えられている。
④ 呼吸・循環のサポート:呼吸中枢・心臓血管中枢との連絡を持ち、運動時の換気量増加・血圧調整に関与。「あくびで患側の手が緩む」「咳で腕が曲がる」といった臨床観察現象はこの連絡に関係していると推測されているが、メカニズムの詳細は完全には解明されていない。
⑤ 霊長類での力制御(Baker 2011):近年の研究ではRSTが筋収縮に必要な力の大きさをコード化する能力も持つことが示唆されている。CST損傷後のRSTによる代償的な手の運動制御回復の可能性が注目されている。
皮質-網様体系の全体像 ― 経路比較表(修正版)と脳卒中後の変化
| 経路名 | 起始・走行 | 脊髄内への主な入力 | 主な生理作用 | 脳卒中後の変化 |
|---|---|---|---|---|
| 皮質脊髄路(CST) 錐体路 |
大脳皮質(M1/PMC)→ 錐体交叉 → 前角 | (+) 遠位筋・手指筋への直接興奮性投射(単シナプス) ※拮抗筋の相反抑制はIa介在ニューロン経由 |
遠位四肢の随意・精細運動の駆動。RST・脊髄反射系へのトップダウン制御 | 損傷で精密運動↓・RST制御喪失→ RST代償的優位に |
| 皮質網様体路(CRT) 錐体外路 |
運動前野(area6)/SMA → 内包後脚 → 橋・延髄網様体 | 網様体核を興奮・抑制し(+/-)姿勢制御を準備 | 動作前の姿勢フィードフォワードと近位筋トーン調整 | CST損傷と同経路で損傷されやすい。CRT損傷で近位筋・姿勢制御↓ |
| 内側網様体脊髄路(橋RST) 橋 |
橋網様体核 → 前索(同側優位) | (+) 体幹・伸筋・抗重力筋への興奮性入力(近位筋全般への広域バイアス) | 抗重力姿勢保持・体幹安定・歩行リズム(立脚相) | CST/CRT制御喪失で代償的に亢進→ 近位筋過剰バイアス→ 屈曲-内転シナジー(CSTの選択的制御消失と組み合わさって) |
| 外側網様体脊髄路(延髄RST) 延髄 |
延髄網様体核 → 側索(両側性) | (+) 屈筋ニューロンへの興奮性入力。内側RSTの調節も担う | 屈曲運動の駆動・トーンのバランス調節(内側路との相補) | 調節機能低下でトーン過剰・反射亢進が促進 |
| 前庭脊髄路(lat-VST) 平衡 |
外側前庭核 → 同側前索 | (+) 伸筋・抗重力筋を興奮 | 平衡・転倒防止(内耳からの平衡感覚情報を筋緊張に変換) | 過活動で伸展スパズム・尖足 |
🔬 脊髄内の介在ニューロンネットワーク ― CST損傷後の反射系変化
痙縮を理解するには、脊髄内の抑制系介在ニューロンの役割が重要です。CSTは脊髄に達した後、運動ニューロンへの直接入力だけでなく、以下の介在ニューロン系への制御も行っています。
Ia相反抑制介在ニューロン:主動筋を収縮させる際に拮抗筋を抑制するニューロン。CSTはこのニューロンを賦活し、スムーズな随意運動を可能にします。CST損傷後にこの抑制系が機能不全となり、屈筋・伸筋の同時収縮(共同収縮)が増加します。
Renshaw細胞(反回抑制):運動ニューロンが興奮すると、その軸索側枝からRenshaw細胞を介して自身を抑制するフィードバック回路。CSTはRenshaw細胞を抑制することで自己抑制を弱め、より持続的な随意運動を可能にします。CST損傷後はRenshaw抑制が過剰となり筋活動が不安定になる可能性があります。
Ib抑制介在ニューロン(Golgi腱器官からの入力):過剰な筋力発揮を防ぐ腱器官からの抑制系。CST損傷後に変調し、力の調節が困難になります。
⚠️ CSTの「抑制ブレーキ」という表現について
「CSTがRSTに抑制ブレーキを供給する」という説明は臨床的にわかりやすい表現ですが、より正確には「大脳皮質はCRT(皮質網様体路)を通じてRSTへのトップダウン制御信号を供給しており、これが損傷されることでRSTが過剰となる」です。CSTが直接RSTを抑制するのではなく、CRT損傷→網様体核へのコントロール消失→RST脱抑制という経路が主要なメカニズムです。また、脊髄レベルでのIa介在ニューロン・Renshaw細胞の機能不全も痙縮の重要な要因です。
脳卒中後の網様体脊髄路病態 ― 3つのメカニズム
① 内側網様体脊髄路(橋RST)の代償亢進
CST・CRT損傷 → 橋RST上位制御喪失 → 近位筋への過剰バイアス → 屈曲-内転シナジー
脳卒中後、CST(皮質脊髄路)とCRT(皮質網様体路)の両方がダメージを受けます。これらが供給していた「脊髄・網様体へのトップダウン制御」が消失すると、橋の内側RST が相対的に優位となります。橋RSTは本来、体幹・抗重力筋の安定に関与しており、近位筋全般への広域バイアスを持ちます。CSTによる遠位・選択的筋制御が消失した状態では、上腕二頭筋・腸腰筋・大腿内転筋などの近位屈筋系が相対的に優位となります。臨床的には「肩が前方に突き出す・肘が曲がる・股関節が屈曲位」という屈曲-内転シナジーパターンとして現れます。
② 前庭脊髄路(lat-VST)との協調失調
VST過活動 → 肩甲下筋・大胸筋の共同収縮 → 内旋固縮・伸展スパズム
前庭脊髄路(VST)は内耳からの平衡感覚情報を伸筋・抗重力筋への興奮として変換する経路です。脳卒中後はCSTによるVSTへのトップダウン制御が消失し、VSTが相対的に過剰となります。これにより肩甲下筋・大胸筋が同時収縮し、上腕が過度に内旋した状態で固まりやすくなります。下肢では立脚期の伸展スパズム・尖足がVST過活動の代表的な臨床像です。触診では肩の前面が膨らんで骨頭が目立ち、内旋位固縮として観察されます。
③ 脊髄内伸張反射ループの過敏化
Ia伸張反射閾値低下 + 介在ニューロン機能不全 → 速度依存性の筋緊張増大(痙縮)
脳卒中後、CSTが脊髄介在ニューロン(Ia相反抑制系・Renshaw細胞)へのトップダウン制御を失うと、これらの抑制系が機能不全に陥ります。その結果、Ia求心性線維(筋紡錘からの信号)がα運動ニューロンへ容易に伝達されるようになり(伸張反射の閾値低下)、わずかな動きや速いストレッチで”カクッ”と収縮が始まるキャッチ現象が生じます。持続的な筋緊張により筋・結合組織の粘弾性変化(短縮)が加わり、最終的に関節可動域制限へと発展します。γ運動ニューロンの調整不全も筋紡錘感度の異常亢進に寄与すると考えられています。
痙縮・筋緊張亢進の神経生理と臨床評価
| メカニズム | 神経生理のポイント | 脳卒中後の臨床所見 |
|---|---|---|
| ① 内側RST(橋)代償亢進 | CRT/CSTトップダウン制御喪失 → 橋網様体核の脱抑制 → 近位筋への広域バイアス亢進 | 上腕二頭筋・肩周囲屈筋の持続高トーヌス。肩関節前下方への求心力不均衡 → 骨頭の前方突出・軽度下方亜脱臼 |
| ② 前庭脊髄路(VST)過活動 | CST制御消失 → VST脱抑制 → 伸筋・抗重力筋への過剰興奮性入力 | 肩甲下筋+大胸筋の共同収縮優位(上肢内旋固縮)。立脚期の伸展スパズム・尖足 |
| ③ 脊髄介在ニューロン機能不全 | Ia相反抑制↓・Renshaw抑制変調 → 拮抗筋同時収縮増加・伸張反射閾値低下 | 速度依存性の”キャッチ”(Modified Tardieu Scale で評価)。拮抗筋共同収縮による運動制御不全 |
| ④ 延髄RST調節機能低下 | 延髄RST(屈筋・トーンバランス調節)の機能低下 | 筋緊張の”引き算”ができず全体的トーン過剰。夜間・睡眠時の変動(自律神経連絡による) |
| ⑤ 筋・結合組織の二次変化 | 持続的過緊張 → 筋・腱・関節包の短縮・線維化(神経メカニズムから二次的な構造変化へ) | 他動関節可動域制限(ROM制限)。安静時にも関節抵抗が存在する”挛縮”への移行 |
痙縮の臨床評価スケール
📏 Modified Ashworth Scale(MAS)と Tardieu Scale ― 目的に応じた使い分け
| 評価スケール | 評価内容 | 網様体系病態との対応 | 特徴・限界 |
|---|---|---|---|
| Modified Ashworth Scale(MAS) | 他動運動時の筋抵抗(0〜4点)。一定速度で関節を動かしたときの抵抗の程度 | 内側RST亢進・Ia閾値低下・筋の二次変化を総合的に反映 | 速度を統制しないため「神経性痙縮」と「筋・結合組織の拘縮」を区別しにくい。簡便で広く使用 |
| Tardieu Scale(Modified版) | 遅い速度(V1)と速い速度(V3)での抵抗を比較。速度依存性(R2-R1)を算出 | Ia伸張反射閾値低下(速度依存性の神経性痙縮)を特異的に評価 | 「神経性痙縮」と「拘縮」を区別できる。V1とV3の差が大きいほど神経性痙縮の寄与が大きい。臨床研究では推奨度が高い |
| Penn Spasm Frequency Scale | 自発的な筋スパズムの頻度(0〜4点) | RST脱抑制による自発的筋放電の頻度を反映 | 患者の主観的な報告に基づく。夜間スパズムの評価に有用 |
臨床的ポイント:ボツリヌス毒素(BTX-A)治療の適応判断にはTardieu Scaleが推奨されます(速度依存性の神経性痙縮が主体かどうかを確認するため)。MAS 3点以上でも、Tardieu Scale でR2-R1 ≒ 0 の場合は拘縮が主体であり、BTX-Aの適応は低い可能性があります。
💡 脳卒中後の臨床兆候と網様体系の対応関係
RST亢進による脊髄反射の過敏
・速度依存性の抵抗と安静時の筋緊張増大(Tardieu Scale・MAS陽性)
・正常な刺激(様々なスピードでの他動ストレッチ)や不快刺激(皮膚・自律神経系)に対する過剰反応
・歩行時の姿勢変化に伴う大幅な筋緊張変動
皮質脊髄路の随意活動減少と定型的シナジー出現
・痙縮様の同時収縮(例:肘を伸ばそうとすると肘が曲がる)
・定型的シナジーパターン(上肢:屈曲-内転-回内シナジー、下肢:伸展-内転-足底屈曲)
・連合反応(健側使用時に患側が不随意に動く:RSTの両側投射的性質と関連)
脱抑制した網様体系と感情・自律神経の連動
・感情変化(怒り・不安・痛み)に伴う筋緊張上昇(網様体は辺縁系と連絡)
・「あくびで患側手が緩む」「咳で腕が曲がる」といった臨床観察(呼吸中枢と運動系の連絡による推測されるメカニズム。詳細は未解明)
・交感神経性症状(発汗・血圧変動)との連動
歩行・姿勢制御との関係 ― CPGと網様体路
動物実験では、脊髄の中枢性パターンジェネレータ(CPG:Central Pattern Generator)が運動リズムの生成に関与することが分かっています。頸部・腰部の介在ニューロンが屈筋・伸筋を交互に活性化し、自動的なリズム運動を生成します。ヒトでは運動は中脳歩行誘発領域(MLR)を含む脳幹回路で調整され、大脳皮質運動前野がCRTを通じて脳幹網様体路へ投射することで、RSTは皮質脊髄路と協働して姿勢制御と歩行リズムを統合します。
🏃 歩行における内側・外側RST の役割(修正版)
立脚相(体重支持):内側RST(橋)が体幹・伸筋への興奮性入力を維持し、抗重力的な荷重受容を支援。前庭脊髄路(VST)と協調して転倒防止の抗重力活動を持続します。
遊脚相(振り出し):延髄RST(外側)が屈筋系の運動ニューロンへ興奮性入力を行い、股屈曲・膝屈曲・足背屈の連動(屈曲シナジー)を適切な強さで駆動します。
体幹の回旋安定(歩行中):内側RSTが多裂筋・脊柱起立筋を絶えず微調整。CRTを通じた皮質からのフィードフォワード制御が体幹の先行的安定に貢献します。
脳卒中後の歩行障害:CST損傷+CRT損傷 → 内側RST代償亢進 → 立脚相は伸展パターンの過剰(VST過活動との相乗)、遊脚相は延髄RST/CSTによる屈曲シナジーの精細制御が失われ → 分回し歩行・鶏歩・尖足などの代償パターンが出現します。
| 歩行相 | 正常時の主なRST機能 | 脳卒中後の変化 | 臨床的観察所見 |
|---|---|---|---|
| 立脚相(支持期) | |||
| 初期接地(IC) | 内側RST:下肢伸筋を予備的に興奮(姿勢フィードフォワード) | VST過活動による伸展パターン過剰 | 膝過伸展・尖足での接地 |
| 荷重応答期(LR) | 体幹RST:体幹側屈筋を安定させ重心移動を制御 | 体幹側屈不足・患側への傾斜 | 麻痺側への体幹傾斜・Trendelenburg徴候 |
| 立脚中期〜末期 | 延髄RST:屈筋への入力で前方推進のための「伸展からの解放」を準備 | 延髄RST機能低下 → 立脚後期に伸展が過剰残存 | 蹴り出し不全・歩幅短縮 |
| 遊脚相(振り出し期) | |||
| 遊脚初期〜中期 | 延髄RST:屈曲シナジー(股屈曲・膝屈曲・足背屈)を適切な強さで駆動 | CST消失により屈曲シナジーの精細制御不全 | 分回し歩行・鶏歩 |
| 遊脚終期 | 内側RST:着地前に伸展への切り替えを準備(両RST協調) | 切り替え遅延・筋緊張変動不安定 | 着地衝撃増大・バランス不安定 |
神経可塑性とRSTによる機能回復 ― 代償・適応の最新知見
脳卒中後のRSTは「過剰な筋緊張・痙縮の原因」として問題視されてきましたが、近年の研究ではRSTが機能回復の重要な足場(scaffold)ともなりうることが示されています。これは「RSTを抑制する」のではなく「RSTを適切にコントロールする」というリハビリ戦略の変化をもたらしています。
🧠 CST損傷後のRSTによる代償的シナプス形成(Zaaimi et al. 2012)
サルのCST(錐体路)を実験的に損傷した研究(Zaaimi et al. 2012, Brain)では、損傷後数週間の経過でRST起源の新しい単シナプス入力(monosynaptic connections)が手の運動ニューロン(手内在筋を支配)へ形成されることが示されました。正常時にはRSTから手の運動ニューロンへの直接単シナプス接続はほとんど存在しませんが、CST損傷後に新たに形成されます。
これは「CST損傷後にRSTが新しい回路を作り、手の運動制御を部分的に代償しようとする」ことを示唆しており、脳卒中後の手機能回復の神経基盤のひとつがRSTである可能性を示しています。ただしこの代償的なRST入力は、精細な手の運動ではなく「粗大な近位筋・遠位筋の協調」に限定される可能性があり、CSTの精細な制御を完全に代替するものではありません。
🧠 RSTと手機能回復の可能性(Baker 2011)
Baker(2011, J Physiol)の総説では、霊長類のRSTが手の機能と機能回復においてより重要な役割を持つことが論じられています。特に:
① 正常な霊長類でも、RSTは把握動作などの近位・遠位筋協調に一定の寄与を持つ
② CST損傷後のRSTによる代償は「粗大な把握(power grip)」には有効だが、精細なつまみ動作(precision grip)の完全回復は難しい
③ リハビリテーションはRSTを介した新しい回路形成(シナプス可塑性)を促進することで効果をもたらす可能性がある
この知見は「脳卒中後の手機能回復でなぜある程度の改善は見られても、精細な手の動きが最後まで残りにくいのか」の神経学的説明になっています。CST依存の精細な手の動きはRSTでは完全に代替できないためです。
💡 神経可塑性を促進するリハビリの方向性 ― RST可塑性の観点から
①課題指向型訓練(Task-oriented training):反復的な日常生活動作訓練は、RSTを介した新しいシナプス形成を促進すると考えられています。「粗大把握 → 精細把握」の段階的アプローチが、CST回復とRST代償の両方を活用します。
②FES(機能的電気刺激):麻痺筋への電気刺激は末梢からの求心性フィードバックを増加させ、脳幹・脊髄レベルでのシナプス再編成を促進する可能性があります。棘上筋へのFESによる肩の求心圧維持はRSTによる骨頭前方偏位の予防にも直結します。
③非侵襲的脳刺激(rTMS・tDCS):健側半球の過活動抑制(低頻度rTMS)または患側運動野の興奮性上昇(tDCS)が、CST/CRTの残存機能の回復とRST代償の最適化に寄与する可能性が研究されています。
④ロボット支援・CIMT:強制的な患側使用(CIMT:Constraint-Induced Movement Therapy)と反復訓練は、CST・RSTの両方の神経可塑性を促進し、代償的な行動パターンの再学習を支援します。
論文エビデンス ― 網様体脊髄路の神経科学的根拠
論文① ヒトの脳の皮質網様体路:拡散テンソル画像を用いた研究
🎯 背景・目的
皮質網様体路(CRT)は姿勢制御・移動能力に関与することが動物研究で示されていたが、ヒトの脳内でCRTを画像化した研究はなかった。DTIを用いてヒトの皮質網様体路を初めて同定することを目的とした。
🔬 方法
1.5テスラMRIにてDTI撮像(ACPC線平行、スライス厚2.3mm)。ROI①を中脳被蓋、ROI②を運動前野(ブロードマンarea6)に設定し、FA値・MD値・線維量を左右半球で測定・比較した。
📊 結果
運動前野(area6)を起始とする皮質網様体路は、皮質脊髄路の前方(前内側)を通り、放線冠・内包後脚を下降し、中脳・橋の被蓋を経て橋延髄網様体へ向かうことが確認された。FA値・MD値・線維量に左右半球間の有意差はなかった(p>0.05)。
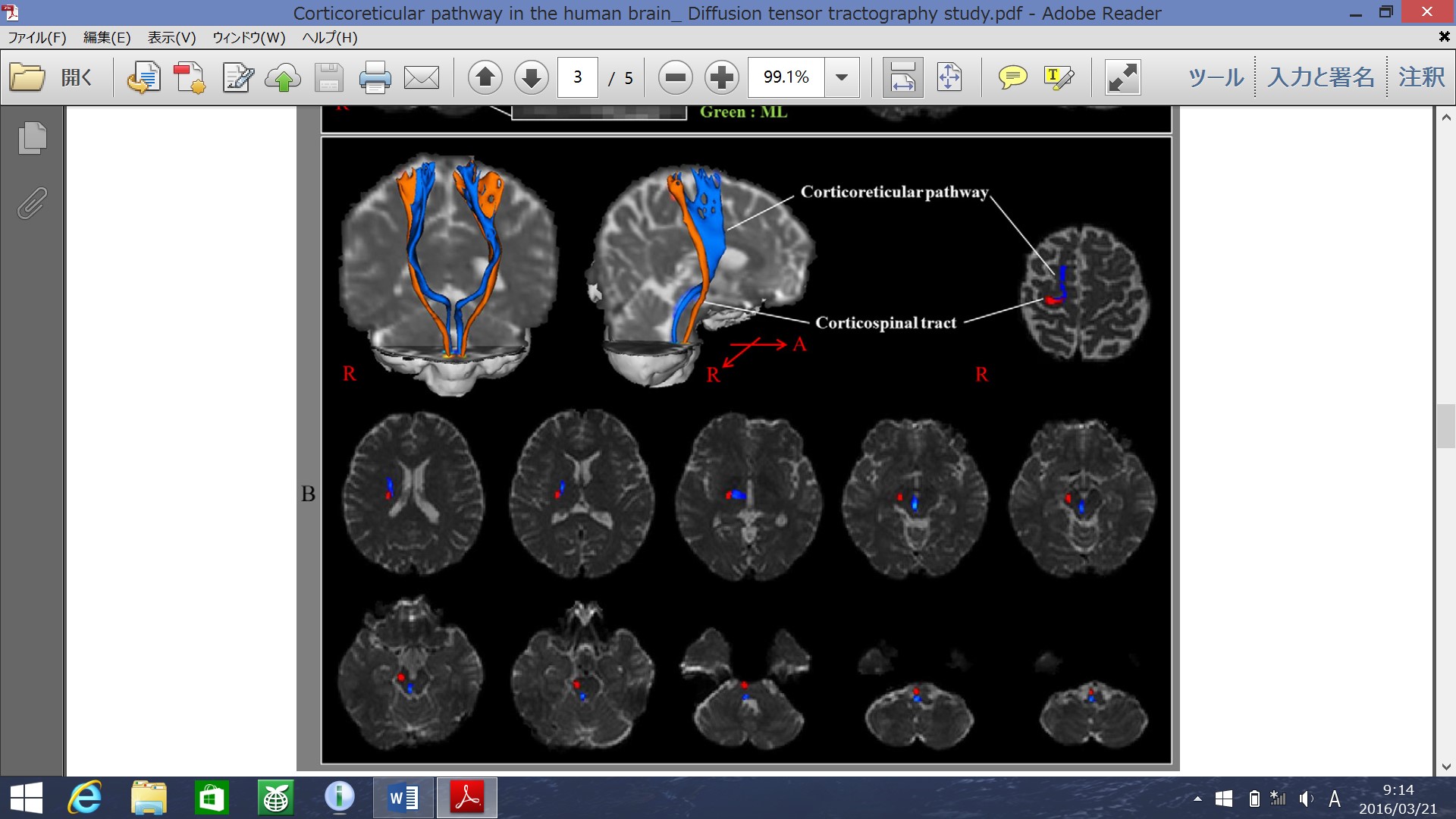
図:32歳男性の皮質網様体路(青)と皮質脊髄路(赤)の経路(Yeo SS et al. 2012より)
💡 臨床への含意
中大脳動脈領域の脳梗塞患者では、CSTが直接障害されなくても、その前内側を並走するCRTが内包・放線冠レベルで損傷されると姿勢制御障害・移動能力低下をきたす。臨床的にCSTが比較的保たれているにもかかわらず姿勢制御が著しく障害されている場合は、CRT損傷の可能性を画像所見(放線冠・内包後脚の前内側部)と照合して評価することが重要。
論文② 皮質脊髄路における体幹筋の神経学的結合の存在
🎯 背景・目的
一次運動野内では「remote effect(ある部位の興奮が隣接部位に波及する現象)」が知られている。体幹筋の収縮が上下肢の皮質脊髄路興奮性(MEP)にどの程度影響するかを明らかにした。
📊 結果・含意
体幹筋(腹直筋)収縮中に上肢・下肢筋のMEPが有意に増大した。体幹筋は一次運動野内で「四肢への興奮波及のハブ」として機能する可能性が示された。逆に体幹筋自体は他筋のremote effectを受けにくかった。上肢筋収縮時も体幹筋MEPがわずかに増大し、上肢-体幹間の双方向的な関係が示唆された。
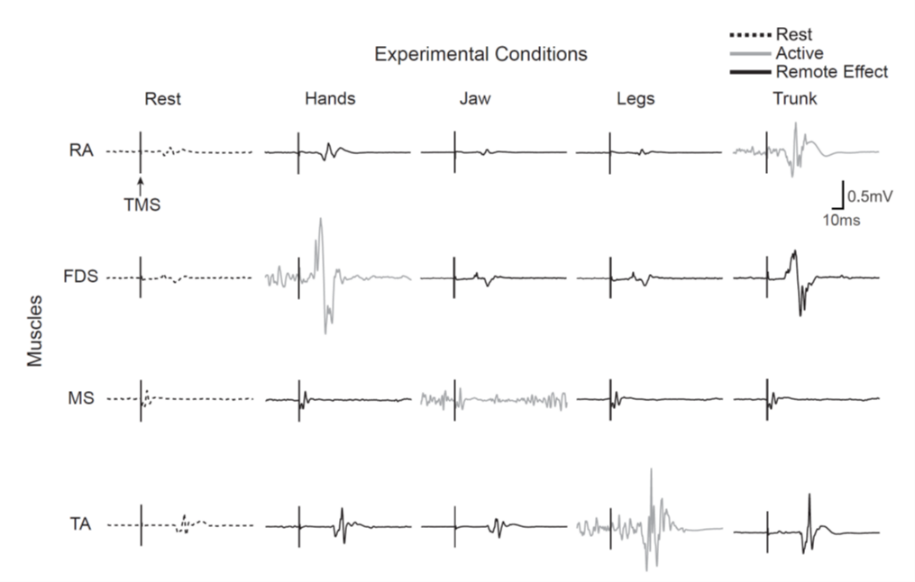
体幹筋収縮時の上下肢MEP増大(1.6MT刺激)
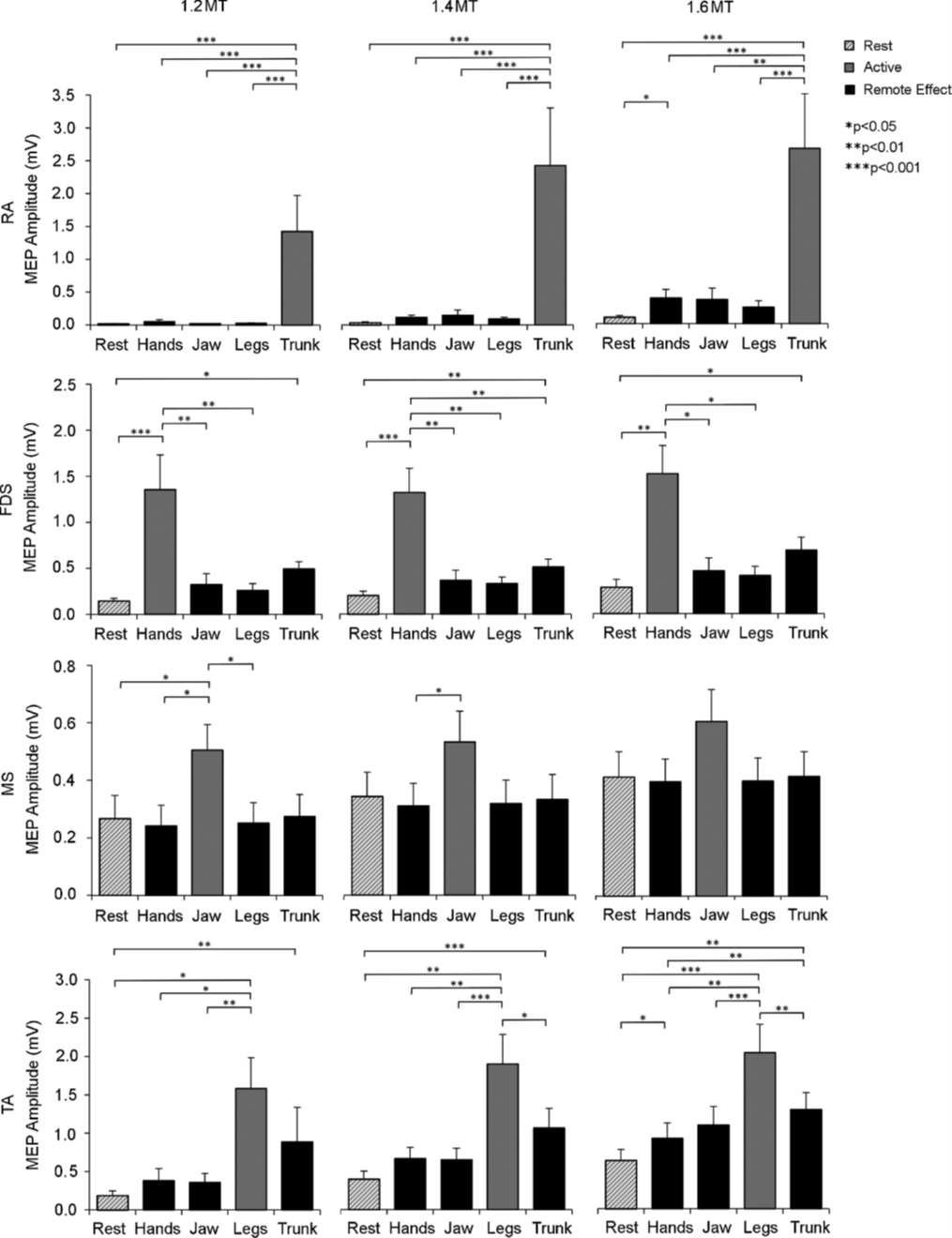
体幹筋収縮時のremote effectが最大(Sasaki et al. 2018)
本研究は健常者での結果であり、脳卒中患者での直接的な検証はさらに必要です。ただし「体幹筋の先行活性化が上下肢の皮質脊髄路興奮性を高める」という原理は、臨床的な体幹先行訓練(立ち上がり前の骨盤前傾・体幹安定姿勢の確保)の神経学的根拠として参照できます。
論文③ CST損傷後のRST代償的シナプス形成(Zaaimi et al. 2012)
🎯 背景・目的
CST損傷後に残存する運動機能を支える神経基盤として、RSTの役割を電気生理学的に明らかにすることを目的とした。
📊 結果
CST損傷後、通常はほとんど存在しないRST起源の手の運動ニューロンへの単シナプス接続(monosynaptic connections)が新たに形成されることが確認された。この変化は損傷後数週間で観察され、損傷後の行動回復の時期と一致していた。
💡 臨床への含意
脳卒中後のある程度の手機能回復はRSTを介した代償的シナプス可塑性が寄与している可能性がある。ただしこのRST代償は精細な指の独立運動(独立した屈曲など)は担えず、粗大な把握動作の回復に限定される。これは「脳卒中後に粗大把握はある程度回復するが、精細なつまみ動作の完全回復が難しい」という臨床経験の神経学的根拠のひとつ。早期からの集中的・反復的な上肢訓練がRST可塑性を促進する可能性がある。
論文④ 運動前野損傷が脳卒中後の移動能力回復に与える影響(Miyai et al. 2003)
🎯 背景・目的
運動前野(PMC/SMA)はCRTの起始部として姿勢制御・近位筋の協調運動に重要とされる。運動前野を含む病変を持つ脳梗塞患者と含まない患者で、移動能力・股関節機能の回復を比較した。
📊 結果・含意
運動前野の損傷を含む脳梗塞患者は、含まない患者と比較して股関節機能・移動能力の回復が有意に不良であった。これはCRT(皮質網様体路)の起始部である運動前野の損傷が、RSTへのトップダウン制御を損ない、姿勢・歩行機能の回復を妨げることを示している。Yeo et al.(2012)がDTIでヒトのCRTの走行を同定したこととあわせると、内包・放線冠レベルでのCRT損傷評価が予後予測に重要であることが示唆される。
リハビリテーションへの応用 ― 網様体系を考慮したアプローチ
🔑 神経系路を意識したリハビリ設計の基本原則(修正版)
① 内側RST亢進への対応(痙縮・シナジー管理):ポジショニング・ハンドリングで近位屈筋を短縮位に置かない。肩の骨頭位置を正しく保つFES(棘上筋・三角筋後部)や適切なスリング使用が将来の痙縮悪化・亜脱臼を予防。痙縮評価にはTardieu Scaleを活用し、神経性痙縮と拘縮を区別して介入を設計する。
② 体幹筋の先行活性化(remote effectの活用):Sasaki et al.(2018)の知見から、上下肢訓練前に体幹筋を先行活性化させることで一次運動野の興奮性を高め、より効率的な運動学習が得られる可能性がある(健常者での研究結果であり、脳卒中患者への直接応用は慎重に)。
③ CST・RST両方の活性化:意識的(CST)と自動的(RST)のシステムをバランスよく活用。初期段階では意識的動作制御から、習熟とともに自動的制御(RST主体)への移行を促す。
④ 課題反復によるRST可塑性の促進:Zaaimi et al.(2012)の知見から、反復的な課題指向型訓練がRSTの代償的シナプス形成を促進する可能性がある。粗大把握から精細把握への段階的訓練がCST回復とRST代償の両方を活用する。
⑤ 感覚フィードバック:神経回復には感覚フィードバックが不可欠。視覚・触覚・固有感覚のフィードバックを組み合わせ、患者が自己の姿勢・動きを認識できる環境を整える。
段階的リハビリプログラム
ポジショニングと痙縮管理(内側RST亢進への対応)
内側RST亢進による筋緊張を抑制するため、患側上肢は肘伸展・前腕回外位・手関節背屈位でのポジショニングを徹底。FESで棘上筋・三角筋後部を賦活し、骨頭求心圧を維持(亜脱臼予防)。温熱療法(ホットパック)+ CPM(肘・手関節)で筋・結合組織の粘弾性を改善。Tardieu ScaleでR2-R1を評価し、神経性痙縮が主体と判断された場合はボツリヌス毒素(BTX-A)治療の主治医への相談も検討。
体幹安定化と姿勢制御の再学習(CRT/RST機能の賦活)
座位での重心移動訓練・体幹回旋訓練でRSTの自動的姿勢制御機能を活性化。骨盤前傾誘導(体幹コア先行活性化)の後に上肢プレーシング訓練を行い、remote effectを活用した運動学習効率の向上を図る(Sasaki et al. 2018)。CRT損傷が疑われる場合(画像上の放線冠・内包後脚前内側部の病変)は姿勢制御の改善に長期を要することを家族・チームに説明する。
動的バランス・歩行訓練(内側RST・延髄RST・CSTの協調再学習)
バランスボード・不安定面でのトレーニングでRST・VST協調を高める。体幹を意識した歩行訓練(麻痺側傾斜のフィードバック付き)。ステップ台訓練で遊脚期の屈曲シナジー制御を練習。PNFの対角パターン(D2屈曲→D1伸展など)で体幹-四肢の協調運動を強化。VST過活動による伸展スパズムが歩行に影響する場合は、肩外旋・前鋸筋訓練・下肢AFO(短下肢装具)の活用を検討。
課題指向型訓練・上肢機能回復(RST可塑性の促進)
Zaaimi et al.(2012)の知見から、反復的な課題指向型訓練がRSTの代償的シナプス形成を促進する可能性がある。粗大把握動作(コップを持つ・ドアノブを回すなど)からの反復訓練を集中的に行う。CIMT(健側抑制・患側集中使用)も並行して検討。FES(機能的電気刺激)を伴う訓練が皮質レベルの再組織化をより効果的に促進する可能性がある。精細なつまみ動作の完全回復は難しいが、粗大把握の実用的な回復を目指す。
日常生活への統合とセルフケア指導
立ち上がり・調理・洗面など日常生活動作(ADL)を実際に練習し、CST(随意)とRST(自動)の協調を生活の中で統合。退院後のセルフケアとして自己ストレッチ(拘縮予防)・ポジショニング方法・患側使用の促進を指導する。RST亢進が続く場合、夜間のスプリント使用・定期的な医師への評価(BTX-A再投与時期の確認)も重要。
新人療法士のための10のチェックポイント
| チェックポイント | 主な経路 | 臨床への応用 |
|---|---|---|
| 橋RST(内側)の本来の役割を理解する | 橋RST(内側) | 本来は体幹・伸筋を興奮させる経路。脳卒中後に「屈曲シナジー」が出るのはCST消失との複合メカニズム |
| 網様体脊髄路(RST)の姿勢制御機能 | RST全般 | 自動的・習慣的な姿勢保持の主役。訓練では意識的制御から自動制御への移行を促す |
| 脊髄内介在ニューロンの役割 | Ia相反抑制・Renshaw | CST損傷後の介在ニューロン機能不全が痙縮・共同収縮の一因。PNFなどで相反抑制を引き出す |
| 体幹筋の協調性重視 | CRT+RST | 腹筋・背筋・側腹筋がバランスよく動くことが姿勢制御の前提。体幹先行活性化を訓練に組み込む |
| 痙縮評価スケールの使い分け | 伸張反射ループ | MASは簡便、Tardieu Scaleは神経性痙縮と拘縮の区別に優れる。BTX-A適応判断にはTardieuが重要 |
| 段階的な負荷調整 | 全経路 | 急激な負荷・過度な刺激は痙縮・筋緊張増加を招く。患者の状態に応じて難易度調整 |
| バランス訓練の積極実施 | RST+VST | 不安定面トレーニングでRST・VST協調を高め、体幹安定性向上 |
| RST可塑性を促進する反復訓練 | 橋RST(代償可塑性) | 集中的・反復的な課題指向型訓練がRST代償シナプス形成を促進する可能性(Zaaimi 2012) |
| 画像所見とCRT走行の照合 | CRT | 内包後脚前内側部・放線冠の病変があればCRT損傷を疑い、姿勢制御回復の予後を慎重に評価 |
| 他の下行路との統合 | RST+VST+赤核脊髄路 | 複数の経路を統合的に考慮した訓練で効果的な機能回復が期待できる |
症例検討 ― 網様体脊髄路を考慮したリハビリ計画
📋 症例:田村さん(70歳・男性)右中大脳動脈梗塞 発症3ヶ月
発症時NIHSS 13点(左上下肢麻痺・構音障害・軽度失語)。MRIで右内包後脚〜放線冠の梗塞(CRT走行経路に一致)。回復期リハ病院に転院。現在は杖歩行可能だが歩行時の体幹傾斜・ふらつきが顕著。上肢は屈曲-内転-回内シナジー(肘角度約70〜80度で固定傾向)。患側肩は内旋位で固まりつつあり、Tardieu Scale で R2(V3時)105度、R1(V1時)85度 → R2-R1=20度 → 神経性痙縮優位と判断。Modified Ashworth Scale(肘屈筋)2点。
神経学的評価と網様体系の関与の分析
| 観察所見 | 推定される神経メカニズム | 関連する経路・介入の根拠 |
|---|---|---|
| 肘屈曲・前腕回内位固定 | 橋RST代償亢進による近位筋過剰バイアス+Ia相反抑制低下 | med-RST過興奮。CSTのIa介在ニューロン制御消失 |
| 肩の前方突出・内旋固縮 | VST過活動 + 上腕二頭筋長頭高トーヌス | lat-VST過活動。FES・ポジショニングの適応 |
| 肘伸展時のキャッチ(Tardieu R2-R1=20°) | Ia伸張反射閾値低下(神経性痙縮優位) | 伸張反射ループ再構築。BTX-A適応検討の根拠 |
| 歩行時の体幹傾斜・ふらつき | CRT損傷(内包後脚前内側部)→RST姿勢フィードフォワード機能低下 | MRI所見と一致。体幹安定化訓練の優先度高 |
| 遊脚期の分回し歩行 | 延髄RST/CSTによる屈曲シナジー精細制御の喪失 | 歩行訓練の優先事項。AFO適応検討 |
| 患側使用時の連合反応 | RSTの両側投射的性質による異常拡散+辺縁系連絡 | 努力量コントロール・リラクゼーション環境の整備 |
Phase別リハビリ治療計画
Phase 1(1〜2週):ポジショニングと痙縮評価・管理
患側上肢は肘伸展・前腕回外・手関節背屈位でのポジショニングを徹底。FES(棘上筋・三角筋後部)で骨頭求心圧を維持(亜脱臼予防)。温熱療法+CPM(肘・手関節)で筋・結合組織の粘弾性を改善。Tardieu ScaleでR2-R1=20度(神経性痙縮優位)を確認 → 主治医にBTX-A(上腕二頭筋・肩甲下筋・大胸筋)の適応を相談。
Phase 2(2〜4週):体幹安定化とCRT/RST機能の賦活
座位での重心移動訓練・体幹回旋訓練でRSTの自動的姿勢制御機能を活性化。骨盤前傾誘導後に上肢プレーシング訓練(remote effectの活用)。CRT損傷(内包後脚前内側部)の画像所見と一致した症状であることをチームで共有し、体幹・近位機能の回復に時間を要することを家族に説明。立ち上がり訓練(体幹前傾先行・股関節主導パターン)を開始。
Phase 3(4〜8週):歩行訓練と動的バランスの向上
バランスボードでの動的訓練でRST・VST協調を高める。体幹意識型歩行訓練(鏡・視覚フィードバック使用)。ステップ台訓練で遊脚期制御を練習。AFO(後足部制動型)の試用で尖足・分回し歩行を改善。PNFの対角パターン(D1伸展 → D2屈曲など)で体幹-四肢協調を強化。BTX-A投与2〜4週後に痙縮再評価し、訓練強度を段階的に上げる。
Phase 4(8週以降):上肢課題指向型訓練とADL統合
Zaaimi(2012)の知見に基づき反復的な課題指向型上肢訓練(コップを持つ・タオルを絞る・ドアノブを回すなどの粗大把握動作から)を集中的に実施。CIMT(健側抑制・患側集中)の導入を検討。精細なつまみ動作の完全回復は難しいことを患者・家族に説明し、実用的な粗大把握動作の自立を現実的な目標として設定。退院後のセルフケア(ポジショニング・自己ストレッチ・BTX-A定期評価)の指導を行う。
リハビリを受けた方の声
「なぜ腕が曲がったまま固まるのか、なぜ体幹が安定しないと手が動かせないのか」、STROKE LABのセラピストさんが神経の経路を図で説明してくれてやっと理解できました。「体幹から治す」という方針の意味が分かってからは、リハビリに積極的に取り組めるようになりました。
70代男性・右中大脳動脈梗塞 発症後5ヶ月
退院後しばらく家で過ごしていたら腕がどんどん固くなってきて怖くなりました。STROKE LABで「MRI画像でこの経路が損傷されている」と具体的に説明を受け、ポジショニングや定期的な評価の大切さを知りました。主治医にボツリヌス治療も相談でき、痛みも少しずつ改善しています。
60代女性・左中大脳動脈梗塞 発症後8ヶ月
よくある質問(FAQ)
網様体脊髄路と皮質脊髄路(錐体路)はどう違いますか?
皮質脊髄路(CST):大脳皮質から脊髄運動ニューロンへ直接投射し、随意的・精細な運動(特に遠位四肢・手指の細かな動き)を担います。また脊髄内の介在ニューロン(Ia相反抑制系・Renshaw細胞)を制御し、スムーズな筋活動の調整も行います。
網様体脊髄路(RST):脳幹の網様体から脊髄へ投射し、自動的・反射的な姿勢制御(体幹の安定・抗重力維持・歩行リズム)を担います。橋RST(内側)は主に体幹・伸筋へ、延髄RST(外側)は主に屈筋系へ興奮性入力を行います。
臨床的には、脳卒中でCSTが損傷されると精細な随意運動が失われ、RSTが上位制御を失って過剰になります。リハビリテーションでは「CSTの残存機能の回復」と「RSTを介した代償的回復」の両方を目標とします。
「痙縮」と「網様体脊髄路」はどのように関係していますか?
正常では、大脳皮質はCRT(皮質網様体路)を通じてRSTへのトップダウン制御を供給し、また脊髄内のIa相反抑制介在ニューロン・Renshaw細胞を調整することで適切な筋緊張バランスを維持しています。脳卒中でCST・CRTが損傷されると、①RSTへのトップダウン制御が消失→RSTが脱抑制 ②脊髄介在ニューロン(Ia相反抑制など)の機能不全→伸張反射閾値の低下 が生じ、痙縮状態が形成されます。
評価と治療:Tardieu Scale(速度依存性評価)で神経性痙縮の程度を評価し、ボツリヌス毒素(BTX-A)治療と組み合わせたリハビリが標準的なアプローチです。BTX-Aは末梢の神経筋接合部に作用するため中枢のRST亢進自体には作用しませんが、過剰な末梢収縮を抑制することで運動学習の機会を増やします。
「体幹訓練が手や足の回復にも良い」というのは本当ですか?
ただし重要な注意点として、この研究は健常者でのデータであり、脳卒中患者で同様の効果が出るかどうかの直接的な検証はさらに必要です。
臨床的に参考になる点:
① 立ち上がり訓練前に骨盤前傾で体幹筋を活性化させると、下肢の皮質脊髄路興奮性が高まり動作が行いやすくなる可能性
② 上肢の精細訓練前に体幹安定姿勢を確保することで、より効率的な運動学習の機会をつくる
「体幹をコアとした統合的リハビリ」という考え方は、この神経科学的知見と整合するものです。
脳幹梗塞・小脳梗塞では網様体脊髄路は特にどう影響しますか?
橋病変:内側RST(橋起始)が障害 → 抗重力・姿勢保持機能が著しく低下。体幹低緊張・体幹失調が主体となる場合がある。NIHSSでは低スコアでも機能障害が深刻なケースが多い(後方循環系のNIHSS過小評価問題)。
延髄病変(Wallenberg症候群):外側RST(延髄起始)の障害 + 嚥下・感覚・自律神経中枢への影響が主体。HINTS試験が鑑別に有用。
小脳病変:小脳→網様体への出力(小脳-網様体路)が障害されることで、RSTを介した協調制御が乱れ、体幹失調・測距異常・企図振戦が生じます。小脳-橋RSTループの機能不全が体幹失調の主要因のひとつです。
これらの病変では、大脳皮質の病変とは異なるリハビリアプローチが必要であり、後方循環系病変に精通した専門家への相談が重要です。
「連合反応」が出るのも網様体脊髄路と関係していますか?
正常では、CSTが脊髄介在ニューロンを精細に制御することで運動は目的の筋のみに限局されます。脳卒中後にCSTが損傷されると、RSTの両側投射的性質により健側での運動時に患側の運動ニューロンも活性化されてしまうことが連合反応の神経学的基盤のひとつと考えられています(ただし完全には解明されていません)。
また、網様体系は辺縁系(感情系)と連絡があるため、不安・痛み・努力的課題などの情動変化も連合反応を増強させます(RSTと辺縁系連絡の臨床的現れ)。
臨床的には、連合反応を完全に消去しようとするのではなく、「努力量のコントロール」「リラクゼーション環境」「体幹安定化による過剰拡散の抑制」「健側運動強度の段階的調整」などを組み合わせて管理します。
「あくびをすると手が緩む」「咳をすると腕が曲がる」のはなぜですか?
「あくびで手が緩む」(推測されるメカニズム):あくびは延髄の呼吸中枢(網様体内)が関与する複合反射行動です。この際、呼吸中枢の活動が同じ網様体内の運動系に一時的な調整をもたらし、筋緊張が緩和されると考えられています。急性期に特に観察されやすい現象です。
「咳で腕が曲がる」(推測されるメカニズム):咳の際の腹圧増加・努力呼気が内側RSTへの刺激となり、近位屈筋のトーヌスが一時的に増大すると考えられています。
これらを臨床的に活用する試みとして、「呼気時に患側上肢を伸展する」「深呼吸とストレッチを同期させる」などのアプローチが一部の施設で行われていますが、エビデンスとしてはまだ臨床観察レベルです。「なぜそうなるか」の確立した神経生理学的説明は今後の研究課題でもあります。
ボツリヌス毒素(BTX-A)治療と網様体脊髄路の関係は?
しかし、臨床的な意義としては:
① 過剰収縮の軽減 → 運動学習の機会拡大:BTX-Aで拮抗筋(例:上腕二頭筋)の過剰収縮が抑制されると、患者が随意的に拮抗筋(例:上腕三頭筋)を動かす機会が増え、より効果的な運動学習とCSTの残存機能の活用が可能になります。
② 筋の構造変化の予防:持続的な痙縮による筋・結合組織の短縮・線維化(拘縮への移行)を予防します。
③ リハビリ効果の最大化:BTX-A投与後の2〜4週間が集中的なリハビリの「治療ウィンドウ」として重要です。
中枢のRST亢進に対するより根本的なアプローチとしては、CRT経路の神経可塑性を促進する「集中的なリハビリテーション」や「非侵襲的脳刺激(rTMS・tDCS)」が研究されていますが、現時点ではBTX-A+リハビリの組み合わせが標準的な管理法です。
参考文献・引用文献
- 1) Lawrence DG, Kuypers HG. The functional organization of the motor system in the monkey. I. The effects of bilateral pyramidal lesions. Brain. 1968;91(1):1-14. 【網様体脊髄路の機能的役割の古典的基礎研究】
- 2) Kuypers HGJM. Anatomy of the descending pathways. In: Brooks VB, editor. Handbook of Physiology. Bethesda: American Physiological Society, 1981:597-666. 【内側・外側RST(伸筋/屈筋)の古典的解剖学的記述】
- 3) Yeo SS, Chang MC, Kwon YH, Jung YJ, Jang SH. Corticoreticular pathway in the human brain: Diffusion tensor tractography study. Neurosci Lett. 2012;508(1):9-12. 【皮質網様体路のDTI同定。CSTの前内側を並走することを確認】
- 4) Yeo SS, Chang PH, Jang SH. The corticoreticular pathway and its role in normal walking. J Hum Kinet. 2013;38:205-214.
- 5) Sasaki A, Milosevic M, Sekiguchi H, Nakazawa K. Evidence for existence of trunk-limb neural interaction in the corticospinal pathway. Neuroscience Letters. 2018;668:31-36. 【体幹筋のremote effect・健常者TMS研究】
- 6) Zaaimi B, Edgley SA, Soteropoulos DS, Baker SN. Changes in descending motor pathway connectivity after corticospinal tract lesion in macaque monkey. Brain. 2012;135(7):2277-2289. 【CST損傷後のRST代償シナプス形成】
- 7) Baker SN. The primate reticulospinal tract, hand function and functional recovery. J Physiol. 2011;589(23):5603-5612. 【RSTと手機能・脳卒中後回復の総説】
- 8) Miyai I, Yagura H, Hatakenaka M, et al. Longitudinal optical imaging study for locomotor recovery after stroke. Stroke. 2003;34(12):2866-2870. 【運動前野損傷と移動機能回復への影響】
- 9) Matsuyama K, Mori F, Nakajima K, et al. Locomotor role of the corticoreticular-reticulospinal-spinal interneuronal system. Prog Brain Res. 2004;143:239-249.
- 10) Lance JW. The control of muscle tone, reflexes, and movement: Robert Wartenberg Lecture. Neurology. 1980;30(12):1303-1313. 【痙縮の定義(速度依存性の抵抗増大)の古典的文献】
- 11) Gracies JM. Pathophysiology of spastic paresis. I: Paresis and soft tissue changes. Muscle Nerve. 2005;31(5):535-551. 【神経性痙縮と筋・結合組織変化の区別。Tardieu Scale根拠】
- 12) Patrick E, Ada L. The Tardieu Scale differentiates contracture from spasticity whereas the Ashworth Scale is confounded by it. Clin Rehabil. 2006;20(2):173-182. 【Tardieu Scale vs MAS比較:神経性痙縮と拘縮の鑑別】
- 13) 金子唯史. 脳卒中の動作分析. 医学書院, 2018. 【経路図・姿勢制御の解説の主要参考文献】
- 14) 金子唯史. 脳の機能解剖とリハビリテーション. 医学書院, 2024. 【本記事の主要参考書】
網様体脊髄路を理解したら、
次は「どう臨床に活かすか」です。
痙縮・姿勢制御・歩行障害に悩む脳卒中後の方へ。
神経系路を考慮した個別リハビリプログラムをSTROKE LABでご相談ください。

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)