【2026年版】視床痛の治療・リハビリテーション方法:予後予測とMRI画像診断まで徹底解説
脳卒中後に発症する痛みの中で最も難治性かつ患者QOLへの影響が大きいのが視床痛(Thalamic Pain / 中枢性脳卒中後疼痛:Central Post-Stroke Pain, CPSP)です。「火がついたような灼熱感」「冷たいものが熱く感じる」「服が触れるだけで激痛が走る」という訴えはこの疾患の典型です。本記事では視床の解剖・機能から視床痛のメカニズム・評価・鑑別診断・薬物療法・神経刺激療法・リハビリテーション・日常生活の工夫まで、患者・家族・医療者が知るべきすべてを体系的に解説します。
▲ 視床痛・脳卒中後疼痛の予後予測について解説(STROKE LAB)
視床痛(Central Post-Stroke Pain:CPSP)は、脳卒中後に生じる神経障害性疼痛の一種で、歴史的には「Dejerine–Roussy症候群」と呼ばれていました。脳卒中患者の約8〜11%が発症し(Andersen et al. 1995; Sackley et al. 2013)、発症から数週間〜数か月後に疼痛が顕在化するケースが多く、急性期には見落とされがちです。正確には視床病変に限らず、脊髄視床路(spinothalamic tract)のいずれかの損傷によって生じる中枢性疼痛を指します。薬物療法・神経刺激療法・感覚統合リハビリを組み合わせた多角的アプローチが回復の鍵です。
- 正式名称:中枢性脳卒中後疼痛(Central Post-Stroke Pain: CPSP)。かつてはDejerine–Roussy症候群とも呼ばれた(1906年に初記載)
- 有病率:脳卒中患者の約8〜11%(Andersen et al. 1995; Sackley et al. 2013)。視床梗塞・視床出血ではさらに高率(25〜50%とも報告)
- 発症時期:脳卒中後1か月以内が最多だが、6か月以降に発症するケースも約20%存在(Klit et al. 2009)
- 原因:視床自体の損傷に限らず、脊髄視床路(STT)のいずれかの損傷に続発する中枢性疼痛。脳幹・皮質病変でも生じる
- 主症状:灼熱痛・電撃痛・アロディニア(触れるだけで痛い)・痛覚過敏・温度感覚異常(温冷の逆転)
- 診断:CPSP確定には①脳卒中後の疼痛発症②MRIで脊髄視床路に沿った病変③他原因の除外、の3条件をすべて満たすことが必要
- 第一選択薬:アミトリプチリン(TCA)・プレガバリン/ガバペンチン(Ca²⁺チャネルα₂δリガンド)。Finnerup et al. 2015のシステマティックレビューで推奨
- rTMS(反復経頭蓋磁気刺激):運動野刺激で中程度の疼痛軽減効果(Lefaucheur et al. 2014ガイドラインでB推奨)。顔面痛への有効性が特に報告される
- MCS(運動野皮質電気刺激:硬膜外):難治例で50〜70%が短期改善。DBSより選好されることが多い(Rasche et al. 2006)
- DBS(脳深部刺激療法):他の慢性疼痛と比べCPSPへの効果は限定的。短期的には一部の患者で有効(Owen et al. 2006)
- TENS:視床痛への効果は一定せず。一部で改善、一部で悪化も報告。慎重な適用が必要
- リハビリの原則:段階的感覚脱感作+運動療法+認知行動療法(CBT)の多角的アプローチ。単一療法では効果が限定的
視床の解剖と機能 ― 感覚の中継基地を理解する
▲ 視床の構造と機能について詳しく解説
視床(Thalamus)は脳の中央部、間脳に位置する左右一対の卵形の灰白質構造です。約3〜4cmの大きさで大脳皮質の直下に存在し、哺乳類では感覚・運動・認知のほぼすべての経路の「中継ハブ」として機能しています。
🧠 視床の解剖学的特徴
位置と形状
間脳の大部分を占める卵形の灰白質。左右一対で第三脳室を挟んで存在。視床間橋(massa intermedia)で連結されることがある
核の数と分類
約60の核(nucleus)に分割。腹側核群(VPL・VPM・VA・VL)・内側核群(MD)・前核群・板内核群(CM・PF)など。それぞれ固有の入出力を持つ
血液供給(痛みに関連)
傍正中動脈・視床膝状体動脈・後脈絡叢動脈が主な供給血管。視床膝状体動脈域(VPL・VPM)の梗塞がCPSPと最も強く関連する
感覚伝達の割合
嗅覚を除く感覚情報の大部分が視床を経由して大脳皮質へ伝達。視覚・聴覚・体性感覚・味覚すべてが通過する「感覚の関門」
視床の5大機能
🔬 視床の主要機能マップ
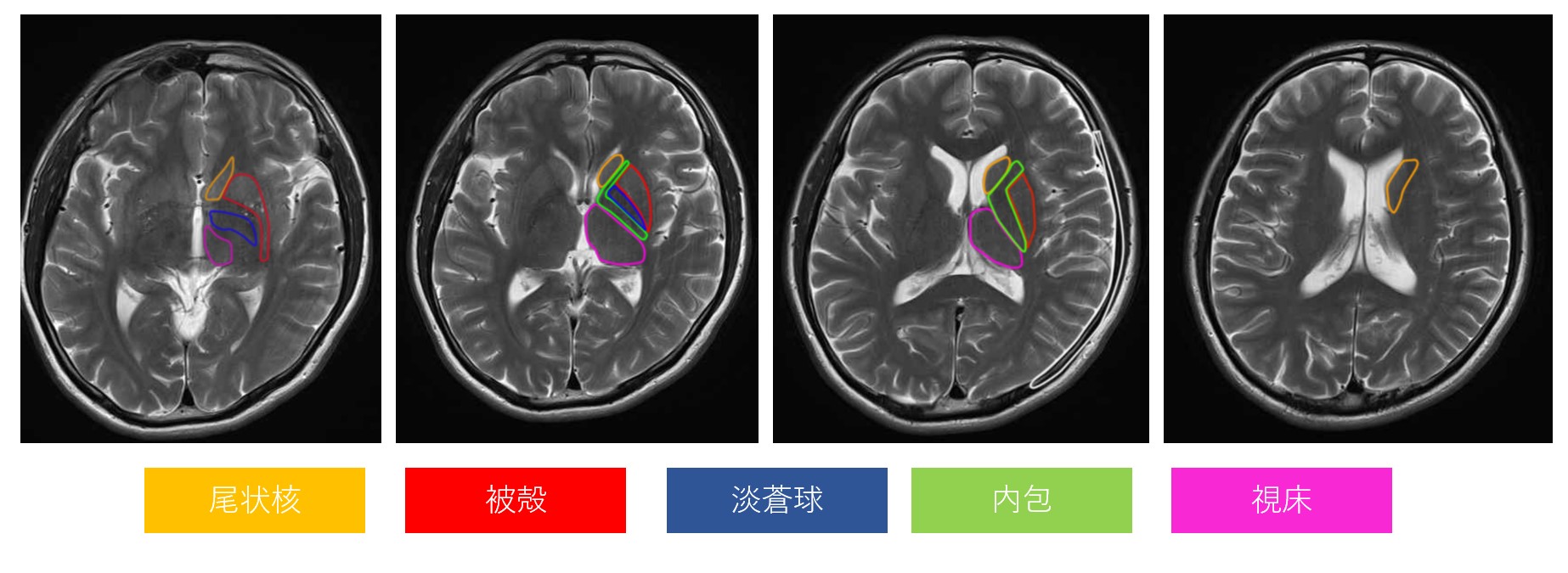
視床のMRI軸位断像。中央部の卵形構造が視床(引用:画像診断Cafe)
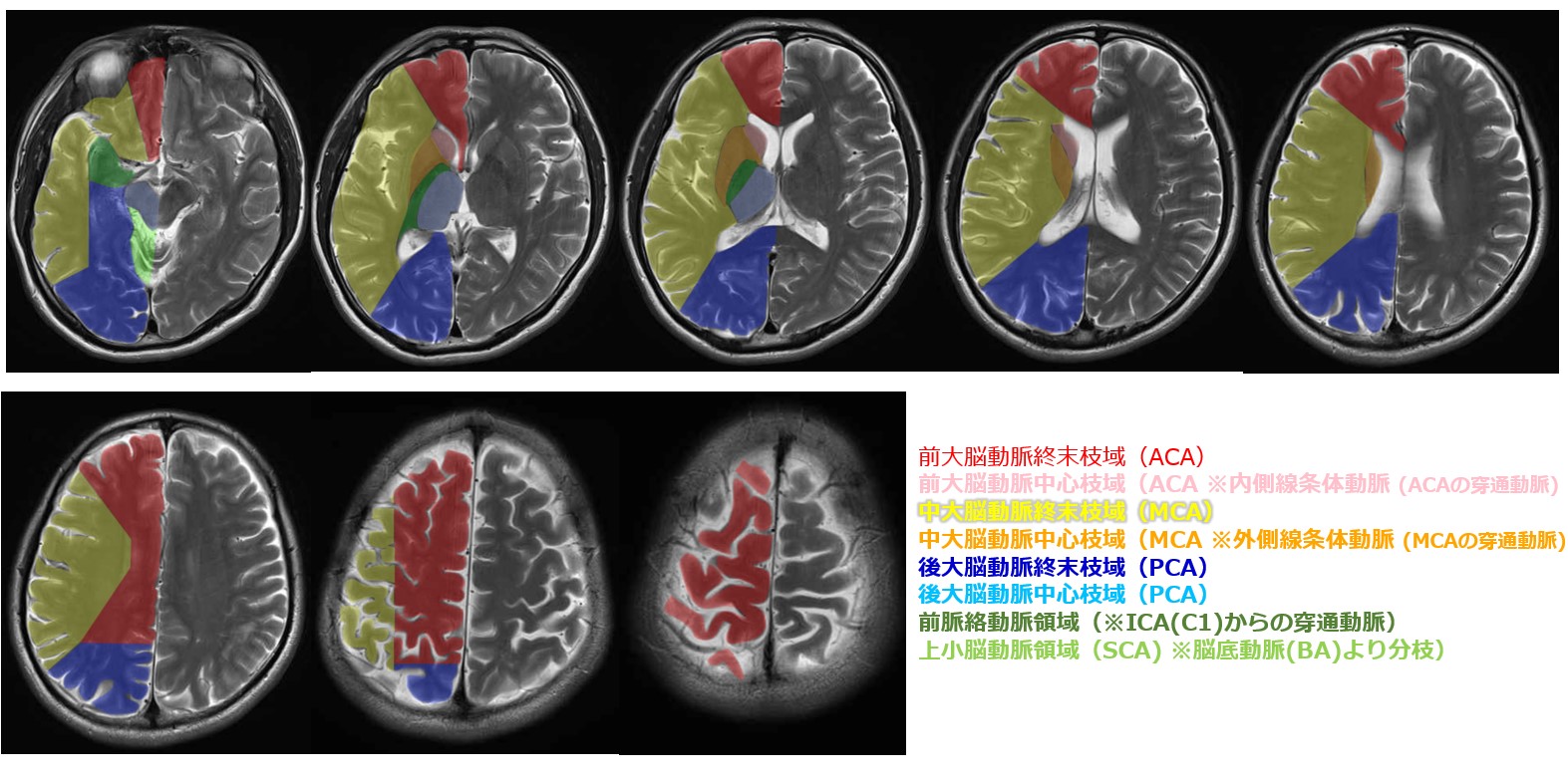
冠状断像で見る視床の位置(引用:画像診断Cafe)
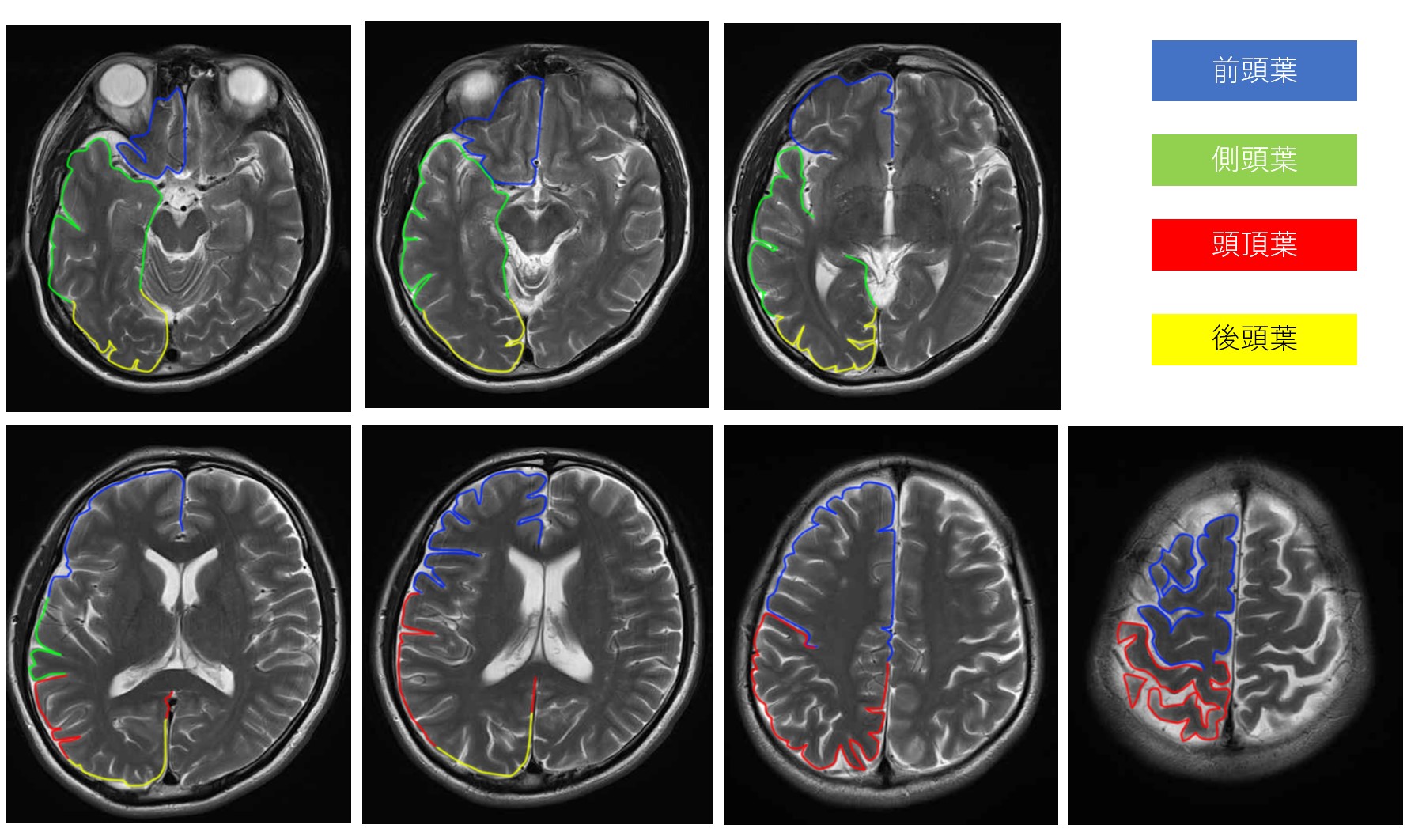
矢状断像で見る視床・脳幹の解剖学的関係(引用:画像診断Cafe)
視床痛とは何か ― 定義・有病率・リスク因子・発症経過
📖 「視床痛」の正式な定義と現代的な理解
「視床痛(Thalamic Pain Syndrome)」は1906年にDejerine・Roussyが初記載した歴史的名称です。現在は「中枢性脳卒中後疼痛(Central Post-Stroke Pain: CPSP)」として広く定義されており、視床病変に限定されず、脊髄視床路(spinothalamic tract: STT)のいずれかの損傷に続発する疼痛のすべてを含みます。
視床梗塞・視床出血が原因であることが多いですが、脳幹梗塞(外側延髄梗塞=Wallenberg症候群など)・放線冠の梗塞・頭頂葉病変でも同様のCPSPが生じます。「視床痛=視床病変に限る」という理解は誤りであることに注意してください。
有病率と発症時期
Sackley 2013(11%)
特に高頻度に発症
(Klit et al. 2009)
📊 発症時期の分布(Klit et al. 2009 のレビューより)
※図は概念的な比率を示しており、各研究で若干異なります。発症時期の分布はKlit H et al. (2009) Central post-stroke pain: clinical characteristics, pathophysiology, and management. Lancet Neurol. 8(9):857-68 を参考に作成。
CPSP(視床痛)のリスク因子
どんな患者がCPSPを発症しやすいか? ― リスク因子の整理
⚠️ 「急性期には気づかれにくい」という臨床上の落とし穴
CPSP(視床痛)の最大の臨床的特徴は、急性期(脳卒中発症直後)には疼痛が前景に立たず、数週間〜数か月後に疼痛が顕在化する発症パターンです。急性期は意識障害・麻痺・言語障害への対応に追われる中、疼痛の訴えが見落とされるケースが少なくありません。
「退院後に突然痛みが出始めた」「リハビリが進んでいるのに最近痛みが増している」という訴えは視床痛のサインである可能性があります。脳卒中後に新たな疼痛が出現した場合は、まずCPSPを鑑別診断の上位に置いてください。
視床痛のメカニズム ― 脳科学的視点から理解する
🔬 視床痛(CPSP)が発生するメカニズム(脊髄視床路の破綻モデル)
💡 「なぜ温度変化で痛みが変動するのか」を理解する
視床痛患者の多くが「寒い環境や冷たいものに触れると激痛が走る」と訴えます。これは温度感覚(熱さ・冷たさ)と痛覚が同じ脊髄視床路(外側脊髄視床路)を経由するためです。この経路が損傷されると、温度情報と痛覚信号の処理が混線し、温度刺激が疼痛として認識されます(温度誘発性疼痛:thermal allodynia)。
また、感情的ストレスや睡眠不足が疼痛を増強することも特徴です。これは扁桃体・前帯状皮質などの情動系脳領域が下行性疼痛促進系を活性化し、視床レベルでの疼痛信号を増幅するためと考えられています。痛み・不眠・抑うつの三重の悪循環がCPSPを難治性にする主要因の一つです。
専門家向け:CPSPの神経生物学的機序の詳細
脱抑制モデル(Disinhibition Model):Leijon・Bowsher(1989年)らが提唱した古典的モデル。外側脊髄視床路(感覚・温痛覚系)の損傷により、本来この経路が担っていた内側脊髄視床路(情動性疼痛系)への抑制が解除される。結果として内側系(視床内側核群:MD核・CM核)を介した情動性疼痛応答が過剰に活性化され、灼熱痛・不快感を特徴とするCPSPが生じるという考え方。
中枢性感作(Central Sensitization):視床の損傷後、通常は抑制性GABAニューロンによって制御されている視床感覚核(VPL・VPM)の神経細胞が過活動となる。自発発火・受容野拡大・閾値低下が生じ、通常痛みを生じない刺激(触覚・冷覚)が痛み信号として皮質へ伝達される(アロディニア)。
視床皮質振動の異常:健常な視床では8〜14Hzの睡眠紡錘波(sleep spindle)に代表される視床皮質リズムが存在する。CPSP患者では損傷後にこの正常なリズムが乱れ、低周波(δ帯域:1〜4Hz)の異常な同期バースト発火が生じることが報告されている(Lenz et al. 1989)。この異常リズムが慢性疼痛の維持に関与している可能性があり、rTMS・MCS(運動野皮質電気刺激)の作用機序のひとつとして「視床皮質振動の正常化」が提唱されている。
グリア細胞の関与:近年、ミクログリアの過活性化・神経炎症がCPSP病態の維持に寄与することが示されており(Zhao et al. 2017)、神経炎症を標的とした新たな治療戦略(TLR4阻害・ミクログリア調節)の研究が進行中。
視床痛の症状と評価方法
視床痛の特徴的な症状 ― 患者が「どう表現するか」
灼熱痛(Burning Pain)
「火がついたような」「熱湯をかけられたような」灼熱感。CPSPで最も多い訴え。持続性で夜間・安静時に増強することが多い
電撃痛・刺痛(Shooting / Stabbing Pain)
「電気が走るような」「針で刺されるような」鋭い痛み。突発的に生じ、数秒〜数分間持続することがある。動作や感覚刺激で誘発されやすい
アロディニア(Allodynia)
「服が触れるだけで激痛」「風が当たるだけで痛い」。通常は痛みを生じない軽い刺激で強い痛みが誘発される。触覚性・温度性アロディニアに分類
温度感覚異常(Thermal Dysesthesia)
「冷たいものが熱く感じる」「温かい湯で手が灼熱する」という温度感覚の逆転現象。体温変化・冷気・入浴で疼痛が変動する
感覚鈍麻との共存(感覚の矛盾)
痛覚・温度覚は過敏だが、識別感覚(触れているものの形・質感の識別)は鈍麻という「矛盾した感覚障害」が同一患者に共存する。CPSPの特徴的所見
情動・睡眠への二次的影響
慢性疼痛による抑うつ・不安・不眠・QOL低下が二次的に生じやすい。疼痛→不眠→情動障害→疼痛増悪の三重の悪循環が形成される
痛みの評価ツール ― 何を使ってどう評価するか
視床痛評価で使用される主要なスケールと手法
| 評価ツール | 評価内容 | 視床痛での主な用途 | 臨床的ポイント |
|---|---|---|---|
| VAS / NRS | 痛みの強さ(0〜10点) | 治療前後の変化モニタリング | 4点以上が臨床的に有意な疼痛の目安。毎セッションで記録 |
| DN4 | 神経障害性疼痛の有無(10項目) | CPSP vs 侵害受容性疼痛の鑑別 | 4点以上で神経障害性疼痛を示唆(感度83%・特異度90%) |
| painDETECT | 神経障害性疼痛のスクリーニング | 外来・在宅での初期評価 | 患者自記式で簡便。19点以上で神経障害性疼痛の可能性が高い |
| LANSS | 神経障害性疼痛の感覚検査も組み込む | DN4と並ぶ神経障害性疼痛スクリーニング | 12点以上で神経障害性疼痛の可能性(感度82%・特異度80%) |
| QST(定量的感覚テスト) | 温度・振動・機械的感覚の定量化 | 感覚経路の損傷部位・程度の精密評価 | 専門的設備が必要。温度閾値・機械的痛み閾値の測定でSTT損傷を確認 |
| BPI(簡易疼痛評価票) | 痛みの強さ+日常生活への影響 | QOL評価・長期フォローアップ | 「最強・平均・現在」の痛みと日常動作への影響を多面的に把握 |
診断基準・鑑別診断・画像所見
CPSP(中枢性脳卒中後疼痛)の診断に必要な3条件
国際疼痛学会(IASP)および複数のガイドラインでは、CPSPの診断に以下の3条件をすべて満たすことを求めています(Klit et al. 2009; IASP基準):
脳卒中後の疼痛発症(発症時期の確認)
疼痛が脳卒中の後に新たに出現したこと。多くは発症後6か月以内に顕在化するが、それ以降の発症も否定しない。急性期からの疼痛は痛覚過敏として始まり、遷延するケースも存在する
MRI(またはCT)で脊髄視床路に沿った血管病変の確認
MRIのDWI・T2/FLAIR像で視床、脳幹(外側延髄など)、または大脳皮質・放線冠などの脊髄視床路沿いの病変が確認されること。病変の場所と症状分布の解剖学的整合性を確認することが重要。梗塞サイズが大きいほど予後が悪い傾向がある
他原因の除外
筋筋膜性疼痛・整形外科疾患・複合性局所疼痛症候群(CRPS)・肩手症候群・末梢神経障害・帯状疱疹後神経痛など他の疼痛疾患が症状の主原因でないことを積極的に除外する
鑑別診断 ― 見落とされやすい類似疾患
| 比較項目 | 視床痛(CPSP) | CRPS(複合性局所疼痛症候群) | 肩手症候群 | 末梢神経障害性疼痛 |
|---|---|---|---|---|
| 原因・機序 | 脊髄視床路の中枢性損傷 | 末梢神経・交感神経の異常 | 肩関節拘縮+浮腫。脳卒中後に多い | 末梢神経の直接損傷(糖尿病等) |
| 疼痛の分布 | 病変対側の半身(顔面〜体幹〜四肢) | 特定の四肢(手・足)に限局 | 肩〜手部に限局 | 末梢神経支配域に沿った分布 |
| 自律神経症状 | 通常なし | 著明(発汗・浮腫・皮膚色調変化) | 手部浮腫・皮膚光沢変化 | 軽度(糖尿病性では発汗障害等) |
| MRI所見との対応 | 脊髄視床路沿いの血管病変で説明可能 | 脳病変との直接対応なし | 脳病変との直接対応なし | 末梢神経の問題(脳病変と独立) |
| 温度感覚の逆転 | ✅ 特徴的(冷刺激→灼熱痛) | △ 局所温度変化はあるが逆転は少ない | ❌ 通常なし | △ 糖尿病性では末梢の温感低下 |
| 治療の方向性 | 抗けいれん薬・TCA・rTMS・感覚統合リハビリ | ステロイド・交感神経ブロック・CRPS専用リハビリ | 肩関節可動域訓練・浮腫管理 | 原疾患治療+神経障害性疼痛薬 |
⚠️ 肩手症候群・CRPSとCPSPの合併に注意
脳卒中後にはCPSP・肩手症候群・CRPSが同一患者に合併することがあります。「麻痺側の肩〜手部の疼痛」という主訴では、これらを区別しないまま対応すると治療が的外れになります。肩手症候群は肩関節拘縮・手部浮腫を合併し、関節可動域訓練で改善することが多い一方、CPSPは感覚系の中枢障害であり、過度な物理的刺激で逆に増悪することがあります。感覚検査(温度覚・痛覚の分布)・MRI所見・自律神経症状の有無で丁寧に鑑別してください。
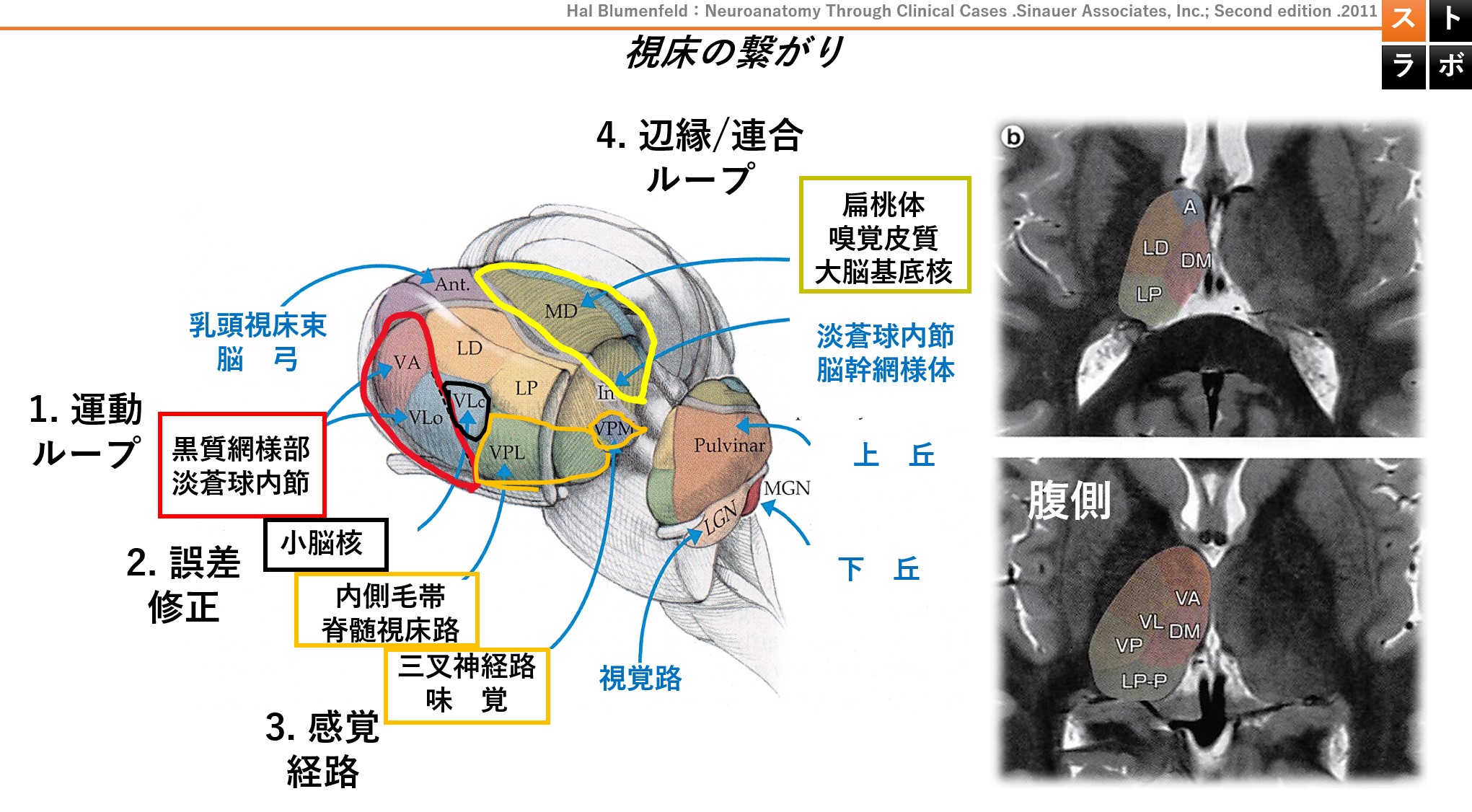
視床梗塞のMRI所見。VPL・VPM核周辺の病変がCPSPの主原因となる
治療アプローチ ― 薬物・神経刺激・外科的治療
💡 視床痛(CPSP)治療の大原則:段階的・多角的アプローチ
CPSPは単一の治療法で完全解決することが難しい難治性疾患です。IASP・日本ペインクリニック学会・Finnerup et al.(2015)のシステマティックレビューでは、薬物療法(第一選択)→ 神経刺激療法(第二選択)→ 外科的治療(最終選択)を段階的に適用し、いずれのフェーズでも心理的アプローチとリハビリテーションを並行させることが推奨されています。
「痛みをゼロにする」ことより「痛みの強さを下げ日常生活への影響を最小化する」ことを現実的な治療目標として患者・家族と共有することが重要です。
第一選択:薬物療法
三環系抗うつ薬(TCA)のアミトリプチリン(amitriptyline)は、CPSP治療で最も強いエビデンスを持つ薬剤です(Leijon & Boivie 1989のRCT;Finnerup et al. 2015)。ノルアドレナリン・セロトニンの再取り込みを阻害して下行性疼痛抑制系を強化し、中枢性感作を抑制します。低用量(10〜25mg/日)から就寝前投与で開始し、副作用(口渇・眠気・便秘・起立性低血圧)を確認しながら漸増します。
SNRIのデュロキセチン(duloxetine)は副作用プロファイルが改善されており、心疾患・前立腺肥大合併例でアミトリプチリンが使用しにくい高齢者での代替薬として選択されます。
プレガバリン(pregabalin)・ガバペンチン(gabapentin)は電位依存性カルシウムチャネルのα₂δサブユニットに結合し、神経終末からの興奮性神経伝達物質(グルタミン酸・サブスタンスP)の過剰放出を抑制します。視床の中枢性感作を末梢・脊髄・脳幹の複数レベルで抑制します。低用量から開始し副作用(眠気・めまい・浮腫・体重増加)を確認しながら漸増。効果発現まで2〜4週間かかるため、焦って中止しないことが重要です。
難治性CPSPで第一選択薬が不十分な場合、トラマドール(弱オピオイド)が補助的に使用されます。トラマドールはオピオイド受容体への作用に加えノルアドレナリン再取り込み阻害効果も持ち、神経障害性疼痛に対して一定の有効性が示されています(エビデンスB)。強オピオイド(モルヒネ・オキシコドン)は依存・耐性・認知機能への悪影響リスクがあるため、CPSP での長期使用は特に慎重に行います。
第二選択:神経刺激療法
⚠️ 重要な訂正:「TMS 77%成功率」の正確な出典について
一部の文献では「TMS(経頭蓋磁気刺激)で最大77%の成功率」と記載されることがありますが、この数字の原著はRasche et al.(2006, Pain)であり、実際には「MCS(Motor Cortex Stimulation:硬膜外運動野皮質電気刺激)」の報告です。TMSとMCSは異なる手技です。MCSは開頭により硬膜外に電極を留置する侵襲的な手術であり、外来で実施するrTMS(経頭蓋磁気刺激)と混同しないことが重要です。rTMSのCPSPへの有効性は「中程度の改善」レベル(Lefaucheur et al. 2014ガイドラインでLevel B推奨)であり、77%という高い数字はrTMSのものではありません。
反復経頭蓋磁気刺激法(rTMS)― 非侵襲的・外来実施可能
反復TMS(rTMS)は頭皮上から磁場パルスを与えて運動野(M1)の神経活動を調整します。1Hz(抑制的)または10Hz以上(促進的)の刺激を使い分け、運動野を介して視床皮質回路の異常なリズムを正常化することで疼痛を緩和すると考えられています。CPSP(中枢性脳卒中後疼痛)に対して4〜8週間の継続施術で中程度の疼痛軽減効果が報告されており(Lefaucheur et al. 2014)、特に顔面痛への有効性が文献で強調されています。ただし効果の持続期間は限定的であり、維持療法が必要になることが多いです。
硬膜外運動野皮質電気刺激(MCS)― 難治例に有効性が高い侵襲的手術
硬膜外MCS(Motor Cortex Stimulation)は開頭手術によって硬膜外腔に電極を留置し、運動野を持続的に電気刺激する方法です。Rasche et al.(2006)の報告では、難治性神経障害性疼痛患者(CPSPを含む)の50〜70%で短期的な疼痛軽減が得られました。DBSと比較して手術リスクが低く、CPSPへの反応性が良好であることから、CPSPの外科的治療としてMCSがより選好される傾向にあります。
「TMS(経頭蓋磁気刺激)」は頭皮上から非侵襲的に実施する外来手技。「MCS(運動野皮質電気刺激)」は開頭して硬膜外に電極を埋め込む外科的手術。同じ「運動野刺激」という概念でも、侵襲性・効果の強さ・適応が大きく異なります。50〜70%の成功率はMCS(外科的)のデータです。
脊髄刺激法(SCS)・脳深部刺激療法(DBS)
DBS(脳深部刺激療法)は視床・視床下部に電極を埋め込む高度侵襲的手術です。他の慢性疼痛(パーキンソン病の振戦・ジストニアなど)への有効性と比べ、CPSPへのDBSは効果が限定的とされています(Owen et al. 2006)。薬物療法・MCSが無効な場合の最終選択肢として検討されます。SCS(脊髄刺激法)は脊髄損傷後疼痛には有効性が示されていますが、脳卒中後CPSPへの適応はエビデンスが限定的です。
リハビリテーション ― 感覚統合・運動・心理的アプローチ
▲ STROKE LABにおける視床痛患者への介入動画(実際のリハビリ場面)
▲ 視床痛・中枢性疼痛への介入アプローチ実例
🏃 リハビリテーションの3本柱とその根拠
① 感覚統合訓練(脱感作・再感作):過敏な感覚系を段階的に「正常化」する訓練。痛みを誘発しない軽度な刺激から始め、神経可塑性を利用して感覚処理の再編成を促す。感覚皮質レベルでの体性感覚マップの正常化が目標。
② 運動療法(神経可塑性の促進):運動は内因性オピオイド放出・下行性疼痛抑制系の活性化・体性感覚皮質の再組織化を促進する。鏡療法(Mirror Therapy)・バーチャルリアリティ(VR)訓練は視覚フィードバックを通じて感覚運動統合を再構築する。
③ 心理的アプローチ(認知行動療法・マインドフルネス):痛みの認知・情動的側面にアプローチ。破局化思考・痛み回避行動を修正し、自己効力感を回復させる。交感神経系の過活動(疼痛増幅因子)を抑制する自律神経調整技法も並行させる。
感覚統合訓練の実際 ― 段階的脱感作(Graded Desensitization)
段階的感覚脱感作プロトコル
素材の選択:綿(最も柔らかい)→ 柔らかい布 → タオル → 振動デバイス、と段階的に素材を変える。患者が「触れても痛くない」と感じる素材・強さを起点とする
部位の選択:アロディニアが軽い部位(感覚過敏の境界域)から開始し、徐々に過敏域の中央へ近づける。体幹→近位→遠位の順で進めることが多い
温度刺激の漸進的導入:ぬるま湯(36〜37℃)への手浴から開始。冷水・氷は初期段階では避ける。温度への慣れが確認できたら徐々に温度幅を広げる
セッション時間と頻度:5〜10分の短時間から開始。患者の耐性に応じて20〜30分へ延長。週2〜3回の施設訓練+毎日の自主訓練(5分)を推奨。翌日の疼痛変化を必ず確認してから次ステップへ進む
鏡療法(Mirror Therapy)・グレーデッドモーターイメージリー(GMI)
鏡を使って健側の運動を患側で行っているように見せることで、脳は「患側が正常に動いている」という視覚情報を受け取り、体性感覚マップの異常な再編成を正常化します。グレーデッドモーターイメージリー(GMI)では①左右識別→②運動イメージ→③鏡療法 の3段階で段階的に痛みの認知を変えていきます。VR(バーチャルリアリティ)訓練はさらに没入感を高め、注意分散効果と感覚運動再統合を同時に提供します。
認知行動療法(CBT)・ペイン教育・マインドフルネスの役割
視床痛における「痛みの知覚」は心理的要因(ストレス・不安・破局化思考)によって大きく増幅されます。認知行動療法(CBT)では①「痛みは危険のサイン」という誤った認知の修正②痛みを避けることによる活動量低下・脱条件付けの悪循環を断つ③段階的な活動参加による自己効力感の回復を目指します。ペイン教育(Pain Neuroscience Education: PNE)では「なぜ痛みが慢性化するのか」を患者が理解することで破局化思考を減らします。マインドフルネスでは痛みそのものへの非評価的注意を訓練し、交感神経系の過活動を抑制します。深呼吸・漸進的筋弛緩法の自宅実践は自律的な痛み管理の基盤となります。
多職種連携と介入ステップ別手順
多職種連携における役割分担
| 職種 | 視床痛ケアにおける主な役割と介入内容 | 連携のポイント |
|---|---|---|
| 医師(神経科・ペインクリニック) | 診断確定・画像評価・薬物療法の導入・調整・神経刺激療法の適応判断・他疾患の鑑別 | 疼痛悪化・新症状は速やかに報告。薬効と副作用の経過をリハビリ側からフィードバックする |
| 理学療法士(PT) | 感覚統合訓練(脱感作)・運動療法・痛みのない範囲での筋力・可動域訓練・歩行・ADL動作の安全管理・鏡療法 | 感覚評価結果と運動療法の強度設定を連動。毎セッションのNRS記録を共有する |
| 作業療法士(OT) | 上肢・手部のアロディニア対応・感覚脱感作訓練・巧緻機能回復・ADL工夫・環境調整・生活用品の選択指導 | 衣服素材・調理用品・日常動作での疼痛トリガーを特定し環境調整に反映 |
| 言語聴覚士(ST) | 構音・嚥下障害合併時の評価・治療。失語症患者の疼痛コミュニケーション支援(痛みを表現できない患者の行動変化を観察) | 失語症患者は疼痛を適切に表現できないことがある。表情・行動変化から疼痛を読み取る観察力が必要 |
| 看護師 | 24時間の疼痛モニタリング・服薬管理・トリガー観察(体位・衣服・温度)・睡眠・情動状態の把握 | 深夜〜早朝の疼痛増強パターン・不眠・服薬後の変化を記録してチームに共有 |
| 臨床心理士・公認心理師 | CBT・マインドフルネス・痛み教育(PNE)・うつ病・不安障害の評価と心理的介入 | 疼痛の心理的増幅因子(破局化・恐怖回避)の評価結果をチームで共有し介入計画に反映 |
| MSW(医療ソーシャルワーカー) | 退院後の支援体制(自費リハビリ・訪問リハビリ・デイケア)の調整・疼痛管理が継続できる生活環境の整備 | 慢性疼痛は在宅移行後も継続ケアが必要。地域支援との連絡窓口として機能 |
介入ステップ別手順(STROKE LAB式)
初期評価 ― 神経学的評価・痛みの性質・感覚地図・機能への影響を多角的に把握
感覚テスト(温度・触覚・針刺激)でアロディニア・感覚鈍麻の分布を体表に図示した感覚地図を作成。DN4・NRS・BPIで疼痛を定量化。MRI所見と照合して病変部位と症状分布の解剖学的整合性を確認。ADL・睡眠・情動・活動制限への影響を評価して介入優先順位を決定する。
薬物療法の確認と医師との連携 ― リハビリタイミングを最適化
処方薬(種類・用量・開始時期・副作用)を把握し、薬効が安定してきた時期にリハビリ強度を高める計画を立てる。眠気・めまい等の副作用がある場合はセッション時間・内容を調整。効果不十分と感じた場合は速やかに医師へフィードバックする。
感覚統合訓練の段階的導入 ― 痛みを誘発しない刺激から始める
感覚地図の「境界域(過敏度が低い部位)」から開始し5〜10分の短時間セッションで実施。素材・強度・部位を段階的に変更。翌日の疼痛持続・増強がないことを確認してから次ステップへ進む。自主訓練の手技を習得させ、自宅でも毎日5分の継続を促す。
運動療法・鏡療法の並行実施 ― 痛みのない範囲で機能回復を促進
NRS 2〜3点以下を維持することを目標に負荷調整。関節可動域・筋力維持訓練から開始し、鏡療法・GMIを組み合わせて感覚運動統合を促進。急激な疼痛増強があれば即座に中止し医師・チームに報告する。
心理的アプローチ・自己管理能力の育成
CBT・ペイン教育(PNE)・マインドフルネスを導入。「痛みをコントロールできる」という自己効力感の育成が最重要。深呼吸・漸進的筋弛緩法・リラクゼーション技法を指導し、毎日の自主実践を習慣化させる。家族・介護者にも痛み管理の方法を伝える。
長期フォローアップ ― 定期的な再評価と多職種カンファレンス
2〜4週ごとにNRS・ADL・睡眠・QOLを再評価し、プログラムを修正。疼痛の増悪・新症状出現時は速やかに医師へ報告して薬物療法の見直し・神経刺激療法の追加を検討。在宅移行後も自費リハビリ・訪問リハビリ・オンラインリハビリで継続支援を行う。
患者・家族のための日常生活の工夫
視床痛は24時間・365日の継続的なセルフマネジメントが回復の鍵を握ります。以下の工夫は自宅でも実践できる日常生活の調整です。
衣類・寝具の工夫
縫い目が少ない・シームレスの素材を選ぶ。綿100%の柔らかい肌着から試してみる。着圧の強い靴下・弾性ストッキングはアロディニアを増強する可能性があるため担当医・療法士に相談の上使用する
シーツの素材をシルク・竹繊維など摩擦の少ない素材に変える。掛け布団の重さで疼痛が増す場合はリフター・布団クリップで重さを分散する。患側を圧迫しない安楽なポジショニングを療法士と相談して決める
急激な温度変化(冷房→屋外・熱い風呂)が疼痛を誘発しやすい。室温を一定に保つ(26〜28℃程度が快適な人が多い)。入浴はぬるめのシャワーから試して徐々に慣らす。冷房の風が直接患部に当たらないよう工夫する
手部のアロディニアがある場合、柔らかい綿手袋や薄い手袋で物体との接触刺激を軽減できることがある。ただし感覚脱感作訓練の進行状況に合わせて「保護に頼りすぎない」バランスが重要
日常動作・社会参加での工夫
熱い鍋・冷たい食材に直接触れることは初期段階では避ける。シリコン製トング・断熱グローブ・滑り止めマットなどの補助具を活用。作業時間を分割して疲労と疼痛の増強を防ぐ
タオルでの摩擦刺激を避けるためシャワーノズルで流し洗いから試みる。乾燥後は「叩かず押し当てる」形でタオルを使う。保湿剤は皮膚の状態を安定させ感覚閾値の安定に役立つことがある
電車・バスの冷房が直接当たる席を避ける。混雑した場所での押し合いはアロディニアを強く誘発する。外出前に目的地の混雑時間帯を確認し、空いている時間帯に行動するスケジューリングが有効
就寝前の入浴温度を適切に調整(ぬるめが基本)。寝る1〜2時間前にリラクゼーション(深呼吸・漸進的筋弛緩法)を行う。「眠れないことへの不安」が疼痛を増幅するため、眠れない夜は「横になるだけでよい」と割り切ることも重要
⚠️ 家族・介護者が知っておくべき3つの注意点
① 「痛みを我慢させない・激励しすぎない」:視床痛の痛みは精神的に弱いから感じるのではなく、神経系の客観的な機能障害によるものです。「頑張れ」「根性で乗り越えろ」は患者の心理的負担を増やし、疼痛をさらに増悪させることがあります。
② 「マッサージ・強い圧迫は慎重に」:善意のマッサージ・さする動作が過敏な皮膚に強い疼痛を引き起こすことがあります。触れ方・圧力は必ず担当療法士に確認してから行ってください。
③ 「疼痛日記のつけ方を患者・家族で共有する」:「いつ・どこが・どんな痛みで・何がトリガーになったか」を記録することで、担当医・療法士との情報共有の質が大幅に向上します。スマートフォンのメモアプリで簡単な記録を続けることを勧めてください。
最新エビデンス ― TMS・MCS・DBS・リハビリ

視床痛(中枢性疼痛)についての最新知見まとめ①

視床痛(中枢性疼痛)についての最新知見まとめ②
| 治療法 | 主なエビデンスの内容・出典 | エビデンスレベル | 臨床的推奨 |
|---|---|---|---|
| アミトリプチリン(TCA) | Leijon & Boivie 1989のRCTで有意な疼痛軽減。Finnerup et al. 2015でも第一選択として推奨 | A(RCTに基づく強いエビデンス) | ✅ 第一選択 |
| プレガバリン・ガバペンチン | 神経障害性疼痛全般への広いエビデンス(Finnerup et al. 2015)。副作用プロファイル良好 | A(強いエビデンス) | ✅ 第一選択 |
| ラモトリギン | Vestergaard et al. 2001のRCTでCPSPへの有効性示唆。ただしサンプル数が少ない | B(中程度) | △ 代替薬として検討 |
| トラマドール(弱オピオイド) | 神経障害性疼痛全般でB推奨(Finnerup et al. 2015)。依存リスクに注意 | B(中程度) | △ 補助的使用 |
| rTMS(反復経頭蓋磁気刺激) | 運動野刺激(M1-rTMS)でCPSP・神経障害性疼痛に中程度の改善。Lefaucheur et al. 2014でLevel B推奨 | B(中程度) | ✅ 第二選択候補(非侵襲的) |
| MCS(硬膜外運動野皮質電気刺激) | Rasche et al. 2006:難治性疼痛の50〜70%で短期改善。CPSPへはDBSより選好される傾向 | B(中程度・観察研究中心) | ⚠️ 難治性への外科的選択肢 |
| DBS(脳深部刺激療法) | Owen et al. 2006:他の慢性疼痛よりCPSPへの効果は限定的 | C(エビデンス限定的) | ⚠️ 最終手段(慎重に適応判断) |
| TENS(経皮的電気神経刺激) | 様々な結果。一部で改善、一部で悪化の報告あり(Klit et al. 2009レビュー) | C(エビデンス不十分・結果不一致) | ⚠️ 慎重な適用・厳密なモニタリング必須 |
| 認知行動療法(CBT) | 慢性疼痛全般でQOL改善の一貫したエビデンス(Turk et al. 2008) | A(慢性疼痛全般) | ✅ 薬物療法と並行推奨 |
| 鏡療法・GMI | CRPS・幻肢痛でLevel Bエビデンス(Moseley 2006)。CPSPへの直接研究は少ないが理論的根拠が強く試みる価値あり | B(類似疾患のエビデンス) | ✅ 試みる価値あり |
新人療法士のための10の注意点
① 痛みの評価は慎重かつ丁寧に
過度な刺激は疼痛を悪化させます。DN4・NRS等を使って疼痛を定量化し、「どんな痛みが・いつ・何で誘発されるか」を丁寧に把握してから介入を計画してください。「とりあえずやってみる」は禁物です。
② 感覚過敏の程度と分布を感覚地図で可視化
感覚統合訓練の前に、体表の感覚地図(どこが過敏でどこが鈍麻か)を作成することが介入精度を大幅に高めます。境界域から介入を開始し、徐々に過敏域へ近づけます。
③ 心理的状態への感度を高める
ストレス・不安・不眠はCPSPを増幅させます。リハビリ前後の患者の表情・言動・睡眠状況から心理的状態をキャッチし、必要に応じてリラクゼーション技法や心理士へのコンサルテーションを行ってください。
④ 運動療法は「NRS 2〜3点以下」を目安に
「痛みが出るまで追い込む」はCPSP患者には禁物。NRS 2〜3点以下を維持しながら段階的に負荷を上げます。セッション中は疼痛のモニタリングを欠かさず、増強したら即時中止・調整します。
⑤ コミュニケーションを密に保つ
CPSPは患者ごとに疼痛パターンが大きく異なります。「今どんな感じですか?」を介入中に定期的に確認し、痛みが増した場合は即座に中止・対応を調整する柔軟性を持ってください。
⑥ 薬物療法との連携を意識する
処方薬の種類・用量・副作用(眠気・ふらつき)を把握してリハビリを計画します。鎮痛効果が最大化するタイミング(服薬後1〜2時間)にリハビリを行うと効果的なことがあります。
⑦ 自己管理能力の向上を促す
CPSPは慢性的です。深呼吸・リラクゼーション・軽ストレッチなど、患者が自宅でできる自己管理技術を指導し、日常生活での疼痛コントロール力を高めてください。疼痛日記の活用も有効です。
⑧ 鏡療法・GMIで感覚運動統合を再構築
鏡療法・グレーデッドモーターイメージリー(GMI)で、脳の体性感覚マップの異常な再編成を正常化することを目指します。段階的に①左右識別→②運動イメージ→③鏡療法の順で進めます。
⑨ リハビリ計画は毎回状態確認のうえ設定
「先週できたから今週も同じ強度」という思い込みは危険。前日の疼痛状態・睡眠・ストレスによって毎日閾値が変動します。毎セッション開始前にNRSで確認してから介入内容を決定してください。
⑩ 疼痛トリガーを把握・患者に伝える
寒冷・振動・特定の姿勢・疲労・ストレス・混雑した環境などの個別トリガーを生活史から把握し、環境調整・日常動作指導に反映させます。トリガーを患者自身が認識できるようにすることが自己管理の第一歩です。
よくある質問(FAQ)
視床痛は完全に治りますか?
「痛みをゼロにする」から「痛みと共に質の高い生活を送る(QOL改善)」への目標転換も重要な治療の一環です。予後を左右する主な因子として①早期治療開始②病変サイズが小さい③心理的サポートの充実④多職種連携の質の高さ が挙げられています。
視床痛の痛みはどのくらいの期間続きますか?
治療なしで自然に解消することは稀で、未治療のままでは慢性化・難治化するリスクが高まります。「最近痛みが強くなった」「新しい疼痛が出現した」場合は速やかに専門医に相談してください。
「触れるだけで痛い(アロディニア)」への対処法を教えてください。
①まず「何が触れても痛くない素材・状況」を特定する(例:柔らかい絹の布はOKだが綿タオルは痛い)
②痛みを感じない素材・強さで患部周辺(境界域)から毎日5分の感覚刺激を行う
③1〜2週間後に症状が安定していたら少しだけ刺激の強度・素材を変える
④並行して薬物療法(抗けいれん薬・TCA)で神経過敏を抑制する
絶対に避けるべきことは「我慢して痛い刺激を与え続ける」ことです。これはかえって神経の感作を強め、慢性化を促進します。必ず理学療法士・作業療法士の指導のもとで行ってください。
脳卒中後、どのくらいで視床痛が出始めますか?
6か月以降に発症する患者も約20%存在します(Klit et al. 2009)。「脳卒中はよくなってきているのに最近痛みが出てきた」という訴えは視床痛のサインです。速やかに主治医に相談してください。
視床痛の治療薬はどれくらいで効果が出ますか?
アミトリプチリン・プレガバリンは低用量から開始し、副作用(眠気・ふらつき・口渇・便秘)を確認しながら漸増します。副作用が強い場合は主治医に相談して薬剤・用量の変更を検討します。薬物療法で効果が不十分な場合は、rTMS・MCS・DBSなどの神経刺激療法との組み合わせが検討されます。
リハビリを続けるほど視床痛が悪化することはありますか?
ただし「訓練直後に少し痛みが増えること(24時間以内に回復)」と「慢性的な疼痛の悪化(翌日以降も持続)」は区別する必要があります。後者は過負荷のサインです。担当PT・OT・STとともに定期的にNRSをモニタリングし、「今日のリハビリ後はどうでしたか?」という確認を継続してください。視床痛のリハビリは「急いで良くしようとしない」ことが長期的な成功につながります。
視床痛とCRPS(複合性局所疼痛症候群)・肩手症候群はどう違いますか?
鑑別の実践的なポイント:①CPSPは病変対側の半身全体に分布しやすく、温度感覚の逆転(冷刺激→灼熱痛)を伴うことが特徴②CRPSは発汗・皮膚色調変化・浮腫などの自律神経症状が目立つ③肩手症候群は肩関節拘縮と手部浮腫が主で、可動域訓練で改善しやすい。
これらが合併する場合もあるため、感覚検査・MRI所見・自律神経症状の有無で丁寧に鑑別し、それぞれに適した治療を選択することが重要です。
STROKE LABの視床痛リハビリ ― 急性期から退院後まで
退院後しばらくして「服が触れるだけで足が痛い」という症状が出てきて、主治医に相談したら視床痛と言われました。STROKE LABで感覚統合訓練とミラーセラピーを受け、少しずつ布の感触に慣れることができました。完全には消えていませんが、以前の「何もできない」状態から「工夫すれば外出できる」状態になれました。
60代女性・視床梗塞発症後7か月
「温かいものが熱く感じる」「冷たいものが痛い」という奇妙な感覚が続いていました。STROKE LABのセラピストに段階的な温度刺激訓練を行ってもらい、半年後には温度に対する過剰な反応が大幅に改善しました。QOLが戻ってきた実感があります。
70代男性・視床出血後9か月
視床痛リハビリの設計フロー(5ステップ)
Step 1 徹底的な初期評価:DN4・NRS・QST・感覚地図作成・MRI所見照合で「何がどこでどう損傷されているか」を解剖学的に特定
Step 2 チーム方針の決定:PT(運動・感覚統合)/ OT(ADL・上肢アロディニア対応)/ ST(構音・嚥下合併時)/ 心理士(CBT・PNE)の役割分担を多職種カンファレンスで明確化
Step 3 段階的介入:感覚脱感作(週1〜2回)+鏡療法+運動療法+心理的アプローチを並行実施。2週ごとに評価して漸増
Step 4 薬物療法・神経刺激との連携:主治医と疼痛の変化を情報共有し、服薬タイミングをリハビリ計画に反映
Step 5 在宅移行支援:家族への疼痛管理教育・自宅環境の調整指導・外来/訪問/オンラインリハビリによる継続フォロー体制の構築
参考文献・引用文献
- 1) Dejerine J, Roussy G. Le syndrome thalamique. Rev Neurol (Paris). 1906;14:521-532. 【視床痛の原著(Dejerine-Roussy症候群の初記載)】
- 2) Andersen G, Vestergaard K, Ingeman-Nielsen M, Jensen TS. Incidence of central post-stroke pain. Pain. 1995;61(2):187-193. 【有病率8%の基本文献】
- 3) Sackley C, et al. Rehabilitation of central post-stroke pain. Cochrane Database Syst Rev. 2013. 【有病率11%の報告・コクランレビュー】
- 4) Klit H, Finnerup NB, Jensen TS. Central post-stroke pain: clinical characteristics, pathophysiology, and management. Lancet Neurol. 2009;8(9):857-868. 【CPSPの発症時期分布・最重要レビュー論文】
- 5) Leijon G, Boivie J. Central post-stroke pain—a controlled trial of amitriptyline and carbamazepine. Pain. 1989;36(1):27-36. 【アミトリプチリンのCPSPへの有効性を示した最初のRCT】
- 6) Kumar B, Kalita J, Kumar G, Misra UK. Central poststroke pain: a review of pathophysiology and treatment. Anesth Analg. 2009;108(5):1645-1657.
- 7) Finnerup NB, et al. Pharmacotherapy for neuropathic pain in adults: a systematic review and meta-analysis. Lancet Neurol. 2015;14(2):162-173. 【神経障害性疼痛薬物療法の最高レベルシステマティックレビュー・プレガバリン/アミトリプチリンのエビデンス】
- 8) Lefaucheur JP, et al. Evidence-based guidelines on the therapeutic use of repetitive transcranial magnetic stimulation (rTMS). Clin Neurophysiol. 2014;125(11):2150-2206. 【rTMSガイドライン:CPSPへのLevel B推奨の根拠】
- 9) Rasche D, Ruppolt M, Stippich C, Unterberg A, Tronnier VM. Motor cortex stimulation for long-term relief of chronic neuropathic pain: a 10 year experience. Pain. 2006;121(1-2):43-52. 【MCS(硬膜外運動野皮質電気刺激)の50〜70%有効率の根拠論文。TMSとは異なる侵襲的手術】
- 10) Owen SL, Green AL, Stein JF, Aziz TZ. Deep brain stimulation for the alleviation of post-stroke neuropathic pain. Pain. 2006;120(1-2):202-206. 【DBS vs CPSPの有効性・限界の検討】
- 11) Vestergaard K, et al. Lamotrigine for central poststroke pain: a randomized controlled trial. Neurology. 2001;56(2):184-190. 【ラモトリギンのCPSPへのRCT】
- 12) Lenz FA, et al. Abnormal neuronal activity in the somatosensory thalamus in patients with central pain. J Neurophysiol. 1989;62(2):503-506. 【視床の異常バースト発火とCPSPの関連】
- 13) Moseley GL. Graded motor imagery for pathologic pain: a randomized controlled trial. Neurology. 2006;67(12):2129-2134. 【GMI(グレーデッドモーターイメージリー)のCRPS・幻肢痛への有効性:Level Bエビデンス】
- 14) Turk DC, Swanson KS, Tunks ER. Psychological approaches in the treatment of chronic pain patients. Can J Psychiatry. 2008;53(4):213-223. 【慢性疼痛へのCBT・心理的アプローチのエビデンス】
- 15) Hatem SM, et al. Rehabilitation of motor function after stroke. Front Hum Neurosci. 2016;10:442. PubMed
- 16) 日本ペインクリニック学会. 神経障害性疼痛薬物療法ガイドライン改訂第2版. 2016.
- 17) 日本脳卒中学会. 脳卒中治療ガイドライン2021(改訂2023).
視床痛で「もう諦めるしかない」と
思っていませんか?
難治性の視床痛にも、段階的なリハビリと最新のアプローチで
QOLを大きく改善できる可能性があります。
急性期からの一貫した視床痛ケアをSTROKE LABにご相談ください。

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)











