【2026年版】脳卒中・脳梗塞後のワーラー変性の診断は?リハビリテーションからMRI・CTまで解説
脳梗塞・脳卒中の急性期に虚血で死滅した神経細胞の「軸索」が、その後どのように変性・消失していくかをご存知でしょうか。今回は、ワーラー変性(Wallerian Degeneration)について、発生メカニズム・脳内での5段階プロセス・MRI/DTI・CTによる画像所見・ベッドサイドでの観察ポイント・リハビリテーションとの関係・最新エビデンスまで、専門家目線と患者目線の双方で徹底解説します。
ワーラー変性(Wallerian Degeneration)とは、神経線維(軸索)が細胞体から切り離された後に遠位側が変性・崩壊するプロセスです。1850年にAugustus Volney Wallerによって初めて記載され、末梢神経だけでなく脳卒中・脳梗塞後の中枢神経系でも広く生じます(梗塞の部位・範囲・関連経路によって程度は異なります)。梗塞によって死滅した運動皮質ニューロンの軸索は皮質脊髄路に沿って変性が進み、発症後数日から数週間・数ヶ月の経過で片麻痺・感覚障害・言語障害の「障害の広がり」に寄与します。MRIのT2・FLAIR・DTI(拡散テンソルイメージング)で非侵襲的に評価でき、リハビリテーション計画の予後予測や介入戦略に直結する重要な病態生理です。
- 正式名称:Wallerian Degeneration(ワーラー変性)。1850年にAugustus Wallerが記載
- 定義:神経線維(軸索)が細胞体から切り離された後、遠位側(末梢側)が変性・崩壊するプロセス。末梢神経系・中枢神経系のいずれにも生じる。脳梗塞後は梗塞巣に関連する経路で程度の差はあれ必ずみられる二次変性
- 脳卒中との関係:梗塞後に死滅した皮質ニューロンの軸索(主に皮質脊髄路・視放線・弓状束)が変性。「一次損傷の遠隔部まで障害が広がる」二次損傷として機能予後に影響
- 発生時期:梗塞後数時間〜数日以内に軸索変性開始。T2/FLAIR変化は亜急性〜慢性期(2〜4週以降)に顕在化。DTIは早期から異常検出可能
- 画像:MRI T2/FLAIR = 白質高信号 | DTI(FA低下・MD上昇)= 軸索・ミエリン破壊 | CT = 慢性期の低密度変化(早期感度は低い)
- 主要経路:皮質脊髄路(運動麻痺)・視放線(視野障害)・弓状束(失語症)・視床皮質路(感覚障害)などで高頻度に生じる
- リハビリとの関係:変性の程度(DTI FA値)は運動機能回復の予測因子。変性が強い患者では神経可塑性を促進する集中的介入(CI療法・rTMS・tDCS)の重要性が増す
- 中枢神経系の限界:末梢神経と異なり中枢神経では軸索再生が困難(グリア瘢痕・阻害因子による阻害環境)。代償的可塑性(スプラウティング・迂回路形成)が機能回復の主メカニズム
- モニタリング:DTI-FA・MD(拡散係数)の経時的追跡が変性の進行・安定化の客観的指標。理学療法士・作業療法士・言語聴覚士が観察すべき臨床サインと連動
ワーラー変性とは ― 定義・歴史・発生メカニズム
ワーラー変性は1850年、英国の生理学者Augustus Volney Wallerが坐骨神経切断後の末梢神経を追跡した研究で初めて系統的に記載しました。神経線維(軸索)が細胞体(核)から切り離されたとき、切り離された遠位側の軸索が崩壊・消失していくこのプロセスは、彼の名を冠して「Wallerian Degeneration」と呼ばれています。
脳卒中・脳梗塞の文脈では、梗塞によって死滅した上位運動ニューロン(一次運動野・内包・脳幹の皮質脊髄路)の軸索が、梗塞巣より遠位側(下位運動ニューロンに向かう方向)に向かって変性していく現象として理解されます。
🔬 中枢神経系 vs 末梢神経系:ワーラー変性の違い
共通点:どちらの系でも、細胞体から切り離された軸索は時間の経過とともに変性し、ミエリン(髄鞘)が崩壊し、マクロファージ・ミクログリアによる貪食(クリーンアップ)が起きます。
中枢神経系の大きな違い(治療上の重要ポイント):末梢神経系では「シュワン細胞」がガイド管(バンゲル帯)を形成して軸索再生を積極的にサポートします。一方、中枢神経系ではオリゴデンドロサイト由来の阻害因子(Nogo-A・MAG・OMgp)やグリア瘢痕(反応性アストロサイトが形成するバリア)が再生を強力に阻害します。このため、脳梗塞後のワーラー変性は「原則として可逆的でない」ことが、リハビリテーション戦略において決定的に重要な前提となります。
| 比較項目 | 中枢神経系(脳・脊髄) | 末梢神経系 |
|---|---|---|
| 主なサポート細胞 | ミクログリア・アストロサイト | シュワン細胞 |
| 軸索再生の可能性 | 非常に限定的(グリア瘢痕・阻害因子) | 可能(バンゲル帯がガイド) |
| 変性の時間スケール | より遅い(数週〜数ヶ月単位) | 相対的に速い(数日〜数週) |
| MRI/DTI検出 | T2/FLAIR高信号・DTI-FA低下で追跡可能 | 主に臨床症状・神経伝導検査で評価 |
| リハビリの主目標 | 神経可塑性の促進・代償経路の開発 | 軸索再生の促進・神経再支配の促進 |
| 機能回復のメカニズム | 迂回路・スプラウティング・用依存的可塑性 | 軸索再生・標的への神経再支配 |
脳卒中後のワーラー変性 ― 5段階プロセスと時間経過
脳梗塞後のワーラー変性は以下の5段階で進行します。各ステージを理解することが、画像所見の読み方とリハビリ計画の時間的戦略の両方に不可欠です。
初期損傷(発症直後〜数時間)
脳卒中によって血流が遮断された領域の神経細胞が虚血性に死滅します。この時点では梗塞巣内の神経細胞体(核)と軸索がともに障害されています。軸索は細胞体から「切り離された状態」となり、ワーラー変性のスタートラインに立ちます。この段階でMRIのDWI(拡散強調画像)で梗塞巣の高信号が現れますが、ワーラー変性の軸索経路(遠位側)はまだ画像上は正常です。
染色分解(Chromatolysis):数時間〜数日
生き残った損傷ニューロンの細胞体では、ニッスル物質(粗面小胞体)が膨張・分散する「染色分解」が起きます。これは損傷修復のための代謝亢進の反応ですが、細胞体が回復できるかは損傷の程度によります。また切り離された軸索の遠位側では、早くも軸索骨格(ニューロフィラメント・微小管)の崩壊が始まります。
軸索変性(Axonal Degeneration):数日〜数週
細胞体から切り離された軸索の遠位側が、カルシウム依存性のプロテアーゼ(カルパイン)活性化などを介して活発に崩壊します。同時にミエリン(髄鞘)も崩壊し始めます。この段階からDTIで拡散係数(MD)の上昇・FA(フラクショナル異方性)の低下として検出が可能となってきます(特に亜急性期以降)。
食作用(Phagocytosis):数週〜数ヶ月
ミクログリア(脳内常駐マクロファージ)・血液由来マクロファージが活性化し、崩壊したミエリン・軸索の残骸を貪食(食作用)によって除去します。このクリーンアップは変性の程度・範囲に応じて数週から数ヶ月かかります。この時期にMRI T2/FLAIRで白質高信号として可視化されるようになります。
慢性期変化・代償的可塑性(数ヶ月〜)
変性・クリーンアップが完了した後、白質路は萎縮・体積減少します。この経路にかかわる脳構造(同側大脳脚の萎縮・脳幹の変化など)も二次的に変化します。一方でこの時期、用依存的神経可塑性(デンドライトスプラウティング・シナプス強化)や迂回路形成によって機能的代償が起きます。この代償的可塑性こそがリハビリテーションの介入標的です。
脳卒中後に変性しやすい主な白質路
🧠 皮質脊髄路(錐体路)
運動皮質→内包後脚→大脳脚→延髄錐体→脊髄。最も変性が生じやすく、片麻痺の程度と強く相関。内包後脚のDTI-FA値は上肢運動機能回復の予測因子として広く研究されています。
👁️ 視放線(Meyer loop含む)
外側膝状体から視覚野へ至る経路。側頭葉・後頭葉・頭頂葉梗塞後に変性。同名半盲・四分盲の二次的悪化に関与することがある。
💬 弓状束・上縦束
ブローカ野・ウェルニッケ野を結ぶ言語白質路。左半球梗塞後の失語症の遷延化にワーラー変性による弓状束の変性が関与。DTIで評価可能。
🖐️ 視床皮質路
視床→大脳皮質感覚野を結ぶ感覚路。視床梗塞・内包梗塞後の感覚障害の持続にワーラー変性が寄与。視床痛(中枢性疼痛)の病態生理にも関係。
⚠️ 変性が「障害の広がり」をもたらすメカニズム
ワーラー変性は梗塞巣自体の障害とは独立した「二次的な遠隔障害」を生み出します。例えば、内包を梗塞した患者では発症後数週〜数ヶ月かけて同側大脳脚のMRI変化(萎縮・高信号)が出現することがあります(Zhang et al. 2018)。これは直接の梗塞巣とは別の部位ですが、臨床的には「なぜ時間が経っても症状が改善しないのか」「なぜ新しい変化が画像に出てきたのか」を説明する際に重要です。
担当の医療スタッフが「画像に新しい変化があります」と説明したとき、それがワーラー変性による変化なのか、新たな梗塞なのかを区別することが、適切な治療・説明・リハビリ計画につながります。
ワーラー変性の画像グレード分類(Grade 0〜3)
ワーラー変性の重症度は画像所見をもとに段階的に評価されます。代表的なのは皮質脊髄路(内包後脚〜大脳脚)に対するグレード分類で、主にT2/FLAIR・DTIを組み合わせて判断します。
| グレード | MRI所見の概要 | DTI-FA | 臨床的意味・リハビリへの示唆 |
|---|---|---|---|
| Grade 0 | T2/FLAIR・DTIともに変化なし | 健側と差なし | 皮質脊髄路は保たれている。良好な運動回復が期待できる |
| Grade 1 | DTIでわずかなFA低下あり。T2/FLAIRは正常〜軽度変化 | 健側比10〜30%低下 | 部分的変性。残存経路が多く、積極的なリハビリで改善が見込める |
| Grade 2 | T2/FLAIRで白質路に沿った高信号。DTIで中等度FA低下 | 健側比30〜60%低下 | 中等度変性。代償経路活用が中心戦略。強度・多様性の高いリハビリが有効 |
| Grade 3 | T2/FLAIRで明確な高信号・萎縮。DTIで高度FA低下〜経路断絶 | 健側比60%以上低下 | 高度変性。皮質脊髄路の機能的寄与が限定的。同側路・脳幹経由路の積極的活用、神経刺激療法(rTMS・tDCS・FES)との組み合わせが推奨される |
※グレード分類は施設・研究者によって基準が異なります。上記は代表的な4段階分類の概要です(Bhatt et al. 2016 等を参考)。
🔑 DTI-FA + MEP(運動誘発電位)の組み合わせによる予後予測
内包後脚・大脳脚のDTI-FA値と、経頭蓋磁気刺激で測定するMEP(Motor Evoked Potential:運動誘発電位)の有無を組み合わせることで、脳卒中後の上肢運動機能回復の予測精度が単独評価より大幅に高まります。
予後予測の組み合わせパターン(Stinear et al. PREP2アルゴリズム等を参考):
①MEP陽性 + FA軽度低下(Grade 0〜1):皮質脊髄路が機能しており、良好な運動回復(Fugl-Meyer 20点以上の改善)が期待できる。課題指向型・高強度訓練が最も有効。
②MEP陰性 + FA中等度低下(Grade 2):直接経路の損傷があるが代償経路の活性化余地がある。CI療法・ロボットリハビリ・神経刺激療法の組み合わせで代償経路を積極的に開発する戦略が有効。
③MEP陰性 + FA高度低下(Grade 3):機能的回復は限定的と予測されるが、「あきらめ」ではなく代償経路(同側路・前補足運動野経由路)の最大活用と日常動作への適応戦略を組み合わせる。補装具・FES・環境調整の早期導入も重要。
注:PREP2アルゴリズムはエビデンスが蓄積されつつあるツールですが、個々の患者への適用には専門医の判断が必要です。予後予測は「治療努力の上限を決める」ためでなく、「戦略を最適化する」ために使います。
MRI・DTI・CTによる画像所見 ― 何がいつ見えるか
白質変化に高感度
最早期・最詳細
慢性期・初期評価に
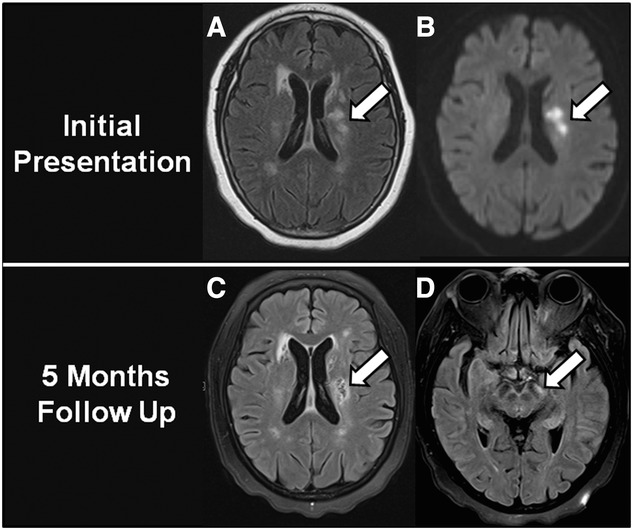
図引用:Wallerian Degeneration Beyond the Corticospinal Tracts(J Neuroimaging, 2016)
MRIによるワーラー変性の評価 ― 白質変化の「金標準」
| シーケンス | ワーラー変性での所見と解釈 |
|---|---|
| T2 | 変性軸索内の水分含量増加により白質路に沿った高信号として出現(亜急性〜慢性期)。梗塞巣から遠位方向に高信号が延びるパターンが特徴的 |
| FLAIR | T2と同様の高信号変化。脳室周囲の白質病変との鑑別に有用。慢性期には萎縮(体積減少)として現れることも |
| DWI | 急性〜亜急性初期:制限拡散(高信号・ADC低下)→ 時間経過でADC上昇(変性・脱髄の進行を反映)。Musson & Romanowski(2010)は橋梗塞後の中小脳脚に急性期の制限拡散変化を報告 |
| DTI-FA | フラクショナル異方性(FA)低下:軸索の方向性が失われることを反映。梗塞後数週間から有意な低下が検出可能。運動機能予後との相関が高く(Qin et al. 2012)、リハビリ計画の予測因子として最も感度が高い |
| DTI-MD | 平均拡散係数(MD)上昇:ミエリン崩壊・細胞内構造の喪失による水の自由拡散増加を反映。FA低下と組み合わせて変性の程度を定量評価 |
CTによる評価 ― 初期評価・慢性期変化の検出
| 時期 | CTでのワーラー変性関連所見 |
|---|---|
| 急性期 | ワーラー変性自体はCTでほぼ検出できない。梗塞巣の初期変化(ASPECTS)・出血除外が主目的 |
| 亜急性期 | 変性経路(白質路)に沿った微細な密度変化は通常CTでは判別困難。MRIが必要 |
| 慢性期 | 神経経路に沿った低密度域・萎縮・体積減少としてCT上に出現(Becerra et al. 1995)。同側大脳脚の萎縮・側頭葉や大脳脚の低密度化が観察されることがある |
急性期の救急評価ではCT(迅速・出血検出・禁忌少ない)が第一選択です。ワーラー変性の評価・予後予測・リハビリ計画の根拠となる白質変化の精密評価にはMRI(特にDTI)が必須です。MRI禁忌(ペースメーカーなど)の患者では、慢性期の経過追跡にCTを補助的に使用します。
MRI・DTI・CTの役割分担まとめ
| 評価項目 | MRI(T2/FLAIR) | DTI(FA・MD) | CT |
|---|---|---|---|
| 急性期(数時間〜数日)の変性検出 | △ 早期は不明瞭 | ✅ 早期から変化検出可 | ❌ ほぼ検出不可 |
| 亜急性〜慢性期(2週以降)の変性 | ✅ 高信号として明瞭 | ✅✅ FA低下・MD上昇で定量的 | △ 低密度変化として出現 |
| 白質路の経路可視化(tractography) | ❌ | ✅✅ 最も詳細 | ❌ |
| 運動機能予後予測 | △ 病変範囲で間接的 | ✅✅ FA値との相関が実証済み | ❌ |
| 出血除外・初期梗塞評価(ASPECTS) | ✅ DWIが最も鋭敏 | △ 補助的 | ✅✅ 最速・広く利用可能 |
| 多発性硬化症等との鑑別 | ✅ 高解像度画像 | ✅ 追加情報を提供 | ❌ |
| 所要時間・利用しやすさ | 中程度(20〜40分) | 追加10〜15分(MRIと同時施行) | 最短(5分未満) |
ベッドサイドでの観察・日常の確認ポイント
ワーラー変性の進行は直接「ベッドサイドで見える現象」ではありません。しかし、変性の進行・安定・代償的改善は神経学的評価・機能的評価・リハビリの進捗・認知行動的変化として間接的に観察されます。以下の4つの視点から継続的にモニタリングすることが、早期の再評価と介入修正につながります。
神経学的検査での変化
MMT(徒手筋力テスト)・感覚検査・NIHSS・Fugl-Meyer の繰り返し評価で「筋力・協調・感覚・言語機能」の変化を追跡します。以前より握力が低下、または関節の随意運動が減少している場合、ワーラー変性の進行を疑い画像フォローを医師に相談する根拠となります。
機能・ADLの変化
日常生活動作(FIM・Barthel Index)の改善が停滞・低下している場合、変性の進行または不適切なリハビリ戦略の可能性を示唆します。特に「以前できていた動作が難しくなった」変化は変性の進行として記録し、チームで共有することが重要です。
リハビリ進捗の停滞・低下
同一の訓練内容でパフォーマンスが向上しない、または悪化する場合は患者の神経学的状態の再評価が必要です。特に発症後2〜12週は変性が進行する時期であるため、この時期のリハビリの量・質・戦略を定期的に見直します。停滞が続く場合は追跡DTI撮像を医師に相談することを検討してください。
認知・行動・情動の変化
集中力低下・記憶障害・感情失禁・うつ症状は、ワーラー変性による白質路(特に前頭葉接続線維)の変化が関与する可能性があります。認知機能の低下がリハビリへの参加度を低下させる悪循環に陥る前に、神経心理士・言語聴覚士と連携した早期評価・支援が重要です。
💡 「画像のフォロー」はいつ行うか ― 臨床的タイミングの目安
急性期初回MRI(DWI)は全例に行われます。ワーラー変性の経過評価のためのフォローアップMRI(特にDTI)は一般的に以下のタイミングが推奨されます:①発症後4〜6週(亜急性期変化が明瞭化)②発症後3ヶ月(慢性期変化・萎縮の定量評価)③神経学的悪化または停滞が続く場合(タイムリーな追加評価)。定期的な追跡DTIにより、変性の進行と代償的可塑性の両方をモニタリングし、リハビリ介入の強度・内容を調整します。
ワーラー変性に対するリハビリテーション戦略
ワーラー変性に「特定のリハビリ」があるわけではありません。しかし、変性の理解がリハビリ目標・戦略・タイミングを大きく変えます。中枢神経系では軸索再生が困難であることを前提に、①残存回路の最大活用(用依存的可塑性) ②代償経路の積極的開発 ③外部からの神経刺激による可塑性促進という3軸でアプローチします。
理学療法 ― 運動回路の再構築
作業療法 ― 機能・ADLの代償と再学習
言語聴覚療法 ― 言語・嚥下路の再建
神経刺激療法 ― 可塑性促進の最前線
ワーラー変性で皮質脊髄路が重度損傷した患者に対して、残存回路を通じた神経可塑性を外部から促進する技術が注目されています。
| 技術 | 作用機序 | エビデンス水準 |
|---|---|---|
| rTMS(反復経頭蓋磁気刺激) | ①非障害側M1への低頻度刺激(1Hz)で過剰興奮を抑制(半球間抑制モデル)、または②障害側M1への高頻度刺激(10Hz)で興奮性を促進。ただし②の臨床的有効性は①より不確実で患者選択に注意が必要 | 中程度(RCT複数。リハビリとの併用で有効性高まる傾向。単独では限定的) |
| tDCS(経頭蓋直流刺激) | アノード電極で障害側皮質を促進、またはカソード電極で非障害側を抑制。シナプス可塑性のLTP様効果 | 中程度(メタ解析で有効性示唆。独立した効果は不確実) |
| FES(機能的電気刺激) | 末梢から感覚フィードバックを与え皮質再編成を促進。ワーラー変性があっても末梢神経は保たれている場合が多い | 中〜高(RCT複数) |
| BMI(脳機械インターフェース) | 残存する皮質活動を読み取り外骨格を動かす。変性した皮質脊髄路をバイパス | 低〜中(研究段階。重度麻痺への将来的な適用に期待) |
時期別リハビリテーション戦略 ― ワーラー変性の進行に合わせたアプローチ
ワーラー変性は発症後の時間経過で進行します。各フェーズでリハビリの重点を変えることが、神経可塑性を最大限に活かす鍵です。
| 時期 | ワーラー変性の状態 | リハビリの主目標 | 具体的アプローチ |
|---|---|---|---|
| 急性期(発症〜2週) | |||
| 発症直後〜数日 | 梗塞完成。変性開始前期。軸索はまだ一部機能 | 二次合併症予防・廃用予防 | 早期離床・ポジショニング(肩亜脱臼予防)・ROM訓練・嚥下評価(STと連携) |
| 発症1〜2週 | 軸索変性が活発に進行中 | 残存経路の早期活性化 | 麻痺側の積極的な課題指向型訓練開始。疼痛・痙縮管理。DTI・MEP評価で予後方針の初期設定 |
| 亜急性期(2週〜3ヶ月) ― リハビリ効果が最も得られやすい時期 ― | |||
| 2〜6週 | 変性ピーク。食作用が活発。T2変化が出現 | 用依存的可塑性の最大化 | 高強度・高反復の課題指向型訓練。CI療法の導入検討。FESとの併用で感覚フィードバック強化 |
| 6週〜3ヶ月 | 変性が進行から安定化へ移行。代償的可塑性が活発化 | 代償経路の積極的開発 | DTI-FA・MEPによるグレード再評価。Grade 2〜3ではrTMS/tDCSとの組み合わせ訓練を積極的に検討。ロボットリハビリ・ゲームリハビリ導入 |
| 慢性期(3ヶ月以降) | |||
| 3〜12ヶ月 | 変性ほぼ完了。白質路萎縮が安定。代償経路が確立しつつある | 確立した代償経路の強化・ADL定着 | CI療法の集中実施。ADLへの応用訓練(書字・調理・外出)。補装具・FESの定着。家族指導・環境調整 |
| 1年以降 | 変性安定。神経可塑性は低下するが維持される | 維持と社会参加の促進 | 訪問リハビリ・外来リハビリでの継続強化。認知・情動サポート(うつ・疲労への対応)。就労・趣味活動への復帰支援 |
⚠️ 「慢性期だからあきらめる」は誤りです ― エビデンスが示す事実
ワーラー変性が完了した慢性期でも、神経可塑性は継続して存在します。発症後6ヶ月〜数年経過した患者でもCI療法・rTMS・集中訓練で有意な機能改善が得られることが複数の研究で示されています。「発症から何ヶ月を超えたら回復しない」という絶対的な期限はなく、適切な介入・高強度訓練・日常での使用機会の確保が継続的な回復を支えます。ただし、変性が高度(Grade 3)かつ慢性期の場合は「機能回復」と「機能補完(代償・適応)」のバランスを戦略的に設計することが重要です。
臨床ケーススタディ ― ワーラー変性と向き合うリハビリ
📋 症例:石川さん(58歳・男性)左内包後脚梗塞 発症から1年経過
右片麻痺(上肢優位)・軽度失語症 | DTI追跡モニタリング実施例
🏥 急性期(発症1週以内)
突然の右上下肢脱力と軽度の発語障害で救急搬送。MRI DWIで左内包後脚の点状梗塞を確認。NIHSS 7点(右上肢3点・言語1点ほか)。tPA適応外(症状発現から4.5時間超)。初期DTI撮像でFA値は健側と比較して左内包後脚に軽度低下(変性の始まりを示唆)。
📅 亜急性期(発症2〜8週)
追跡MRI(FLAIR)で左内包後脚から大脳脚にかけての高信号域が出現(ワーラー変性の進行を反映)。DTI-FAは健側比で有意に低下し、変性の進行が確認された。右上肢の握力はやや回復傾向にあったが、この時期にMMT評価で「右手の細かい動きが以前より遅くなった」との自覚症状も報告。画像変化と臨床所見の両面から多職種でワーラー変性の進行を共有。リハビリ戦略の見直しを行った。
PT:課題指向型アプローチ中心に上肢・体幹の統合訓練を強化。OT:巧緻動作(箸・書字・キーボード)の段階的再学習プログラム開始。ST:軽度失語に対して言語訓練(呼称・文産生)と嚥下スクリーニング継続。
🔬 慢性期(3〜12ヶ月)
発症3ヶ月時点のDTI:FA値は健側比で有意に低下し安定化傾向。Fugl-Meyer上肢スコアは回復途上(架空数値のため記載なし)。机上の書字は可能になったが、素早いリーチ動作では代償パターン(体幹の過剰使用)が残存。OTでCI療法(2週間集中プログラム)を導入。介入後に上肢機能指標・MAL(使用量スケール)の改善を認めた。同時期に検討・実施したrTMS(1Hz・非障害側M1への抑制刺激)はリハビリとの組み合わせで4週行ったが、rTMSの単独効果は現時点では評価困難。
💬 認知・行動の変化
発症後6ヶ月から「少し忘れっぽくなった」「集中が続かない」の訴え。神経心理検査(MoCA)で軽度の注意・作業記憶低下を確認。白質路(前頭葉接続線維)のDTI変化との関連を医師に報告。認知リハビリ(注意訓練・デュアルタスク訓練)をPT・OT訓練の冒頭に組み込み開始。
📊 12ヶ月転帰
| 評価指標 | 発症時 | 3ヶ月 | 12ヶ月 |
|---|---|---|---|
| NIHSS | 7点 | 3点 | 2点 |
| Fugl-Meyer(上肢)傾向 | 重度麻痺 | 中等度改善 | 軽度残存 |
| DTI-FA(梗塞側路) | 低下開始 | 有意低下・安定化傾向 | 安定(変性完了) |
| mRS | 4 | 2 | 1 |
| 退院先 | 急性期病院 | 回復期病棟 | 自宅 |
⚠️ 本ケースは典型的な臨床経過を示す教育目的の架空事例です。数値・スコアはすべて例示であり、実際の患者データではありません。
エビデンスと最新知見
DTI-FA値は脳卒中後の運動機能回復の強力な予測因子
Qin et al.(2012, PLoS One)は脳卒中後患者においてDTIによる拡散指標(FA・MD)を追跡し、ワーラー変性に伴うFA低下と軸索完全性喪失・ミエリン破壊を定量的に評価。発症後の経時的変化がリハビリの転帰予測に有用であることを示しました。特に内包後脚・大脳脚のFA値は上肢運動機能(Fugl-Meyer)との強い相関を示し、治療戦略の個別化に貢献します。
橋梗塞後の中小脳脚に急性期からワーラー変性の制限拡散が検出可能
Zhang et al.(2018, Chinese Medical Journal)は橋梗塞後の患者において、梗塞巣とは別に中小脳脚(MCP)のMRI T2高信号とDTI変化を経時的に追跡。梗塞後数日〜数週間でワーラー変性が橋から中小脳脚に広がることを確認。変性の速度・範囲が後方循環系病変の転帰に影響することを示しました。
橋梗塞後に中小脳脚の制限拡散(DWI高信号)が急性期から出現
Musson & Romanowski(2010, Pol J Radiol)は橋梗塞後の患者において、中小脳脚(MCP)にDWI高信号・ADC低下(制限拡散)が急性期に出現することを報告。これは通常の梗塞拡張ではなく、急性ワーラー変性の反映と考えられます。後方循環病変でのDWI解釈において、梗塞と急性変性を区別することの重要性を示す事例として引用されています。
専門家向け:ワーラー変性と神経可塑性・脳回復の分子メカニズム
軸索変性のカルシウム依存性メカニズム(SARM1経路):近年の研究で、ワーラー変性の主要な分子スイッチとしてSARM1(Sterile Alpha and TIR Motif Containing 1)タンパク質が同定されました。SARM1はNAD+(ニコチンアミドアデニンジヌクレオチド)を分解することで軸索変性を駆動します。SARM1阻害薬は変性遅延の可能性があるとして研究中であり、将来的な神経保護療法への応用が期待されます。
中枢神経系での阻害因子:Nogo-A(RTN4)・MAG(ミエリン関連糖タンパク)・OMgp(オリゴデンドロサイトミエリン糖タンパク)はNgR(Nogo receptor)に結合してRhoA/ROCKシグナルを活性化し、成長円錐の崩壊・軸索再生阻害を引き起こします。RhoA/ROCK阻害薬(ファスジル等)は動物モデルで再生促進を示しており、臨床応用の研究が続いています。
DTI-FAと予後の生物学的根拠:DTI-FAの低下は「軸索方向性の喪失」を反映しています。軸索が変性するとミエリンが崩壊し、水の拡散が等方性(各方向均等)に近づくためFAが低下します。FA値はピクセル単位の微細構造を反映するため、残存する機能的回路の「容量」を推定する最良の非侵襲的指標です。MEP(運動誘発電位)との組み合わせによる予後予測精度がさらに高まることが複数の研究で示されています。
グリア瘢痕と新たな治療標的:反応性アストロサイトが形成するCSPG(コンドロイチン硫酸プロテオグリカン)豊富なグリア瘢痕は軸索再生の物理的バリアとなります。コンドロイチナーゼABC(細菌由来酵素)でCSPGを分解する実験的アプローチが脊髄損傷・脳卒中モデルで再生促進を示しており、臨床試験へ向けた研究が進行中です。
よくある質問(FAQ)
ワーラー変性は「新しい脳梗塞」と区別できますか?
ワーラー変性の特徴:①梗塞巣から連続する「既知の白質経路(皮質脊髄路・視放線など)」に沿って変化が広がる ②DWIでは急性梗塞とは異なる拡散パターン(早期は制限拡散、後期はADC上昇)③発症からの時間経過と一致した経路変化(亜急性〜慢性期に顕在化)。
新規梗塞との違い:新規梗塞はDWIで「新しい高信号病変」として出現し、臨床的な神経学的悪化を伴うことが多い。ワーラー変性は既存の経路に沿った緩徐な変化であり、突然の新たな神経症状を生じないのが原則です。
疑問がある場合は担当医に「今の画像変化はワーラー変性ですか、新しい梗塞ですか?」と直接確認することをお勧めします。これは治療方針を大きく左右する重要な区別です。
ワーラー変性が進んでいる患者はリハビリをあきらめるべきですか?
変性した皮質脊髄路が機能しなくなっても、脳には①同側路(同側の補助運動野・皮質脊髄路)②脳幹経由の迂回路(赤核脊髄路・網様体脊髄路)③健側半球からの経脳梁(トランスカロサル)的寄与 などの代替経路があります。これらを積極的に強化するのが、高強度のリハビリ・神経刺激療法(rTMS・tDCS)の目標です。
DTI-FA値が低い患者ほど「代償戦略を使いながらの積極的な課題指向型訓練」が回復の鍵になります。あきらめるのではなく、「どの経路を使って機能を取り戻すか」の戦略を組み直す機会です。
患者や家族が「ワーラー変性」と言われたらどう受け取るべきですか?
①ワーラー変性は予想された経過の一部:脳梗塞を起こした後、関連する神経経路がある程度変性することは「予測できた経過」であり、新たな病態の発生ではありません。②変性の速度が落ち着けば安定:DTI-FAが安定化すれば「進行が止まった」ことを意味します。③代償的可塑性と並行して進む:変性が起きる同時期に、脳の他の部分が機能を引き継ぐ代償的可塑性も進行します。この代償をリハビリが最大化します。
「悪い知らせ」ではなく、「現在の脳の状態を正確に理解して、最適なリハビリ計画を立てるための情報」として受け取ってください。
DTI検査はどこでも受けられますか?費用は?
費用:日本では通常のMRIは保険適用ですが、DTIの後処理解析(FA・tractography)は施設・目的によって保険適用外(自費)となる場合があります。実施可能かどうか・費用の目安については担当医に「DTI撮像と解析を追加できますか、費用はどうなりますか」と確認してください。
実施できない施設でも、通常のMRI T2/FLAIRによるワーラー変性の評価(白質路の高信号パターン)は多くの施設で可能です。DTIほど定量的ではありませんが、変性の存在と大まかな範囲は把握できます。
リハビリはどのくらいの頻度・時間が必要ですか?
急性期〜亜急性期(最重要時期):可能であれば1日2〜3時間の集中訓練(PT+OT+STを合算)。「練習量と回復量は比例する」という量依存的関係(dose-response relationship)は複数の大規模研究で支持されています。
CI療法実施時:標準プロトコルでは1日6時間・2週間(計60時間)の集中訓練が基本です。変形プロトコル(1日3時間・4週など)でも効果は認められています。
慢性期:週2〜3回以上の訓練継続が機能維持・緩やかな改善に有効です。ただし「とにかく量」ではなく、適切な難易度・バラエティ・集中した注意を要求する課題であることが神経可塑性促進の条件です。
日本の回復期リハビリ病棟では保険上の上限(PT・OT・ST合計最大3時間/日)がありますが、自主訓練・FES・家族補助による訓練を加えることで訓練量を補うことができます。担当セラピストに「家で追加できる自主訓練メニュー」を具体的に作成してもらうことをお勧めします。
家族はリハビリにどう関わればよいですか?
✅ 効果的な関わり方:
・セラピストから「家でできる自主訓練メニュー」を教わり、一緒に練習する(最重要)
・日常生活で麻痺側の使用を促す声かけ(「右手でコップを持ってみよう」など)
・困ったときだけ手を添える「見守り支援」で自発的な努力を引き出す
・認知・情動の変化(急に怒りっぽい・落ち込みが続く)を観察し担当者に報告する
・カンファレンスに参加し、リハビリ目標・退院後の計画を医療チームと共有する
⚠️ 避けたい関わり方:
・すべての動作を代わりにやってしまう(廃用性萎縮・使用非依存性悪化のリスク)
・「もう無理」「あきらめよう」といったネガティブな言葉かけ
・セラピストの指示と異なる独自の方法での訓練(代償パターンの固定化リスク)
家族のサポートが「患者が自分でやる機会を奪わない」バランスで行われることが、長期的な自立度向上につながります。担当PT・OT・STに「自宅での関わり方を具体的に教えてほしい」と遠慮なく相談してください。
STROKE LABのワーラー変性への取り組み
STROKE LABでは、DTI所見・神経学的評価・機能評価(Fugl-Meyer・FIM・SIAS)を統合した「神経回路地図に基づくリハビリ設計」を行っています。ワーラー変性の存在を「あきらめの根拠」にするのではなく、「どの代替経路を活性化するか、どの時期に何の介入を行うか」の戦略立案の出発点として活用します。
脳梗塞から1年経って「もう回復は止まった」と言われていました。STROKE LABで初めてDTIの話を聞き、「右の経路は変性しているけれど、同側の経路を使って動きを引き出せる可能性がある」と説明していただいて、あきらめていたリハビリを再開しました。CI療法の2週間集中プログラム後、右手でスプーンが持てるようになりました。数字で状態を説明してもらえることが、こんなにも力になるんだと感じました。
60代女性・左内包梗塞発症から18ヶ月
「ワーラー変性が見られます」とMRIの結果で言われた時、家族全員でパニックになりました。STROKE LABで「これは経過の一部で、これをふまえて次の訓練方針を変えます」と具体的に説明してもらえて初めて前向きになれました。医療者と家族が同じ言葉で話せることの大切さを実感しました。
患者家族(70代男性・右中大脳動脈梗塞)
参考文献
- 1) Waller A. Experiments on the section of the glossopharyngeal and hypoglossal nerves of the frog, and observations of the alterations produced thereby in the structure of their primitive fibres. Philos Trans R Soc Lond. 1850;140:423-429.
- 2) Qin W, Zhang M, Piao Y, et al. Wallerian Degeneration in Central Nervous System: Dynamic Associations Between Diffusion Indices and Their Underlying Pathology. PLoS One. 2012;7(7):e41038. PMC3400645
- 3) Zhang Z, Liu Z, Qin W, Chen Y, Liu Z. Clinical and Radiological Features of Wallerian Degeneration of the Middle Cerebellar Peduncles Secondary to Pontine Infarction. Chin Med J. 2018;131(6):665-671. PMC5865311
- 4) Musson R, Romanowski C. Restricted Diffusion in Wallerian Degeneration of the Middle Cerebellar Peduncles Following Pontine Infarction. Pol J Radiol. 2010;75(4):38-43. PMC3389899
- 5) Becerra J, Puckett W, Hiester E, et al. MR-Pathologic Comparisons of Wallerian Degeneration in Spinal Cord Injury. AJNR Am J Neuroradiol. 1995;16(1):125-133.
- 6) Concha L, Gross DW, Beaulieu C. Diffusion tensor tractography of the limbic system. AJNR Am J Neuroradiol. 2005;26(9):2267-2274.
- 7) Feng W, Wang J, Chhatbar PY, et al. Corticospinal tract lesion load: An imaging biomarker for stroke motor outcomes. Ann Neurol. 2015;78(6):860-870.
- 8) Lemon RN. Descending pathways in motor control. Annu Rev Neurosci. 2008;31:195-218.
- 9) Sofroniew MV, Vinters HV. Astrocytes: biology and pathology. Acta Neuropathol. 2010;119(1):7-35.
- 10) Bhatt DL, Bhattacharyya S, et al. Wallerian Degeneration Beyond the Corticospinal Tracts: Conventional and Advanced MRI Findings. J Neuroimaging. 2016. DOI:10.1111/jon.12404
- 11) Stinear CM, Barber PA, Smale PR, et al. Functional potential in chronic stroke patients depends on corticospinal tract integrity. Brain. 2007;130(Pt 1):170-180. 【PREP/PREP2アルゴリズムの原型となった研究。DTI-FA+MEPによる予後予測】
- 12) Stinear CM, Byblow WD, Ackerley SJ, et al. PREP2: A biomarker-based algorithm for predicting upper limb function after stroke. Ann Clin Transl Neurol. 2017;4(11):811-820.
- 13) Loubinoux I, Carel C, Pariente J, et al. Correlation between cerebral reorganization and motor recovery after subcortical infarcts. Neuroimage. 2003;20(4):2166-2180. 【皮質下梗塞後の脳再編成と運動回復の相関。可塑性の経時的変化を示す】
- 14) Ward NS, Brown MM, Thompson AJ, Frackowiak RS. Neural correlates of outcome after stroke: a cross-sectional fMRI study. Brain. 2003;126(Pt 6):1430-1448.
- 15) Kwakkel G, Kollen BJ, van der Grond J, et al. Probability of regaining dexterity in the flaccid upper limb: impact of severity of paresis and time since onset in acute stroke. Stroke. 2003;34(9):2181-2186. 【脳卒中後の上肢機能回復の確率と重症度・経過時間の関係を示す代表的研究】

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)