【2026年版】低酸素脳症(HIE)とは?原因・MRI診断・低体温療法からリハビリまで徹底解説
今回は、心停止・窒息・出産時トラブルなどで脳が酸素不足に陥ることで起こる深刻な脳障害、低酸素脳症(Hypoxic-Ischemic Encephalopathy:HIE)について、開発背景から原因・MRI診断・治療(低体温療法)・リハビリテーションまで徹底解説します。「成人と小児でどう違う?」「MRI所見の3パターンは?」「低体温療法はいつ・どう使う?」「言語療法・理学療法・作業療法での具体的介入は?」という現場のリアルな疑問にすべて答えます。
低酸素脳症(Hypoxic-Ischemic Encephalopathy:HIE)は、脳が十分な酸素を受け取れない(低酸素)または血流が不足する(虚血)状態により生じる脳の機能障害・構造的損傷です。心停止・窒息・出産時合併症など多様な原因で発症し、迅速な治療(心肺蘇生・低体温療法・酸素療法)がなければ重篤な後遺症や死亡に至ります。成人・小児ともに早期診断と多職種チームによるリハビリテーションが長期的な機能回復の鍵を握ります。
- 正式名称:Hypoxic-Ischemic Encephalopathy(低酸素虚血性脳症)。低酸素(O₂供給不足)と虚血(血流不足)の双方を含む広義の呼称
- 成人の最多原因:心停止(院外・院内ともに)。次いで窒息・重篤な低血圧・一酸化炭素中毒・薬物過剰摂取
- 小児(新生児)の最多原因:周産期仮死(胎盤剥離・臍帯問題・子宮破裂・難産)。生存出生1000人に1〜2人発生(高所得国)
- 病態の時間軸:酸素停止後10秒で意識消失・4〜5分で不可逆的神経損傷が始まる。再灌流後の二次障害(興奮毒性・フリーラジカル)が6〜24時間にわたって継続
- MRI損傷パターン:① Watershed(分水嶺型)② BG-TH(基底核・視床型)③ Global(全脳型)の3パターン。DWIが最も高感度(発症24時間以降)
- 治療的低体温法:新生児HIEは33〜34°C・72時間(Grade A)。成人心停止後はTTM2試験(2021)以降「発熱回避(37.5°C以下:ERC/ESICM 2021)」が主流。「33°C vs 37.5°C以下」で有意差なし
- リハビリ介入の原則:急性期からの早期離床・多職種連携が必須。PT(運動機能)・OT(ADL・認知)・ST(言語・嚥下)が同時並行で介入
- 予後を決める3因子:① 無酸素時間の長さ ② 脳損傷の部位・範囲(MRI) ③ 低体温療法の開始タイミング
- EEGの役割:痙攣の検出(臨床的に見えないNCSEを含む)・予後予測(burst suppressionは不良)・低体温療法中のモニタリング
- Apgarスコアとの関係:5分Apgar ≦3は重症HIEの独立予測因子。ただしApgar正常でもHIEが潜在している場合あり。臍帯血ガス分析(pH<7.0 または BE ≦ −16 mEq/L)との組み合わせで評価(TOBY試験基準)
低酸素脳症とは ― 定義・病態・発生機序
低酸素脳症(HIE)は、脳への酸素供給低下(低酸素:hypoxia)と血流低下(虚血:ischemia)が合わさって生じる脳の機能障害・構造的損傷の総称です。両方が重なることで単独のどちらよりも強い障害をもたらすことが病態の特徴です。
⏱ HIEの時間軸と二次損傷機序
脳は体重の2%を占めるに過ぎませんが、全身の酸素消費量の約20%を使用します。このため、酸素供給が途絶えると極めて短時間で障害が始まります。
一次障害(Primary Injury):酸素停止後10秒で意識消失・30〜40秒でEEG上の脳波消失・4〜5分以上継続すると不可逆的な神経細胞死が始まります。ATPが枯渇し、イオンポンプが機能しなくなることで細胞内にCa²⁺が流入し、神経細胞が崩壊します。
二次障害(Secondary Injury):再灌流後6〜24時間にわたって「興奮毒性(グルタミン酸過剰放出)」「フリーラジカル(活性酸素種)産生」「炎症カスケード(TNF-α・IL-1β・IL-6)」「アポトーシス」が連続して進行し、一次障害を超える広範な損傷をもたらすことがあります。低体温療法はこの二次損傷を抑制することを主目的としています。
HIEの発生メカニズム:4段階プロセス
(原因発生)
(4〜5分〜)
(6〜24時間)
(48〜72時間)
HIEの病態は4段階で進行。低体温療法は③〜④の二次損傷フェーズへの介入が主目的
🧠 脳の脆弱性が高い部位
代謝需要が高い部位ほど早期に障害されます。基底核・視床・海馬CA1・プルキンエ細胞(小脳)は特に脆弱。これがMRIのBG-THパターンや記憶障害・運動障害の基盤となります。
💧 分水嶺領域の脆弱性
前大脳動脈・中大脳動脈・後大脳動脈の境界領域(分水嶺ゾーン)は血流が最も弱く、低血圧・心停止時に最初に虚血にさらされます。これがWatershedパターンの解剖学的基盤です。
原因 ― 成人・小児別の主要因
成人における主要原因(5大原因)
心停止(Cardiac Arrest)― 成人HIEの最多原因
窒息(Asphyxia)― 呼吸路の閉塞・水中溺水
重篤な低血圧(Profound Hypotension)
一酸化炭素中毒(Carbon Monoxide Poisoning)
薬物過剰摂取(Drug Overdose)
小児(新生児)における原因分類
| 発症時期 | 主要原因 | 臨床的特徴 |
|---|---|---|
| 出産前(胎児期) | ||
| 胎盤早期剥離 | 胎盤が子宮壁から早期剥離→胎児への血流急減 | 母体の強い腹痛・性器出血・胎児心拍数低下 |
| 子宮破裂 | 子宮壁の裂開→胎児への酸素供給遮断 | 帝王切開既往・過強陣痛が誘因になることあり |
| 重度の母体低血圧 | 母体の血圧急落→胎児血流不足 | 脊椎麻酔・大量出血・仰臥位低血圧が原因 |
| 出産時(周産期) | ||
| 臍帯の問題 | 臍帯脱出・臍帯巻絡・臍帯結節による血流遮断 | 分娩監視装置上の遅発一過性徐脈が指標 |
| 難産(分娩遷延) | 頭部が骨盤内に長時間圧迫→脳血流遮断 | 吸引・鉗子分娩が必要なケース |
| 母体の心臓合併症 | 出産時の急性心機能低下→胎児酸素供給不足 | 周産期心筋症・不整脈が原因になることあり |
| 出産後(新生児期) | ||
| 呼吸不全 | 新生児の不十分な呼吸→酸素供給低下 | 呼吸窮迫症候群(RDS)・胎便吸引症候群(MAS) |
| 持続的な心停止・不整脈 | 新生児期の心臓機能停止→脳血流遮断 | 先天性心疾患・電解質異常が背景に |
| 重症感染症(敗血症) | 全身性炎症反応→血流障害・低血圧 | GBS(B群連鎖球菌)・大腸菌が新生児敗血症の主因 |
診断 ― 臨床評価・MRI・EEG

HIE診断の全体フロー
臨床評価 ― バイタル・神経学的評価・意識レベル
意識レベル(GCS・JCS)・瞳孔反応・呼吸パターン・血圧・SpO₂をベッドサイドで評価。新生児ではApgarスコア(特に5分スコア≦3が重症HIEの指標)・臍帯血ガス分析(pH<7.0またはBE≦−12が基準)を使用。神経学的評価では、痙攣・筋緊張低下・哺乳力低下・原始反射消失が重要なサインです。
画像診断(MRI・CT)― 損傷部位・パターンの同定
MRI(特にDWI:拡散強調画像)が最も高感度。発症後24時間以降に感度が上昇し、48〜72時間で最も鮮明になります。CTは急性期(出血除外・緊急時)に有用ですが感度はMRIに劣ります。新生児では頭部超音波(HUS)がベッドサイドスクリーニングとして有用です。
EEG(脳波検査)― 痙攣検出・予後予測・低体温療法中モニタリング
臨床的に見えない非痙攣性てんかん重積(NCSE)の検出に必須。低体温療法中の持続的EEGモニタリング(cEEG)は標準的管理手段です。EEG背景活動パターンは予後予測の強力な指標となります。
EEG背景活動パターンと予後の対応
| EEGパターン | 特徴 | 予後の目安 |
|---|---|---|
| 正常〜軽度異常 | 基本的な背景活動は保たれる。周期的変動あり | ✅ 良好(Sarnat Grade Ⅰに対応) |
| 中等度異常(discontinuous) | 不連続性あり。Low voltageだが反応性あり | ⚠️ 中等度(Sarnat Grade Ⅱに対応) |
| Burst Suppression(バースト抑制) | 高振幅バーストと等電位サイレントの交互出現。低体温中に出現することもある(解釈に注意) | 🔴 不良(特に低体温療法終了後も持続する場合) |
| 等電位(Flat/Isoelectric) | ほぼ平坦・脳波活動がほぼ消失 | 🔴🔴 重度不良(Grade Ⅲ・広範な皮質損傷) |
| てんかん性放電(電気的痙攣) | 臨床的痙攣を伴わないNCSE(非痙攣性てんかん重積)を含む | 🔴 急性期の予後悪化因子。積極的な抗痙攣治療が必要 |
🧠 成人心停止後HIE:予後予測のマルチモーダルアプローチ(ERC/ESICM 2021)
単一の検査での予後予測は誤差が大きく、現在は複数の検査を組み合わせるマルチモーダル予後予測が国際標準(ERC/ESICM 2021ガイドライン)です。ROSC後72時間以降(発熱回避管理終了後)に以下の指標を統合評価します:
① 神経学的診察:瞳孔反射(光反射消失)・角膜反射・痛み刺激への反応(GCS M1〜2)を評価。特に両側瞳孔反射の消失は高特異度の不良指標。
② EEG:バースト抑制・等電位・反応性消失は予後不良。一方、早期のEEGでの「反応性あり」は予後良好の指標。
③ 体性感覚誘発電位(SSEP):両側N20成分の消失は特異度〜100%の予後不良指標(ERC/ESICM 2021 Strong recommendation)。
④ 血液バイオマーカー:NSE(神経特異エノラーゼ)>60 μg/L(72時間値)は予後不良と相関。S100Bタンパクも補助指標として使用。
⑤ 脳画像:CT上の灰白質・白質の分界消失(GWR低下)・MRI DWIの広範な制限拡散が予後不良指標。
⚠️ 重要:いずれの単一指標も偽陽性(実際は回復するのに「不良」と予測)のリスクがゼロではありません。家族との意思決定プロセスには十分な時間(少なくとも72時間以上)と複数指標の確認が不可欠です。
血液検査・電気生理学的検査
臍帯血ガス分析(新生児)・血液ガス・乳酸値・神経特異エノラーゼ(NSE)・S100Bタンパク(成人の予後バイオマーカー)。体性感覚誘発電位(SSEP)はN20成分の消失が予後不良の強い指標として使用されます(感度・特異度とも高い)。
MRI損傷パターン3分類(DWI/ADC所見)
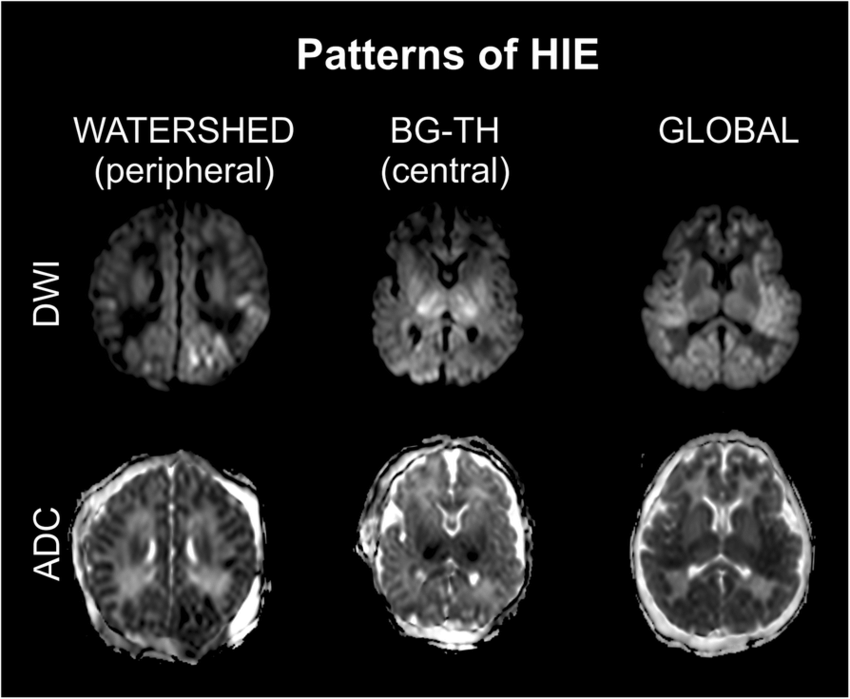
画像引用:Neurodevelopmental effect of intracranial hemorrhage observed in hypoxic ischemic brain injury in hypothermia-treated asphyxiated neonates(ResearchGate)
| パターン | MRI上の障害部位 | 主な発症状況 | 予後 |
|---|---|---|---|
| ① Watershed(分水嶺型) | 頭頂部外側・前頭・後頭の分水嶺領域の皮質・白質 | 低血圧・部分的・慢性的な低灌流 | 中等度(機能回復の余地あり) |
| ② BG-TH(基底核・視床型) | 両側基底核(尾状核・被殻)・視床の対称的障害 | 急激な全身性低酸素(心停止・周産期仮死) | 中等〜重度(運動障害・認知障害が残存しやすい) |
| ③ Global(全脳型) | 大脳皮質全体・白質・深部核すべてに広範な障害 | 長時間の心停止・最重症の低酸素状態 | 重度(死亡率高・重篤な後遺症) |
🔬 各MRIパターンの臨床的意味
Watershed(分水嶺型):脳の「水圧が最も弱い末端領域」に相当する分水嶺ゾーンが選択的に障害されます。DWI画像では頭頂部外側に異常信号が出現。比較的緩徐な低灌流(手術中の低血圧・重症心不全)に典型的です。回復の余地が3パターン中では最も大きい傾向があります。
BG-TH(基底核・視床型):エネルギー需要が最も高い脳深部核(基底核・視床)が選択的に障害されます。急激かつ完全な低酸素(心停止・窒息)に典型的。DWI/ADCで両側対称性の異常が特徴的。後遺症として運動障害(アテトーゼ・ジストニア)・認知機能障害が残存しやすいです。
Global(全脳型):長時間の心停止や最重症の低酸素状態で大脳皮質全体が障害されます。MRIでは脳溝の消失・灰白質全体のDWI異常が見られます。予後は最も重篤で、死亡または遷延性意識障害となることが多いです。
小児(新生児)HIEの診断特有ポイント
📊 Apgarスコアの活用
1分・5分・10分後に評価。5分Apgar≦3が重症HIEの指標。ただしApgar正常でも臍帯血ガスのpH低下があればHIEを除外できません。Apgar単独での判断は不十分です。
🩸 臍帯血ガス分析
分娩直後の臍帯血でpH・BE(塩基過剰)・乳酸を測定。pH<7.0またはBE≦−16 mEq/L(TOBY試験基準)が重症HIEの判断基準の一つ。施設プロトコルによりBE閾値は−12〜−16 mEq/Lまで幅があります。
Sarnat分類(新生児HIE重症度の世界標準分類)
| Grade | 臨床所見・特徴 |
|---|---|
| Grade Ⅰ (軽度) |
過覚醒・易刺激性・筋緊張亢進・哺乳力やや低下。EEG正常〜軽度異常。24〜48時間以内に正常化することが多く、予後良好(神経学的後遺症は稀)。低体温療法の適応については施設・ガイドラインごとに議論あり |
| Grade Ⅱ (中等度) |
意識レベルの低下・筋緊張低下・原始反射減弱・臨床的または電気的痙攣あり。EEG上の周期的異常パターン。低体温療法の主要適応対象。適切な治療で約50〜60%が正常または軽微な障害にとどまる |
| Grade Ⅲ (重度) |
昏睡状態・筋緊張著明低下(flaccidity)・原始反射消失・自律神経障害(不整脈・瞳孔散大固定)・難治性痙攣。EEG:Burst suppression〜等電位(flat)。死亡率高(30〜50%)・生存者の多くに重篤な後遺症(脳性麻痺・重度知的障害) |
治療 ― 低体温療法・薬物・蘇生
💊 HIE治療の基本原則:「時間が脳を救う」
HIEの治療において最も重要なのは「時間」です。心停止から4〜5分以内のCPR開始・低体温療法は発症から6時間以内の開始が神経保護効果の前提条件です。チームとしての迅速な対応が転帰を左右します。
治療は段階的に:① 蘇生(ABCの確保) → ② 低体温療法(二次損傷抑制) → ③ 痙攣管理 → ④ 臓器サポート → ⑤ リハビリテーションの流れで進みます。
① 蘇生(Resuscitation)
心肺蘇生(CPR)・アドバンスト気道管理
② 治療的低体温法(Therapeutic Hypothermia)― 最重要治療
低体温療法 ― 二次神経損傷を抑制する標準治療
低体温療法は体温を33〜36°Cに下げることで脳の代謝需要を低下させ、興奮毒性・フリーラジカル産生・炎症カスケードを抑制して二次神経損傷を最小化します。
新生児HIE(≥36週)への適応:2000年代に行われた複数の大規模RCT(CoolCap試験・TOBY試験・NICHD試験)で有効性が確認され、現在は標準治療(Grade A推奨)です。目標体温は33〜34°C・72時間(全身冷却または頭部選択的冷却)。死亡または重篤な後遺症のリスクを25〜30%低減します。
成人心停止後への適応:ROSC後も意識が回復しない患者に使用されてきましたが、TTM2試験(Dankiewicz J, NEJM 2021)では33°Cの積極的冷却と「37.5°C以下の発熱回避管理」で転帰(6ヶ月後の死亡率・神経機能)に有意差がなかったことが示されました。現在のERC/ESICM 2021ガイドラインでは「ROSC後72時間にわたる37.5°C以下の発熱回避」を標準推奨としており、積極的な33°Cへの冷却はハイリスク選択患者に個別判断で行われています。
⚠️ 低体温療法の合併症と管理注意点
低体温関連合併症:凝固障害(PT・APTT延長)・低血圧・不整脈(徐脈)・低血糖・感染リスク増大・電解質異常(低K・低Mg)。これらはモニタリングと補正によって管理します。
復温(Rewarming)の注意:復温速度は0.2〜0.5°C/時以下でゆっくり行います。急速復温は二次損傷の引き金になります。復温後にも発熱(38.5°C以上)の回避が重要です(高体温は神経損傷を悪化させます)。
③〜④ 薬物療法(神経保護・痙攣管理)
痙攣管理(抗痙攣薬)
神経保護薬(補助療法)― 最新エビデンスに基づく整理
かつて有望視されていた薬剤について、近年の大規模RCTで再評価が進んでいます。
⚠️ エリスロポエチン(EPO):HEAL試験(Wu YW et al., NEJM 2022)で、低体温療法を受けた新生児HIEへのEPO(1000 U/kg×6回)投与は2歳時点の神経発達アウトカムをプラセボと比べて改善しないことが示されました(Neutral trial)。現時点では新生児HIEへの補助的EPO投与は推奨されません。
⚠️ アロプリノール:ALBINO試験(Garlach RT et al., NEJM 2023)では、出生直後の産母・新生児へのアロプリノール投与が重篤な神経発達障害または死亡を有意に減少させないことが示されました。現時点では推奨されません。
✅ 引き続き研究中(有望な実験的治療):
・メラトニン:抗酸化・抗炎症・抗アポトーシス作用。低体温療法との併用を検討する小規模試験で安全性確認(大規模RCT進行中)。
・幹細胞療法(臍帯血・MSC):Phase I/II試験で安全性と神経保護の可能性を示す結果あり。大規模有効性試験は未完了。
・キセノンガス(Xe):NMDA受容体拮抗・神経保護作用。TOBY-Xe試験では単独での有意な効果なし。低体温との最適併用方法を探索中。
・硫酸マグネシウム:早産児の脳保護として確立(Grade A)。正期産HIEへの効果は研究段階。
リハビリテーション ― PT・OT・STの実践アプローチ

🏥 HIEリハビリの基本方針:「早期・包括的・多職種連携」
HIEの機能回復において、急性期からの早期リハビリテーション介入が長期転帰を大きく改善することが多くの研究で示されています。脳の可塑性(neuroplasticity)を最大限に活用するために、ICU・急性期病棟の段階からPT・OT・STが連携して介入します。
HIEによる機能障害は①運動機能障害(片麻痺・筋緊張異常・失調)②認知機能障害(記憶・注意・実行機能)③言語・コミュニケーション障害(失語症・構音障害)④嚥下障害の4領域に及ぶことが多く、各職種が独立かつ連携して介入します。
理学療法(Physical Therapy:PT)
ICU・急性期からの早期離床プログラム
意識レベルが安定次第、ベッド上での体位変換(2時間ごと)→ヘッドアップ→端座位→立位→歩行の段階的プロトコルを実施します。早期離床は廃用症候群(筋萎縮・関節拘縮・骨粗鬆症・起立性低血圧)の予防に直結します。意識障害が残存する患者でも、バイタルが安定していれば傾斜台(チルトテーブル)を用いた立位訓練を開始します。血圧・SpO₂・心拍数を継続モニタリングしながら安全に進めます。
プログレッシブ筋力強化と有酸素運動
HIEでは長期の意識障害・ICU管理により重篤なICU-AW(ICU獲得性筋力低下)が生じることが多いです。回復期では抵抗バンド・自重・軽ダンベルを用いたプログレッシブレジスタンストレーニング(特に下肢)と有酸素運動(歩行・エルゴメーター)を組み合わせます。運動強度はボルグスケール(RPE 13〜15程度)と心拍数モニタリングで個別設定します。
姿勢制御・歩行パターン最適化
小脳・基底核・運動野が障害されるHIEではバランス障害・歩行障害が高頻度に残存します。バランスボード・フォームパッドを使ったスタティック/ダイナミックバランス訓練、歩行分析(3Dモーションキャプチャーによる定量的評価)に基づくパターン修正訓練、必要に応じてロボット支援歩行(Lokomat・WPAL)を活用します。転倒リスク評価(TUG・BBS)を定期実施し、住環境整備と連携します。
作業療法(Occupational Therapy:OT)
日常生活動作の段階的自立支援
FIM・Barthel Indexで基本ADL(食事・整容・更衣・トイレ・入浴・移動)を評価し、個別のゴール設定と段階的訓練を行います。上肢機能障害(片麻痺・失調・筋緊張亢進)にはCI療法(Constraint-Induced Movement Therapy:非麻痺側を制限して麻痺側を集中使用)・電気刺激療法(FES・NMES)・ボツリヌス毒素療法の適応を検討します。
認知・注意・記憶・遂行機能への介入
HIEでは海馬・前頭葉・基底核障害を背景として記憶障害・注意障害・遂行機能障害・半側空間無視が生じることがあります。神経心理学的検査(MMSE・MoCA・FAB・TMT・Catherine Bergego Scale)で障害プロファイルを特定し、コンピューター支援認知訓練・メモリーノート活用・環境調整(スケジュール表示・ホワイトボード)・IADL訓練(調理・買い物・金銭管理)を組み合わせます。
言語聴覚療法(Speech-Language Therapy:ST)
失語症・構音障害への個別化アプローチ
標準失語症検査(SLTA)・WAB・SALA検査で言語プロファイルを評価。ブローカ失語(非流暢・理解比較的良好)にはメロディックイントネーション療法(MIT)・機能的コミュニケーション訓練を実施します。重度失語症・無言症にはAAC(補助代替コミュニケーション)デバイス(VOCA・文字盤・タブレットアプリ)を早期から導入します。構音障害には口腔・口唇・舌・喉頭の運動訓練と発話速度調整を組み合わせます。
誤嚥リスク管理と段階的経口摂取
HIEでは球麻痺・仮性球麻痺・協調性障害を背景として重篤な嚥下障害が生じることがあります。VF(嚥下造影)・VE(嚥下内視鏡)による嚥下機能精査を行い、安全な食形態と姿勢(頸部屈曲・健側向き)を決定します。段階的経口摂取プロトコル(FOIS)に沿って進め、誤嚥性肺炎の予防(口腔ケア・食事中の監視)を家族・看護師とともに徹底します。
👪 家族・介護者教育の重要性
HIEのリハビリで見落とされがちなのが家族・介護者への教育とサポートです。日常生活環境でのリハビリ効果を維持・発展させるには、家族が正しいアシスト方法・コミュニケーション戦略・AAC活用法・嚥下介助の方法を習得することが不可欠です。
具体的には:①発話が困難な患者への対応(「はい/いいえ」で答えられる質問形式)②麻痺側の取り扱い(過度な代償使用を防ぐ)③リハビリ効果が出やすい時間帯の活用(覚醒が高い午前中)④介護者の精神的サポート(バーンアウト予防のためのレスパイトケア紹介)などを指導します。
転帰予測と後遺症
HIEの後遺症スペクトラム ― 重症度別・年齢別の転帰データ
📊 新生児HIE後の脳性麻痺(CP)発生率と転帰データ
低体温療法なし(ヒストリカルコントロール):中等度〜重度HIE新生児の約25〜30%に脳性麻痺が発症。重度HIEでは生存者の60〜70%以上に重篤な神経発達障害が残存(Volpe JJ, 2008)。
低体温療法あり(RCTデータ):Shankaran et al. NICHD試験(2012・18〜22ヶ月フォローアップ)では、低体温療法群で「死亡または中等〜重篤な障害」のリスクが有意に低下(NNT≒7)。長期フォローアップ(6〜7歳)でも神経認知・学業成績の改善が確認されています(Shankaran S et al., NEJM 2012)。
後遺症として頻度が高いもの(中等〜重度HIEの生存者):脳性麻痺(CP)25〜35%・認知・知的障害 20〜40%・てんかん 15〜25%・視覚障害 10〜20%・聴覚障害 5〜10%・ASD類似症状・行動障害(長期フォロー研究で報告)。
| 後遺症の領域 | 具体的な症状・障害 | 主に障害される脳部位 | 主担当職種 |
|---|---|---|---|
| 運動機能障害 | 片麻痺・四肢麻痺・痙縮・失調・ジストニア・パーキンソン様症状 | 運動野・基底核・小脳・錐体路 | PT・OT |
| 認知機能障害 | 記憶障害・注意障害・遂行機能障害・失認・半側空間無視 | 海馬・前頭葉・頭頂葉・視床 | OT・ST |
| 言語・コミュニケーション障害 | 失語症(ブローカ・ウェルニッケ・全失語)・構音障害・無言症 | 左半球言語野・運動野・補足運動野 | ST |
| 嚥下障害 | 嚥下反射遅延・誤嚥・球麻痺・食事自立困難 | 脳幹・両側半球(仮性球麻痺) | ST・OT・PT |
| てんかん | 痙攣発作(焦点性・全般性)・NCE(非痙攣性てんかん) | 皮質瘢痕・海馬・基底核 | 医師・看護師 |
| 精神・情動障害 | うつ・不安・PTSD・易怒性・情動調節障害 | 前頭葉・辺縁系・扁桃体 | 心理士・ST・医師 |
| 視覚障害 | 皮質盲・視野障害・眼球運動障害 | 後頭葉・視放線・脳幹 | OT・医師 |
📊 予後を決める主要因子(Evidence-based)
① 無酸素時間(最重要):心停止から蘇生開始まで、または確実な循環回復(ROSC)までの時間が長いほど脳損傷は広範になります。
② MRI所見の損傷パターンと範囲:GlobalパターンはWatershedパターンより予後不良。DWI異常の体積・ADC値の低下度が予後と相関します。
③ 低体温療法の開始タイミング:発症6時間以内の開始が必須条件。遅れるほど二次損傷フェーズに間に合わなくなります。
④ 電気生理学的所見:SSEPのN20消失・EEGのBurst Suppression・脳波の平坦化は予後不良の強い指標。
⑤ 血液バイオマーカー:NSE(神経特異エノラーゼ)の高値・S100Bタンパクの高値が重篤な脳損傷の指標として使用されます。
よくある質問(FAQ)
低酸素脳症と脳梗塞はどう違いますか?
局在性(focal)の脳梗塞に対し、HIEはよりびまん性(diffuse)・両側性の脳障害となることが多いです。ただし分水嶺梗塞(watershed infarction)はHIEと脳梗塞の中間的な病態として位置付けられます。
治療においても、脳梗塞ではtPAや血栓回収療法が主役ですが、HIEではCPR・低体温療法・痙攣管理・全身管理が主軸となり、アプローチが大きく異なります。
低体温療法はどんな患者に使いますか?除外基準は?
① 在胎36週以上の新生児 ② 生後6時間以内 ③ 中等〜重症HIEの証拠(5分Apgar≦5、臍帯血pH<7.0またはBE≦−16 mEq/L(TOBY試験基準)、蘇生に10分以上要したなど)④ 神経学的評価またはEEGで異常あり。これらを組み合わせた施設プロトコルに従い判断します。
成人心停止後の低体温療法適応:ROSC後に意識が回復しない患者(GCS≦8)で、除外基準(活動性出血、心停止前の末期疾患など)がなければ適応。TTM2試験(NEJM 2021)では33°Cの積極冷却と発熱回避管理で転帰に有意差なし。現在のERC/ESICM 2021ガイドラインでは「37.5°C以下の発熱回避(72時間)」を標準推奨としており、積極的な33°Cへの冷却は個別判断で行われます。
主な除外基準:心停止前の重篤な機能障害・活動性の大量出血・凝固障害・真性多血症・妊娠・ターミナルケース選択時など。
HIE後の意識が戻らない場合、リハビリの意味はありますか?
意識障害患者へのリハビリ介入の意義:
① 廃用症候群の予防(拘縮・褥瘡・深部静脈血栓):適切なポジショニング・他動可動域訓練・早期離床が関節拘縮・圧迫性潰瘍を防ぎます。
② 意識回復の機会を最大化:感覚刺激(音楽・声かけ・触覚)が意識回復を促進する可能性があります(Sensory Stimulation Program)。
③ 家族のQOL支援:ケアの方法を家族と共有することで介護者の不安・負担を軽減します。
意識障害の分類・評価にはCRS-R(Coma Recovery Scale-Revised)を使用し、定期的に意識水準を評価することで適切な介入の調整が可能です。
新生児HIEと大人のHIEではリハビリが違いますか?
新生児HIE:発達中の脳への障害であるため、成人の脳損傷後と異なる「神経発達支援(neurodevelopmental support)」の観点が必要です。
・NICU内でのdevelopmental care(ポジショニング・感覚統合刺激・親子間愛着促進)
・退院後は小児リハビリ専門チーム(PT・OT・ST)による発達フォローアップ
・学齢期まで継続的な神経発達評価(GMFCS・MACS・BSID等)と療育の調整
・後遺症として脳性麻痺・知的障害・てんかん・ASD類似症状が現れることがあり、学校・福祉との連携が不可欠です。
成人HIE:既に完成した脳への損傷のため、成人脳損傷のリハビリ原則(早期離床・廃用予防・機能回復訓練)を適用します。ただし心停止後HIEは高齢者に多く、フレイル・認知機能低下・心機能低下を考慮した個別化プログラムが重要です。
退院後はどのようなサポートが必要ですか?
医療面:外来神経学フォロー(てんかん管理・痙縮治療)・外来リハビリ(PT・OT・ST)・訪問リハビリの調整・必要時は介護施設への移行。
福祉・社会面:障害者手帳の取得サポート・障害福祉サービスの利用(居宅介護・就労支援・グループホーム)・介護保険の申請(高齢者の場合)・就労可能な患者への職業リハビリテーション。
家族サポート:介護者のバーンアウト予防(レスパイトケアの利用勧奨)・患者家族会・支援グループへの紹介・心理カウンセリングの利用。
STROKE LABでは退院後のリハビリ継続支援として外来・訪問での評価・介入を提供しています。HIE後の「現状の整理」と「これからの目標設定」のご相談を随時受け付けています。
参考文献・引用文献
- 1) Shankaran S, Laptook AR, Ehrenkranz RA, et al. Whole-body hypothermia for neonates with hypoxic–ischemic encephalopathy. N Engl J Med. 2005;353(15):1574-1584. 【NICHD試験:新生児HIEへの低体温療法の有効性を示した大規模RCT】
- 2) Shankaran S, Pappas A, McDonald SA, et al. Childhood outcomes after hypothermia for neonatal encephalopathy. N Engl J Med. 2012;366(22):2085-2092. 【NICHD長期フォローアップ:6〜7歳での神経認知改善確認】
- 3) Gluckman PD, Wyatt JS, Azzopardi D, et al. Selective head cooling with mild systemic hypothermia after neonatal encephalopathy: multicentre randomised trial. Lancet. 2005;365(9460):663-670. 【CoolCap試験:頭部選択的冷却の有効性】
- 4) Azzopardi D, Strohm B, Edwards AD, et al. Moderate hypothermia to treat perinatal asphyxial encephalopathy. N Engl J Med. 2008;359(18):1817-1826. 【TOBY試験:全身冷却の有効性。BE≦−16 mEq/L基準を使用】
- 5) Dankiewicz J, Cronberg T, Lilja G, et al. Hypothermia versus Normothermia after Out-of-Hospital Cardiac Arrest. N Engl J Med. 2021;384(24):2283-2294. 【TTM2試験:33°Cと37.5°C以下の発熱回避管理で転帰に有意差なし】
- 6) Wu YW, Comstock BA, Gonzalez FF, et al. Trial of Erythropoietin for Hypoxic-Ischemic Encephalopathy in Newborns. N Engl J Med. 2022;387(2):148-159. 【HEAL試験:EPO投与は新生児HIEの神経発達アウトカムを改善しない(Neutral)】
- 7) Garlach RT, Jansen NJG, Bijlsma MWA, et al. Allopurinol for Neonatal Hypoxic-Ischemic Encephalopathy: The ALBINO Trial. N Engl J Med. 2023;389(26):2441-2451. 【ALBINO試験:アロプリノールは重篤な神経発達障害または死亡を有意に減少させない(Neutral)】
- 8) Nolan JP, Sandroni C, Böttiger BW, et al. European Resuscitation Council and European Society of Intensive Care Medicine Guidelines 2021: Post-resuscitation care. Resuscitation. 2021;161:220-269. 【ERC/ESICM 2021:成人心停止後管理の最新ガイドライン。マルチモーダル予後予測・37.5°C以下発熱回避を推奨】
- 9) Thompson CM, Puterman AS, Linley LL, et al. The value of a scoring system for hypoxic ischaemic encephalopathy in predicting neurodevelopmental outcome. Acta Paediatr. 1997;86(7):757-761. 【Thompson Score:新生児HIE重症度スコアの原著】
- 10) Hypothermia after Cardiac Arrest Study Group. Mild therapeutic hypothermia to improve the neurologic outcome after cardiac arrest. N Engl J Med. 2002;346(8):549-556.
- 11) Volpe JJ. Neurology of the Newborn. 5th ed. Philadelphia: Saunders; 2008. 【新生児神経学の標準教科書】
- 12) Teasell RW, et al. Evidence-Based Review of Stroke Rehabilitation (EBRSR). 19th ed. 2020. www.ebrsr.com
- 13) StatPearls. Hypoxic-Ischemic Encephalopathy. Updated 2025. NCBI Bookshelf. NBK532959
STROKE LABの低酸素脳症後リハビリ支援
HIE後リハビリの5ステップアプローチ
Step 1 精密評価:NIHSS・FIM・MoCA・BBS・SLTA・VF/VEなど多角的評価で機能障害プロファイルを特定。MRI所見と照合して「どこがどれだけ障害されたか」を解剖学的に解釈
Step 2 目標設定:転帰予測データと患者・家族の希望を統合した現実的かつ挑戦的な目標を設定。mRS・FIM改善目標を医師・看護師・療法士・家族で共有
Step 3 多職種介入:PT(運動・歩行)・OT(ADL・認知)・ST(言語・嚥下)が独立かつ連携して同時進行で介入。週次カンファレンスで情報共有
Step 4 家族参加型リハビリ:介入に家族が参加し、日常生活でのリハビリ効果の維持・汎化を図る。退院前に住環境評価と住宅改修の提言を実施
Step 5 退院後継続支援:外来・訪問リハビリの継続、福祉サービスへの橋渡し、定期的な再評価と目標の更新
リハビリを受けた方の声
心停止から蘇生されましたが意識が戻るまで3日かかり、「脳に障害が残る」と言われた時は絶望しました。STROKE LABで「どの機能がどう回復できるか」を具体的に説明していただき、PT・OT・STが連携して対応してくれたおかげで、自分で歩けるところまで回復できました。
60代男性・院外心停止後HIE・発症後8ヶ月
新生児の子どもが低酸素脳症と診断された時、正直何もわからず途方に暮れました。STROKE LABで発達フォローアップを続けていただき、「今できることとこれからの見通し」を一緒に考えてもらえることで家族の不安がずいぶん和らぎました。
30代母親・新生児HIEのお子さんのご家族
低酸素脳症の後遺症に、
あきらめない専門リハビリを。
PT・OT・STが連携し、脳神経疾患に特化した評価と介入で機能回復を支援します。
急性期からの一貫したリハビリ計画をSTROKE LABでご相談ください。

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)














