【2026年版】直接路と間接路とは?:大脳基底核の役割と機能〜パーキンソン病まで解説!
脳卒中・パーキンソン病・ハンチントン病などの神経疾患のリハビリを行う上で、大脳基底核の直接路(Direct Pathway)・間接路(Indirect Pathway)・ハイパー直接路(Hyperdirect Pathway)の理解は欠かせません。「なぜパーキンソン病では動き出せないのか?」「ハンチントン病でなぜ不随意運動が起きるのか?」「DBSはなぜ効くのか?」――これらの臨床的疑問はすべて3つの経路の理解から始まります。開発背景・解剖・神経伝達物質・ドーパミンの役割・不随意運動との関係・リハビリ応用まで、世界標準の論文エビデンスとともに徹底解説します。
大脳基底核の直接路・間接路・ハイパー直接路を動画で確認できます。
大脳基底核の直接路・間接路・ハイパー直接路は、随意運動の開始・抑制・緊急停止を制御する3本の神経回路です。直接路(Go回路)は運動を促進し、間接路(NoGo回路)は不要な動きを抑制し、ハイパー直接路(超高速ブレーキ)は皮質から視床下核(STN)への直接経路で即時の運動停止を実現します。この3経路のバランスが崩れることでパーキンソン病・ハンチントン病・ジストニアなどの運動障害が生じます。リハビリテーション専門家は3経路の特性を理解することで、より根拠に基づいた介入計画を立てることができます。
- 直接路(Direct Pathway):皮質 → 線条体(D1受容体)→ GPi/SNr → 視床 → 皮質。GPi/SNrの抑制が弱まり視床が脱抑制 → 運動促進(Go)
- 間接路(Indirect Pathway):皮質 → 線条体(D2受容体)→ GPe → STN → GPi/SNr → 視床 → 皮質。GPi/SNrが強く活動し視床を抑制 → 運動抑制(NoGo)
- ハイパー直接路(Hyperdirect Pathway):皮質 → STN → GPi/SNr → 視床。線条体を経由せず最短経路で瞬時に全運動出力を停止(超高速ブレーキ)
- ドーパミンの二面性:D1受容体(直接路)= 興奮性 → 運動促進。D2受容体(間接路)= 抑制性 → 間接路を弱め運動しやすくなる。両方向で「運動の促進」に働く
- パーキンソン病:黒質緻密部(SNc)のドーパミン産生ニューロン喪失 → 直接路↓ & 間接路↑ → GPi/SNrの過活動 → 視床抑制↑ → 運動困難(無動・固縮)
- ハンチントン病:D2受容体ニューロン(間接路)の変性 → 間接路↓ → GPi/SNrの抑制低下 → 視床が過活動 → 過剰な不随意運動(舞踏病)
- DBS(深部脳刺激)の原理:STNへの高周波刺激でSTNの過活動を抑制 → GPi/SNrの過活動が抑えられる → 視床の運動出力が回復 → パーキンソン病症状改善
- リハビリへの応用:直接路 = リズム運動・聴覚キューで活性化。間接路 = 重心移動・停止-再開練習で調整。ハイパー直接路 = 突発的刺激への反応訓練で活性化
- 直接路MSNマーカー:D1受容体 + サブスタンスP・ダイノルフィンを共発現。間接路MSNはD2受容体 + エンケファリンを共発現。HDではエンケファリン陽性ニューロン(間接路)が先に変性するため初期症状が舞踏病(間接路機能喪失)となる(Reiner et al. 1988)
- 4機能ループ(Alexander et al. 1986):①運動ループ(被殻-VA/VL視床)②眼球運動ループ(尾状核体部-MD視床)③前頭前野ループ(尾状核頭部-MD視床)④辺縁系ループ(側坐核-腹側淡蒼球)。PDで運動+認知+感情が同時に障害される理由
- 3経路の伝達速度(Nambu et al. 2002):ハイパー直接路≒2〜3ms → 直接路≒5〜6ms → 間接路≒10〜15ms。「全停止→選択的Go→競合抑制」の3段階・時間的モデルが随意運動選択の基本原理
- 報酬予測誤差(Schultz et al. 1997):ドーパミンはRPEシグナルとして機能。成功→DA増加→D1促進→直接路強化(正の強化学習)。適切な難易度設定とフィードバック設計がドーパミン系の運動学習を促進するリハビリ根拠
大脳基底核とは ― 解剖学的基礎と各構造の役割
大脳基底核(Basal Ganglia)は大脳半球の深部に位置する複数の核の集合体で、随意運動の調節・認知機能・報酬処理・習慣形成に関与する重要な神経回路網です。大脳皮質からの入力を受け、視床を経由して皮質への出力を調節するという「皮質-基底核-視床-皮質ループ」を形成しています。
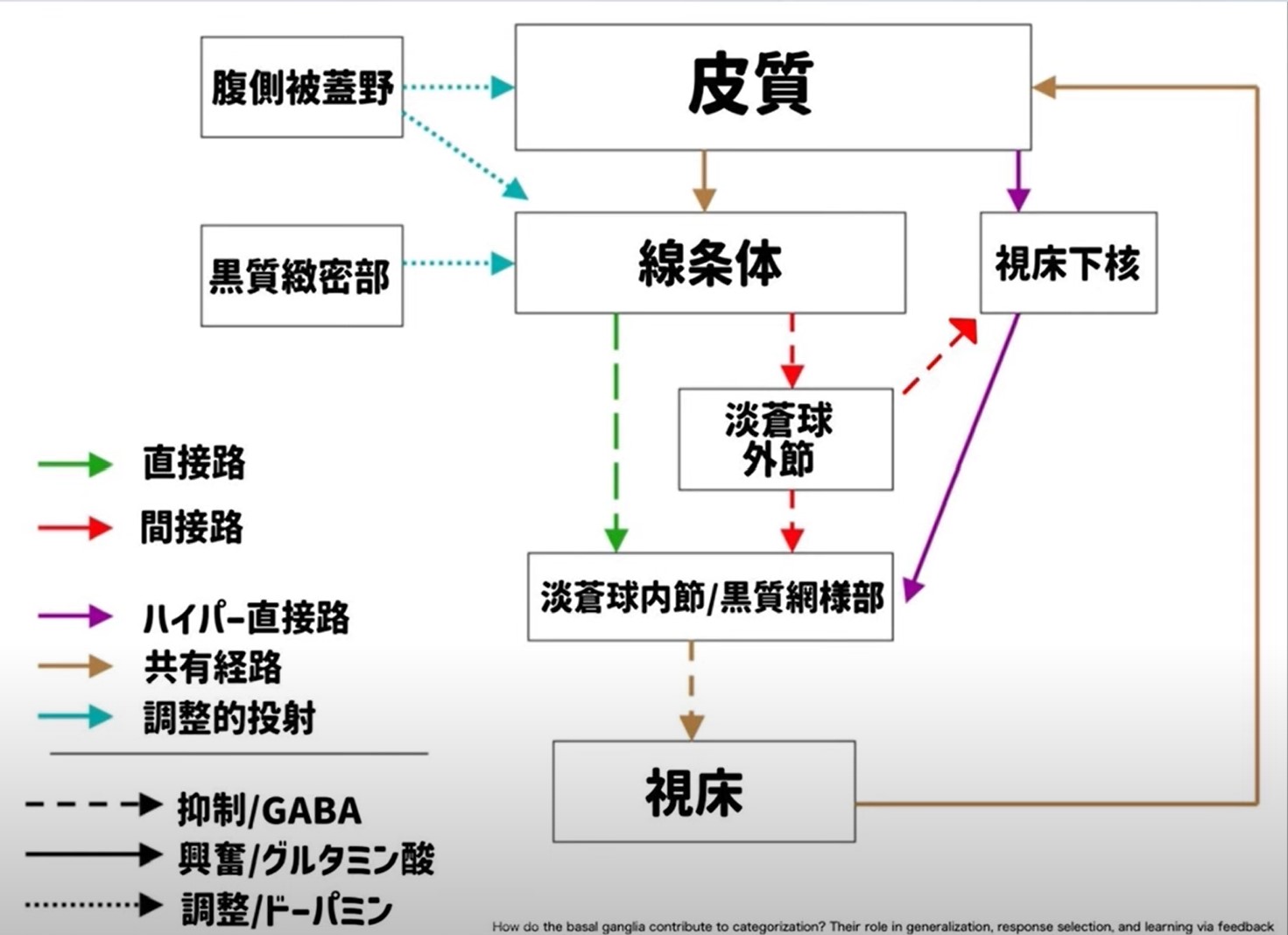
▲ 大脳基底核の経路概略図(Sager et al. 2008 を参考)
🔬 大脳基底核の主要構造と機能の一覧
線条体(Striatum:尾状核・被殻・側坐核):大脳基底核の主要な入力部位。皮質・視床・黒質から広く入力を受ける。運動調節・報酬処理・習慣学習に関与。尾状核は認知・実行機能、被殻は運動制御、側坐核は報酬・動機付けと関連が深い。
淡蒼球外節(GPe:Globus Pallidus externus):間接路の中継核。線条体から抑制性入力(GABA)を受け、STNを抑制する。GPeの機能障害は間接路の乱れをもたらす。
淡蒼球内節(GPi:Globus Pallidus internus):大脳基底核の主要な出力核のひとつ。視床に抑制性(GABA)投射を送り、直接路・間接路の統合出力として随意運動の制御に不可欠。
黒質網様部(SNr:Substantia Nigra pars reticulata):GPiと同様の機能を持つ大脳基底核の出力核。特に眼球運動・頭部運動の制御に関与。
黒質緻密部(SNc:Substantia Nigra pars compacta):ドーパミン産生ニューロンの中心部位。線条体へのドーパミン投射(ニグロストリアタール経路)を通じて直接路・間接路の活動を調節。パーキンソン病ではここのニューロンが変性脱落する。
視床下核(STN:Subthalamic Nucleus):間接路・ハイパー直接路の重要な中継核。GPiとSNrへ興奮性(グルタミン酸)投射を送り、視床抑制に寄与。DBS(深部脳刺激)の主要なターゲット。
腹側被蓋野(VTA:Ventral Tegmental Area):SNcと並ぶドーパミン産生部位。側坐核・前頭前野への投射(中脳辺縁系・中脳皮質経路)を通じて報酬・動機付け・依存症に関与。
🧪 直接路・間接路MSNを区別する神経ペプチドマーカー
線条体の中型有棘ニューロン(MSN)は外見上同じに見えますが、直接路と間接路のニューロンは共存する神経ペプチドで区別できます。この知識は神経変性疾患の病態理解に不可欠です。
直接路MSN:D1受容体 + サブスタンスP(Substance P)・ダイノルフィン(Dynorphin)を共発現。サブスタンスPはGPi/SNrへの抑制を強化するペプチドとして機能。免疫組織化学でサブスタンスP陽性ニューロンを染色することで直接路ニューロンを同定できる。
間接路MSN:D2受容体 + エンケファリン(Enkephalin)を共発現。エンケファリンはGPeへの抑制に関与するオピオイドペプチド。ハンチントン病ではエンケファリン陽性ニューロン(間接路)が直接路ニューロンより先に変性することが病理学的に確認されている(Reiner et al. 1988)。これがHDの初期に舞踏病(間接路機能喪失)が現れる理由の一つ。
🔄 大脳基底核の4つの機能ループ ― 運動だけではない
大脳基底核は「運動制御だけの器官」ではありません。皮質-基底核-視床-皮質ループは機能的に4〜5つの並列ループとして機能し、それぞれ異なる脳領域に関与します(Alexander et al. 1986)。
① 運動ループ(Motor Loop):一次運動野・補足運動野・運動前野 ← 被殻(後側)← VA/VL視床。随意運動の開始・制御が主機能。パーキンソン病で最も影響を受ける。
② 眼球運動ループ(Oculomotor Loop):前頭眼野(FEF)← 尾状核(体部)← 背内側視床(MD核)。眼球運動の計画・抑制を担当。SNrが上丘(SC)への出力を制御し、サッケードに関与。
③ 前頭前野ループ(Prefrontal/Cognitive Loop):背外側前頭前野(DLPFC)← 尾状核(頭部)← MD視床。実行機能・ワーキングメモリ・認知的柔軟性を担当。パーキンソン病の認知障害はこのループの障害と関連。
④ 辺縁系ループ(Limbic Loop):眼窩前頭皮質・前帯状皮質(ACC)← 側坐核・腹側線条体 ← 腹側淡蒼球 ← MD視床。動機付け・感情・報酬処理を担当。依存症・強迫性障害・ADHD・うつ病との関連が深い。
※脳卒中・パーキンソン病などの大脳基底核疾患では「運動障害のみ」ではなく認知・感情・動機付けの問題も合併しやすい理由がこのマルチループ構造から理解できます。
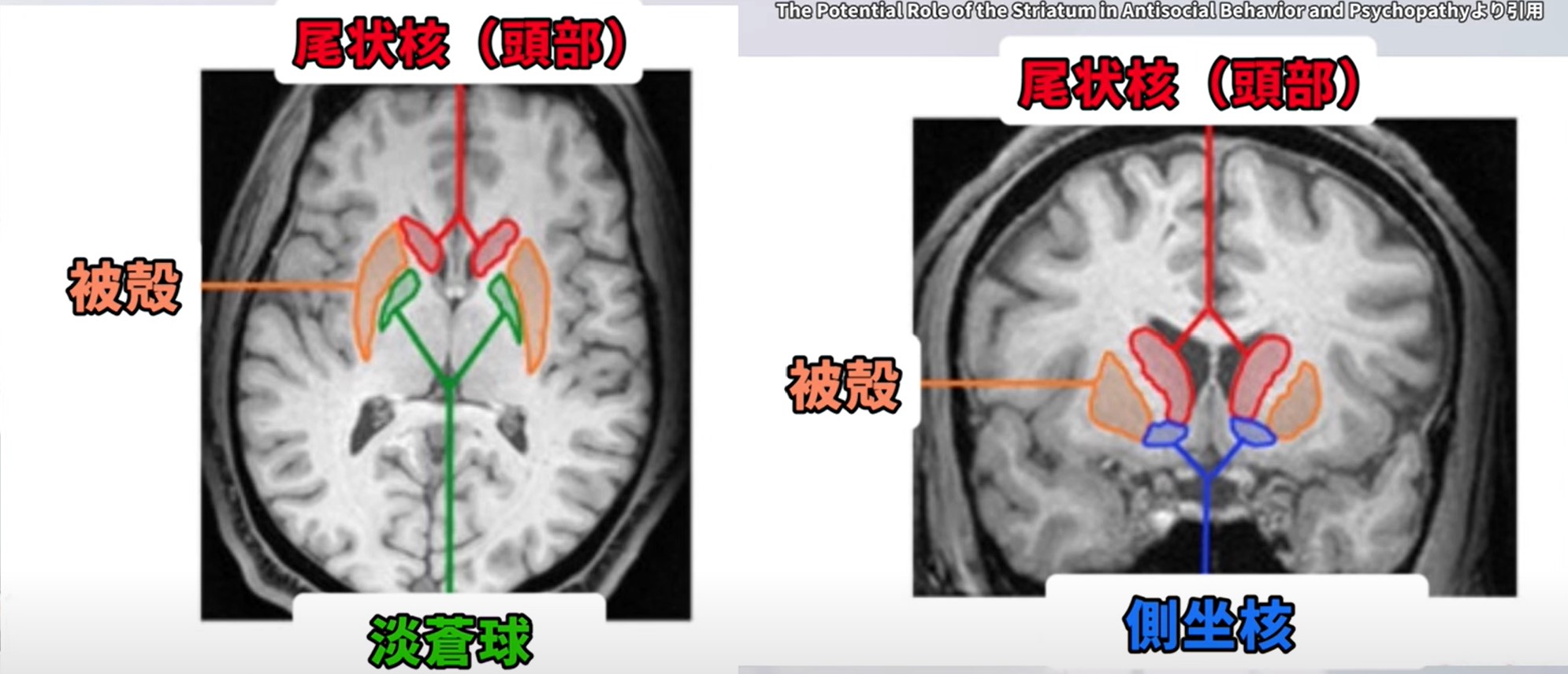
▲ 線条体(尾状核・被殻・側坐核)の解剖
3つの経路の全体像と比較 ― Go / NoGo / 超高速ブレーキ
運動促進
運動抑制
直接路 超高速ブレーキ
即時停止
| 比較項目 | 直接路(Go) | 間接路(NoGo) | ハイパー直接路 |
|---|---|---|---|
| 主な役割 | 運動の開始・促進 | 不要な運動の抑制・選択 | 全運動の即時停止・緊急制御 |
| 神経回路(要約) | 皮質→線条体(D1)→GPi/SNr→視床 | 皮質→線条体(D2)→GPe→STN→GPi/SNr→視床 | 皮質→STN(直接)→GPi/SNr→視床 |
| 中継核数 | 少ない(高速) | 多い(調整型) | 最少(超高速) |
| ドーパミン受容体 | D1受容体 → 促進 | D2受容体 → 抑制(弱める) | 直接受容体関与なし |
| 列車の比喩 | 🚄 特急列車(青信号) | 🚃 ローカル線(黄信号) | 🚨 非常ブレーキ(赤信号) |
| 障害時の症状 | 無動・固縮(PD) | 舞踏病(HD)・過運動 | 衝動制御障害・すくみ |
| 代表疾患 | パーキンソン病 | ハンチントン病 | STN病変・衝動制御障害 |
💡 3経路の統合的理解 ― なぜバランスが重要か
直接路(Go)と間接路(NoGo)は常に拮抗的に働き、「どの動きを選択してどの動きを抑制するか」を決定します。直接路が特定の運動プログラムを選択的に促進する一方、間接路はそれ以外の競合する運動プログラムを抑制することで、動作の精度と選択性が生まれます。これを「フォーカス型抑制(Focused Inhibition)」と呼びます。
ハイパー直接路はこの2経路よりも速く働き(線条体という中継を経由しないため)、一時的に全運動出力をブレーキし、状況変化に応じた行動の切り替えを可能にします。この3経路のバランスが崩れることが、さまざまな運動障害の本質的なメカニズムです。
直接路(Direct Pathway)― Go回路の詳細解説
直接路(Direct Pathway)― 運動を「促進」する特急列車
| 経路ステップ | 詳細と神経伝達物質 |
|---|---|
| ①皮質 | 前頭葉運動関連領域(一次運動野・補足運動野)からグルタミン酸(興奮性)を線条体へ送る |
| ②線条体(D1) | D1受容体を持つ中型有棘ニューロン(MSN)が活性化。GABAによる抑制性信号をGPi/SNrへ送る(GPi/SNrを抑制する) |
| ③GPi/SNr | 線条体からのGABAを受けGPi/SNrの活動が低下(抑制)される。通常GPi/SNrは高頻度発火(60〜80Hz)で視床を強く抑制しているが、この持続的な抑制出力が弱まる |
| ④視床(脱抑制) | GPi/SNrからのGABA抑制が減弱し、視床(VA/VL核)が脱抑制=活性化される。グルタミン酸(興奮性)を皮質へ投射。「脱抑制」とは「抑制の除去による活性化」であり直接興奮ではない点に注意 |
| ⑤再び皮質 | 皮質運動野への興奮性入力が増加 → 随意運動が促進・開始される |

直接路の理解で最も重要な概念は「二重抑制(Disinhibition)」です。線条体がGPi/SNrを抑制し(1つ目の抑制)、その結果GPi/SNrが視床を抑制できなくなる(抑制の抑制=脱抑制)ことで、視床が活性化されます。「抑制の抑制=促進」という逆転のロジックが直接路の本質です。
間接路(Indirect Pathway)― NoGo回路の詳細解説
間接路(Indirect Pathway)― 運動を「抑制・選択」するローカル線
| 経路ステップ | 詳細と神経伝達物質 |
|---|---|
| ①皮質 | グルタミン酸(興奮性)を線条体のD2受容体を持つMSNへ送る |
| ②線条体(D2) | D2受容体を持つMSNが活性化。GABA抑制をGPeへ送る(GPeを抑制する) |
| ③GPe | 線条体からGABA抑制を受け、GPeの活動が低下。GPeからSTNへの抑制(GABA)が弱まる |
| ④STN(脱抑制) | GPeからの抑制が取れてSTNが活性化。グルタミン酸(興奮性)をGPi/SNrへ送る |
| ⑤GPi/SNr | STNから興奮性入力を受けGPi/SNrが強く活性化。GABA抑制を視床へ強力に送る |
| ⑥視床 | 視床が強く抑制される → 皮質への興奮性出力が減少 |
| ⑦結果 | 皮質運動野への入力が減少 → 不要な競合運動プログラムが抑制される(NoGo) |

🎯 間接路の重要概念:「フォーカス型抑制」
直接路が特定の運動プログラムを選択的に「通す」のに対し、間接路は競合する他の運動プログラムを選択的に「通さない」役割を担います。この2つが連動することで、「コーヒーを取りながら他の物を倒さない」「走り始めたときに不必要な腕の揺れを抑える」といった精密な動作の選択が実現されます。これを「フォーカス型抑制(Focused Inhibition)」と呼びます。
また間接路は「動きの質(velocity・fluency)の調整」に関与し、固縮・動作緩慢(bradykinesia)の出現メカニズムにも深く関係しています。
ハイパー直接路(Hyperdirect Pathway)― 超高速ブレーキの詳細
ハイパー直接路(Hyperdirect Pathway)― 一瞬で運動を止める非常ブレーキ
| 経路ステップ | 詳細と神経伝達物質 |
|---|---|
| ①皮質(直接) | 前頭前野・運動関連領域からSTNへ直接グルタミン酸(興奮性)を送る。線条体を経由しないため伝達速度が速い |
| ②STN(即時活性化) | 皮質からの直接興奮性入力でSTNが即時に強く活性化される |
| ③GPi/SNr | STNからグルタミン酸(興奮性)を受けGPi/SNrが爆発的に活性化。強力なGABA抑制を視床へ送る |
| ④視床(急抑制) | 視床が強力かつ急速に抑制される → 皮質への出力が瞬間的にゼロになる |
| ⑤結果 | 進行中の運動プログラムが即時停止される。状況に応じた行動の切り替え・衝動の抑制が可能 |

🔬 ハイパー直接路の臨床的重要性
① 衝動抑制(Impulse Control):「やろうとしたけど止めた」という経験はハイパー直接路によるものです。前頭前野(特に右下前頭回・前補足運動野)からSTNへの信号が衝動的な行動反応を抑えます。ADHDや強迫性障害ではこの機能の障害が指摘されています。またStop Signal課題(GO信号後にSTOP信号が提示される課題)ではハイパー直接路の活性化がfMRIで確認されており、反応抑制の神経基盤として確立されています(Aron & Poldrack 2006)。
② 3経路の伝達速度の違い(Nambu et al. 2002):サルの運動皮質刺激後のGPi記録では、ハイパー直接路:約2〜3ms → 直接路:約5〜6ms → 間接路:約10〜15msという時間的順序が確認されています。この「全停止(ハイパー直接路)→ 選択的GO(直接路)→ 競合抑制(間接路)」という時間的3段階モデルが随意運動選択の基本原理です。
③ すくみ足(Freezing of Gait:FOG)との関係:パーキンソン病のすくみ足は「狭い空間・方向転換・二重課題・感情的ストレス」などのトリガーで前頭葉がSTNへ過剰な「全停止」信号を送ることで歩行が突然停止すると考えられています。リズム聴覚刺激(RAS)・視覚床キュー(床テープ・光投影)・レーザー杖はこの過剰なハイパー直接路活動を外部キューで「上書き」することで歩行の再開を促します(RCTで有効性確認:Nieuwboer et al. 2007)。
④ DBS(深部脳刺激療法)との関係:STNへの高周波刺激(100〜180Hz)がSTNの異常過活動を機能的に「脱同期化・抑制」することで、GPi/SNrの過活動が抑えられ視床→皮質の正常な運動出力が回復します。なお振戦にはVim核(視床の腹中間核)DBSも有効で、本態性振戦では第一選択です。ジスキネジアが顕著な患者にはGPi-DBSが優先されることがあります。
ドーパミンの役割 ― D1受容体とD2受容体の二面性
D1受容体(直接路)とD2受容体(間接路)では正反対の作用がある
ドーパミンは直接路・間接路の両方に影響を及ぼしますが、その作用は受容体の種類によって正反対です。これが「ドーパミンは運動を促進する」という単純な理解では不十分な理由です。
| 受容体 | 所在する回路 | 共役Gタンパク | ドーパミン作用 | 最終的な運動への効果 |
|---|---|---|---|---|
| D1受容体 | 直接路MSN | Gs(cAMP↑) | MSN興奮↑ → 直接路促進 | GPi/SNr抑制↑ → 視床脱抑制 → 運動促進 |
| D2受容体 | 間接路MSN | Gi(cAMP↓) | MSN抑制↓ → 間接路抑制 | 間接路弱体化 → GPi/SNr活動↓ → 視床脱抑制 → 運動促進 |
| ⇒ 両方の受容体を介してドーパミンは「運動促進」に働く(機序は正反対) | ||||
⚡ 報酬予測誤差(Reward Prediction Error)とドーパミン ― 学習との深い関係
ドーパミンは単なる「運動促進ホルモン」ではなく、「報酬予測誤差(RPE:Reward Prediction Error)」を符号化する学習シグナルでもあります(Schultz et al. 1997)。
期待より良い結果:ドーパミンが一過性に増加(「フェーズ発火」)→ D1活性化 → 直接路が強化 → その行動を繰り返す学習が促進される(正の強化)。
期待通りの結果:ドーパミン発火に変化なし → 行動の変化なし。
期待より悪い結果:ドーパミンが一過性に減少(「発火抑制」)→ D1活性低下・D2相対的活性化 → 間接路が強化 → その行動を避ける学習が促進(負の強化)。
この「ドーパミンによるRPE信号」はリハビリテーションにも直接関係します。成功体験の積み重ね(適切な難易度設定・フィードバック)がドーパミン系を通じた運動学習の強化につながります。課題が簡単すぎても難しすぎてもRPEが生まれず、学習効果が低下します。
🔄 コリン作動性介在ニューロン(ChAT)― ドーパミンと拮抗するアセチルコリン
線条体にはコリン作動性介在ニューロン(Tonically Active Neurons:TAN)が存在し、持続的にアセチルコリン(ACh)を放出しています。このAChはドーパミンと拮抗的に働き、直接路を抑制・間接路を促進することで「運動に対するブレーキ」として機能します。
臨床的意義:パーキンソン病の治療に抗コリン薬(トリヘキシフェニジルなど)が使用されるのはこの拮抗関係を利用したものです。ドーパミンが不足した状態では相対的にAChが過剰となるため、AChを抑制することで運動症状(特に振戦・固縮)を緩和します。ただし認知機能への副作用(記憶力低下)があるため高齢者には慎重適用が必要です。
⚠️ パーキンソン病でのL-DOPA療法とジスキネジア
L-DOPA(レボドパ)によるドーパミン補充は直接路・間接路の両方を正常化し、無動・固縮を改善します。しかし長期使用や高用量では「ジスキネジア(薬物誘発性不随意運動)」が生じます。これはパルス状(間欠的)なドーパミン供給によってD1受容体の感受性が過剰に高まり(感受性亢進・Up-regulation)、直接路が「過活動」となった状態です。
持続的なドーパミン供給(経皮吸収型貼付剤・持続皮下注射・DBS)がジスキネジアを軽減する根拠も、この受容体感受性調節の観点から理解できます。さらにアマンタジン(NMDA受容体拮抗薬)はジスキネジア治療の第一選択薬として、直接路過活動を末梢側(グルタミン酸受容体)で抑制することで効果を発揮します。
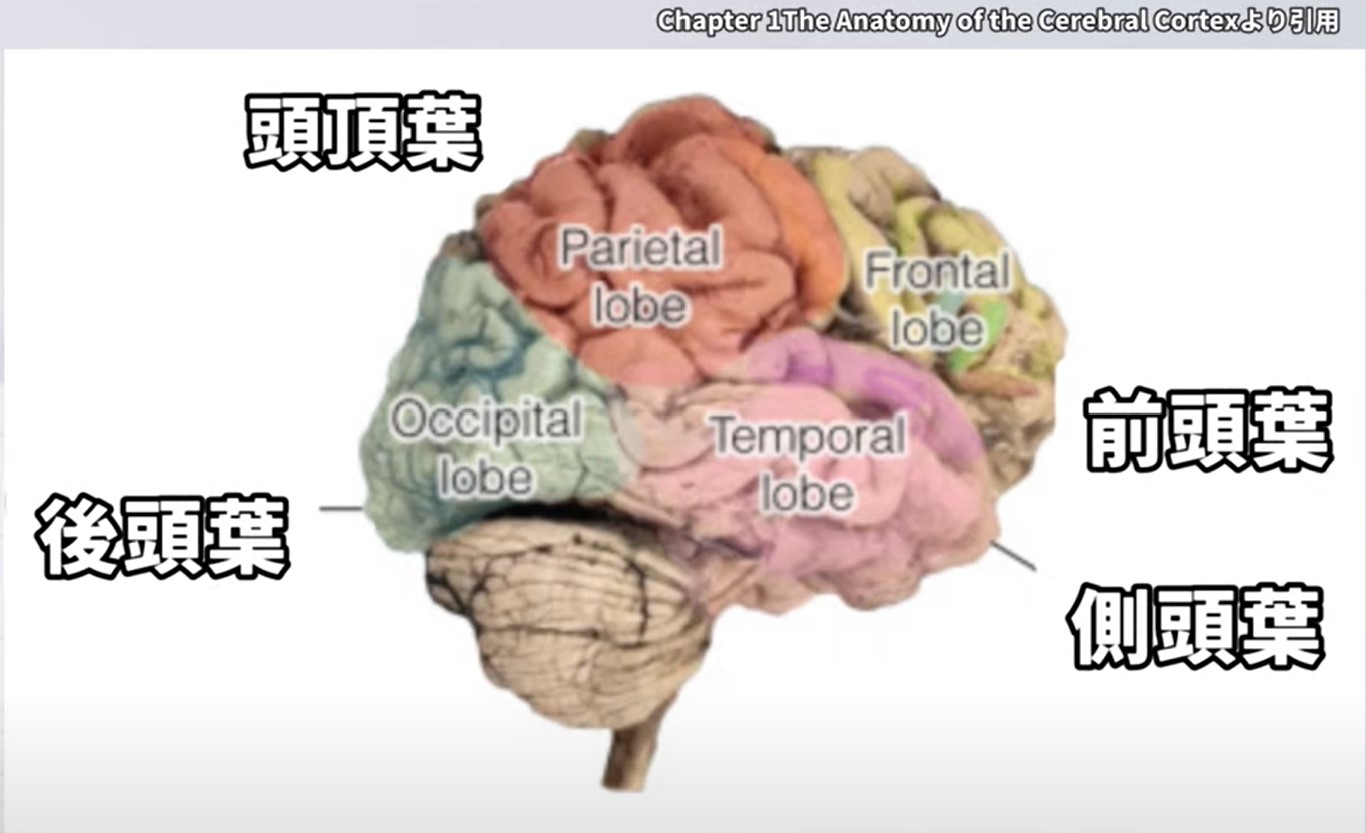
▲ 大脳皮質の各領域と大脳基底核への入力
不随意運動と大脳基底核の病態 ― 8つの症状を解説
🔬 不随意運動の理解には「どの経路のどの核が障害されたか」が鍵
大脳基底核の不随意運動は「直接路過活動(過運動型:舞踏病・ヘミバリズム)」か「間接路過活動(低運動型:固縮・無動)」か「ドーパミン調節の乱れ(混合型:ジスキネジア・振戦)」のいずれかに大別されます。以下の8症状を経路の観点から理解してください。
症状:不規則・短時間・予測不可能な流れるような不随意運動。身体の一部から別の部位に連鎖するように移動する。
病態経路:D2-MSN変性 → GPe脱抑制 → STN抑制↑ → GPi/SNr↓ → 視床脱抑制(過活動)→ 皮質過剰出力
代表疾患:ハンチントン病・シデナム舞踏病
経路分類:間接路障害(過運動型)
症状:ねじれ・反復運動・持続的な不随意収縮・異常姿勢。拮抗筋の同時収縮が特徴。
病態経路:被殻・淡蒼球の興奮性/抑制性バランス異常 + 感覚運動統合の乱れ(視床関与)
代表疾患:原発性ジストニア・脳性麻痺
治療:ボツリヌス毒素・DBS(GPi標的)
症状:受動的関節運動の全可動域にわたる均一な筋抵抗。鉛管様(均一)または歯車様(断続的)。
病態経路:DA不足 → D1↓/D2↑ → 直接路↓・間接路↑ → GPi/SNr過活動 → 視床抑制↑ → 皮質出力↓
代表疾患:パーキンソン病・パーキンソン症候群
経路分類:直接路障害(低運動型)
症状:リズミカルな不随意振動。安静時振戦(4〜6Hz:PD特徴)・姿勢時振戦・動作時振戦(4〜12Hz:本態性振戦)に分類。
病態経路:基底核-視床-皮質ループの異常振動回路形成。小脳系(歯状核-Vim視床-皮質)との相互作用も関与。
代表疾患:パーキンソン病(安静時)・本態性振戦(動作時)
治療:L-DOPA(PD)・β遮断薬(ET)・Vim-DBS
症状:突然・反復的な運動(単純:まばたき・首振り、複雑:跳躍・物への接触)または発声(単純:咳払い、複雑:汚言症)。半随意的で前駆衝動を伴う。
病態経路:線条体(尾状核・被殻)の過活動 + 皮質-基底核ループの調節不全。ドーパミン過感作も関与。
代表疾患:トゥレット症候群・一過性チック症
治療:行動療法(CBIT)・ハロペリドール・クロニジン
症状:片側四肢の激しく投げ飛ばすような大振幅の不随意運動。通常は片側性で急性発症。数週〜数カ月で自然消退することが多い。
病態経路:STN損傷 → GPi/SNrへのグルタミン酸入力↓ → GPi/SNr活動低下 → 視床抑制低下(脱抑制)→ 皮質過活動
代表疾患:STNの梗塞・出血(最多原因)・非ケトン性高血糖
治療:ハロペリドール・クロナゼパム・基礎疾患の治療(多くは自然消退)
| 不随意運動 | 主に障害された構造・経路 | 経路バランス | 治療アプローチ |
|---|---|---|---|
| 過運動型(Hyperkinetic:運動が多すぎる) | |||
| 舞踏病 | 間接路線条体(D2 MSN) | 間接路↓ → 直接路優位 | テトラベナジン・ハロペリドール |
| ヘミバリズム | STN(視床下核)損傷 | GPi/SNr活動低下 | ハロペリドール・消退することも多い |
| ジストニア | 被殻・淡蒼球・視床 | 複合的バランス異常 | ボツリヌス毒素・DBS(GPi標的) |
| 低運動型(Hypokinetic:運動が少なすぎる) | |||
| 無動・固縮 | SNc(ドーパミン産生) | 直接路↓・間接路↑ | L-DOPA・DBS(STN標的) |
| 混合型(Mixed) | |||
| 安静時振戦 | 基底核-視床-皮質ループ異常振動 | 回路全体の振動 | DBS・抗コリン薬 |
| ジスキネジア | 直接路の過感作(D1 Up-regulation) | 直接路過活動 | L-DOPA調整・アマンタジン |
リハビリテーションへの応用 ― 3経路を意識した介入設計
🏃 直接路・間接路・ハイパー直接路をリハビリで活用する3原則
① 直接路(Go)の活性化:外部キュー(聴覚リズム・視覚目標)を使って運動開始の閾値を下げる。補足運動野への内部キューが障害されていても、外部キューは一次運動野を直接活性化できるため有効(Morris et al. 1994)。メトロノーム・床のテープ・リズム音楽がこれに当たります。LSVT-BIG(Lee Silverman Voice Treatment)もこの原理に基づき、大振幅運動を繰り返すことで直接路の運動増幅機構を再較正します。
② 間接路(NoGo)の調整:動作の「停止-再開」や重心移動練習で間接路のフォーカス型抑制機能を強化。「意図した動作のみを精密に実行する」精度訓練に相当します。ミラーセラピー・課題特異的訓練も間接路を含む動作選択回路の再学習を促進します。
③ ハイパー直接路の強化:不規則タイミングの刺激への反応訓練でSTNと前頭前野の接続を強化。すくみ足・転倒予防に直結します。デュアルタスク歩行訓練もこの経路の活性化に寄与しますが、PDでは二重課題が逆効果になる場合もあるため難易度調整が重要です。
📊 エビデンスに基づくリハビリ介入と神経基盤の対応表
| 介入法 | 主な対象経路 | 主なエビデンス | 適応症状 |
|---|---|---|---|
| RAS(リズム聴覚刺激) | 直接路の補完(小脳経由) | Thaut et al. 1996(RCT) | 歩行速度↓・すくみ足 |
| 視覚床キュー(テープ/光) | ハイパー直接路の外部上書き | Nieuwboer et al. 2007(RCT) | すくみ足・方向転換困難 |
| LSVT-BIG | 直接路の運動振幅再較正 | Ebersbach et al. 2010(RCT) | 小刻み歩行・動作緩慢 |
| タンゴダンス | 直接路・間接路・前庭系の統合 | Hackney et al. 2007(RCT) | バランス・歩行・QOL |
| 水中運動(アクアセラピー) | 固縮緩和・間接路の再調整 | Vivas et al. 2011 | 固縮・関節可動域制限 |
| デュアルタスク歩行訓練 | ハイパー直接路・認知ループ | 複数観察研究 | 認知的注意の歩行への応用 |
| 報酬フィードバック訓練 | ドーパミン-RPEによる直接路強化 | 基礎研究エビデンス多数 | 運動学習・習慣形成 |
📋 大脳基底核機能評価に用いられる主な臨床評価ツール
パーキンソン病:
・MDS-UPDRS(Movement Disorder Society-UPDRS):4部構成の標準評価。Part III(運動評価)では固縮・振戦・指タッピング・歩行・姿勢反応を定量化。直接路/間接路バランスの臨床的反映として活用。
・DaTスキャン(DAT-SPECT):ドーパミントランスポーターの密度を核医学的に可視化。線条体のドーパミン欠乏を定量化しPDとETを鑑別。
・TUG(Timed Up and Go Test):立ち上がり〜歩行〜方向転換〜着席を時間計測。直接路の起動性・ハイパー直接路の方向転換能力を間接評価。
・FOG-Q(Freezing of Gait Questionnaire):すくみ足の頻度・重症度を患者報告で評価。ハイパー直接路機能の臨床指標として有用。
ハンチントン病:
・UHDRS(Unified Huntington’s Disease Rating Scale):舞踏病スコアを含む運動・認知・行動・ADLの総合評価。直接路/間接路のアンバランスを数値化。
一般的な大脳基底核機能評価:
・Mini-BESTest:バランス評価(予測的・反応的・感覚性・歩行の4領域)。ハイパー直接路の反応的姿勢制御を含む。
・Stop Signal Task:衝動抑制・反応停止時間(SSRT)の神経心理的評価。ハイパー直接路機能の実験的指標。
ケーススタディ:田中先生と石川さんの4回セッション
パーキンソン病(大脳基底核機能不全)による動作開始困難・固縮・軽度振戦がみられる石川さん(60代・男性)と療法士田中先生の実践的リハビリストーリーです。
初回セッション ― 評価と問題点の整理
主な症状:動作開始の2〜3秒の遅れ・歩行開始時の固縮・コップを持つ際の右手振戦
直接路を狙う ― リズム聴覚刺激(RAS)訓練
🚄 目的:直接路の活性化
メトロノーム(80〜100BPM)に合わせた立ち上がり → 踏み出し → 着席の反復練習。外部リズムキューが線条体を通じず直接運動皮質を促通するため、PD患者の動作開始遅延を改善します。
- 立ち上がり→踏み出し×15回反復
- 足踏みペダル漕ぎ(リズム固定)
- リズム音楽に合わせた腕振り歩行
結果(3回後):
間接路を狙う ― 重心移動・停止-再開練習
🚃 目的:間接路(フォーカス型抑制)の再調整
左右への体重移動 + 不規則タイミングでの「止まれ」の合図による停止・再開練習。不要な筋活動を抑制する間接路の機能を再学習します。
- 左右重心移動 × 20回(速度変化あり)
- 「止まれ」コマンドへの即時停止訓練
- ターゲットへの精密な上肢リーチング
結果:
ハイパー直接路を狙う ― 突発的反応訓練とすくみ足対策
🚨 目的:ハイパー直接路(前頭前野→STN接続)の強化
不規則なタイミングで肩を軽く押す・突然の「止まれ/動け」指示・デュアルタスク歩行などでSTNと前頭前野の反応性接続を強化します。転倒予防・すくみ足対策の核心です。
- 床テープをまたぐ歩行(視覚キュー)
- 突発的な方向転換指示への対応
- デュアルタスク歩行(計算しながら歩く)
1カ月後の総合評価:
よくある質問(FAQ)
直接路と間接路は同時に働くのですか?
時間的には、ハイパー直接路(2〜3ms)がまず全体に「ブレーキ」をかけ、続いて直接路(5〜6ms)が選択した動作の「アクセル」を踏み、最後に間接路(10〜15ms)が競合する動作の「精密ブレーキ」をかけるという3段階で随意運動が実現されます(Nambu et al. 2002)。
なぜパーキンソン病ではリズムキューが効くのですか?
この神経科学的根拠から、RASは複数のRCTでパーキンソン病患者の歩行速度・ストライド長の改善が確認されています(Thaut et al. 1996)。RASの効果的な使用には患者の安静時歩行ケイデンスより10〜15%速いテンポ設定が推奨されており、漸増的に速度向上を図ります。視覚キュー(床のテープ・レーザー杖)も同様の神経経路で機能し、特にすくみ足に有効です。
DBSはなぜSTNを標的にするのですか?GPiとの違いは?
STN-DBSが主流の理由:①STNはGPiより小さく(4〜6mm vs 10〜20mm)電極配置の精度が高い ②刺激電流量が少なく電池寿命が長い ③L-DOPAの用量を30〜50%減量できることが多く、ジスキネジアの軽減にもつながる(Deuschl et al. 2006)。
GPi-DBSが選ばれる場合:①ジスキネジアが顕著でL-DOPA減量が難しい患者 ②認知機能への影響をより慎重に管理する必要がある患者(STN-DBSの方が認知への影響が大きい可能性がある)。
振戦に対してはVim核(視床の腹中間核)-DBSも有効で、本態性振戦では第一選択です。ジストニアにはGPi-DBSが第一選択です。
大脳基底核は「運動」以外にも関係していますか?
認知ループ(背外側前頭前野-尾状核頭部-MD視床):ワーキングメモリ・実行機能・認知的柔軟性を担当。パーキンソン病の40〜80%に認知障害が合併し、進行するとパーキンソン病認知症(PDD)となります。
辺縁系ループ(眼窩前頭皮質-側坐核-腹側淡蒼球):動機付け・感情調節・報酬処理を担当。パーキンソン病の50〜70%に抑うつ・不安症状が合併し、これが直接路の機能低下と並行して生活の質を低下させます。
リハビリへの含意:パーキンソン病患者の「やる気が出ない」「集中できない」は辺縁系・前頭前野ループの障害であり、単なる「精神的な問題」ではありません。成功体験の設計(RPEによるドーパミン放出)が動機付けループの賦活にも貢献します。
ハンチントン病と脳卒中後の不随意運動の違いは?
一方、脳卒中後の不随意運動は梗塞・出血によって特定の核が急性に障害されることで生じます。STN梗塞→急性ヘミバリズム、被殻出血→固縮・運動障害、視床病変→感覚障害を伴う対側運動障害が典型です。発症様式(急性 vs 慢性進行)と症状プロファイルが鑑別の要点です。
大脳基底核の評価にはどのような方法がありますか?
機能的歩行評価ではTUG・10m歩行テスト・FOG-Q・Berg Balance Scale(BBS)・Mini-BESTestが頻用されます。特にMini-BESTestは予測的姿勢調節(直接路)と反応的姿勢調節(ハイパー直接路)を分離評価できる点で臨床的価値が高いです。
神経画像ではDaTスキャン(DAT-SPECT)がパーキンソン病の診断・鑑別に有用で、線条体のドーパミン欠乏パターン(後方被殻優位)を定量化できます。MRIの黒質超音波(Transcranial Sonography)も非侵襲的な補助診断として国際的に使用されています。
神経心理的評価ではStop Signal Task(衝動抑制・ハイパー直接路の機能指標)・MOCA(Montreal Cognitive Assessment:認知ループ評価)・BDI(Beck Depression Inventory:辺縁系ループ評価)が基底核の多面的評価に有用です。
リハビリを受けた方の声
パーキンソン病と診断されてから「なぜ動き始めが遅くなるのか」が全然わかりませんでした。STROKE LABでセラピストさんに「特急列車・ローカル線・非常ブレーキ」という3つの列車の話をしてもらい、自分の脳で何が起きているかがイメージできるようになりました。リズムの音楽に合わせると動きやすくなる理由も納得でき、リハビリへの取り組み方が変わりました。
60代男性・パーキンソン病・リハビリ開始3カ月
脳出血後にヘミバリズムの症状が出て、右手が激しく動いて日常生活が大変でした。「視床下核という核が傷ついたから」と説明してもらい、STNとGPiの関係を図で理解できたことで、なぜ一定期間で症状が軽減していくかも理解できました。治療の先が見えるだけで気持ちが楽になりました。
70代女性・脳出血後ヘミバリズム・退院後外来リハビリ
参考文献・引用文献
- 1) Sager C, et al. (2008). How do the basal ganglia contribute to categorization? Their role in generalization, response selection, and learning via feedback. Neuroscience & Biobehavioral Reviews. PubMed
- 2) Albin RL, Young AB, Penney JB. (1989). The functional anatomy of basal ganglia disorders. Trends in Neurosciences. 12(10):366-375. 【直接路・間接路モデルの原著】
- 3) DeLong MR. (1990). Primate models of movement disorders of basal ganglia origin. Trends in Neurosciences. 13(7):281-285. 【直接路・間接路モデルの確立】
- 4) Nambu A, Tokuno H, Takada M. (2002). Functional significance of the cortico-subthalamo-pallidal ‘hyperdirect’ pathway. Neuroscience Research. 43(2):111-117. 【ハイパー直接路の伝達速度(2-3ms→5-6ms→10-15ms)・時間的3段階モデルの原著】
- 5) Alexander GE, DeLong MR, Strick PL. (1986). Parallel organization of functionally segregated circuits linking basal ganglia and cortex. Annual Review of Neuroscience. 9:357-381. 【4機能ループ(運動・眼球運動・前頭前野・辺縁系)の原著】
- 6) Mink JW. (1996). The basal ganglia: focused selection and inhibition of competing motor programs. Progress in Neurobiology. 50(4):381-425. 【フォーカス型抑制(Focused Inhibition)モデルの原著】
- 7) Reiner A, et al. (1988). Differential loss of striatal projection neurons in Huntington disease. PNAS. 85(15):5733-5737. 【HD初期にエンケファリン陽性(間接路)ニューロンが選択的変性することの原著】
- 8) Frank MJ. (2006). Hold your horses: a dynamic computational role for the subthalamic nucleus in decision making. Neural Networks. 19(8):1120-1136.
- 9) Schultz W, Dayan P, Montague PR. (1997). A neural substrate of prediction and reward. Science. 275(5306):1593-1599. 【報酬予測誤差(RPE)とドーパミンの原著】
- 10) Aron AR, Poldrack RA. (2006). Cortical and subcortical contributions to Stop signal response inhibition: role of the subthalamic nucleus. J Neurosci. 26(9):2424-2433. 【ハイパー直接路と衝動抑制のfMRI原著】
- 11) Thaut MH, McIntosh GC, Rice RR, et al. (1996). Rhythmic auditory stimulation in gait training for Parkinson’s disease patients. Movement Disorders. 11(2):193-200. 【RASのRCT原著】
- 12) Morris ME, et al. (1994). Stride length regulation in Parkinson’s disease. Normalization strategies and underlying mechanisms. Brain. 117(Pt 5):1023-1039.
- 13) Nieuwboer A, et al. (2007). Cueing training in the home improves gait-related mobility in Parkinson’s disease: the RESCUE trial. J Neurol Neurosurg Psychiatry. 78(2):134-140. 【視覚・聴覚キューのRCT(RESCUE試験):すくみ足改善】
- 14) Ebersbach G, et al. (2010). Comparing LSVT-BIG and physiotherapy for people with Parkinson disease: a randomized clinical trial. Neurorehabilitation and Neural Repair. 24(2):193-201. 【LSVT-BIGのRCT原著】
- 15) Hackney ME, et al. (2007). Effects of tango on functional mobility in Parkinson’s disease: a preliminary study. J Neuroeng Rehabil. 4:11. 【タンゴダンスのRCT原著】
- 16) Deuschl G, et al. (2006). A randomized trial of deep-brain stimulation for Parkinson’s disease. NEJM. 355(9):896-908. 【STN-DBSの大規模RCT(L-DOPA 30-50%減量可能)】
- 17) Lanciego JL, Luquin N, Obeso JA. (2012). Functional Neuroanatomy of the Basal Ganglia. Cold Spring Harbor Perspectives in Medicine. 2(12):a009621.
- 18) Obeso JA, et al. (2008). The basal ganglia in Parkinson’s disease: current concepts and unexplained observations. Annals of Neurology. 64(S2):S30-S46.
大脳基底核の3経路を理解したら、
次は「どう介入するか」です。
直接路・間接路・ハイパー直接路の理論を臨床で活かす
根拠に基づいたリハビリプログラムをSTROKE LABでご相談ください。

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024) パーキンソン病の機能促進:医学書院 (2025)